Parodont und Allgemeingesundheit
Parodontitiden zählen zu den häufigsten Erkrankungen der Mundhöhle. Sie sind behandelbar, und ihrer etwaigen Identifizierung als Risikofaktor allgemeinmedizinischer Erkrankungen käme eine große präventivmedizinische Bedeutung zu. Ohne Intervention sind sie oftmals fortschreitend und nehmen in ihrem Verlauf an Komplexität zu. Unter Umständen beeinflussen sie die Fähigkeit zu essen und die Wahl der Speisen. Sie erzeugen Mundgeruch und beeinträchtigen das äußere Erscheinungsbild und die Kommunikationsfähigkeit eines Menschen (Abbildung 1) bis hin zu Einschränkungen seiner Arbeitsleistung und wirtschaftlichen Produktivität [Scannapieco 1998].
Als primäre Ursache für Parodontitiden gilt die mikrobielle Besiedelung der Mundhöhle, die den Boden für eine Vermehrung parodontalpathogener Keime bildet. Darüber hinaus ist ihre Ätiologie und Pathogenese jedoch multifaktoriell und wird durch ein komplexes Zusammenspiel angeborener, erworbener und verhaltensbedingter Faktoren determiniert. So zeigen zum Beispiel viele systemische Erkrankungen orale Symptome und beeinflussen direkt oder durch Nebenwirkungen ihrer Therapien den Verlauf oraler Erkrankungen. Auf der anderen Seite ist die Mundhöhle eine Eintrittspforte für Mikroorganismen in den Körper. Entzündungen im Bereich der Mundhöhle können daher auch Auswirkungen auf die Allgemeingesundheit haben. Die Ergebnisse von tierexperimentellen Untersuchungen [Chung et al. 2000, Brodala et al. 2001] sowie Querschnitts- beziehungsweise prospektive Longitudinalstudien unterschiedlichen Designs können als Indizien für einen Zusammenhang zwischen marginaler Parodontitis und Diabetes mellitus [Aldridge et al. 1995, Grossi et al. 1997, Kocher et al. 2001, Schwahn et al. 2001], Herz-Kreislauf-Erkrankungen [DeStefano et al. 1993, Beck et al. 1996], Schlaganfall, Schwangerschaftskomplikationen [Offenbacher et al. 1996, Offenbacher et al. 1998, Dasanayake et al. 2001a, Jeffcoat et al. 2001], Gastritiden und Atemwegsinfektionen angesehen werden. Es ist jedoch nicht geklärt, ob die Assoziationen oraler und allgemeiner Erkrankungen kausal oder koinzidentiell sind.
Allerdings mehren sich Hinweise darauf, dass Parodontitis als verursachender beziehungsweise modulierender Faktor für verschiedene Krankheiten fungiert [Slavkin und Baum 2000]. Die wichtigsten dieser Erkrankungen wurden in einem "Position Paper" der American Association for Periodontology vorgestellt (Abbildung 2) [Scannapieco 1998].
Akute und chronische Lungenerkrankungen
Die Mikroorganismen aus den supra- und subgingivalen Belägen der Zähne können auf verschiedenen Wegen in den Körper eindringen. So können sie zum Beispiel in den Respirationstrakt aspiriert werden und dort als potentielle Ursache für Pneumonien beziehungsweise chronisch obstruktive Lungenerkrankungen fungieren. Auf diese Weise können sie bei älteren Personen und Personen mit geschwächtem Immunsystem zu lebensbedrohlichen Zuständen führen. In einer Untersuchung an Patienten auf Intensivstationen und in Pflegeheimen kolonisierten Mikroorganismen in der dentalen Plaque, die für die Pathogenese von Erkrankungen des Respirationstraktes verantwortlich sind [Slots et al. 1988, Scannapieco et al. 1992]. Via Aspiration können diese Mikroorganismen zu rezidivierenden Pneumonien führen [Scannapieco und Genco 1999]. Dies gilt in erster Linie bei geschwächtem Immunsystem [Bentley 1984, Scannapieco und Mylotte 1996]. In Querschnittsstudien wurde bei Patienten mit schlechter Mundhygiene ein 4,5fach erhöhtes relatives Risiko für Pneumonien gefunden [Scannapieco und Mylotte 1996].
Bakteriämie
Eine weitere Eintrittspforte für die Bakterien der Mundhöhle besteht entlang der Zahnwurzel. Der Übergang von der Gingiva zur Zahnhartsubstanz ist die einzige Stelle im menschlichen Körper, an der unter physiologischen Bedingungen die Integrität des Epithels durchbrochen ist. Der Margo gingivae ist daher als Grenzfläche zwischen Weich- und Hartgeweben zu betrachten, die prädisponiert für das Eindringen von Mikroorganismen aus der Mundhöhle in das Körperinnere ist. Sie gelangen bei Verlust des epithelialen Attachments und parodontaler Taschenbildung entlang der Zahnwurzel in die Blutbahn und lösen eine Bakteriämie aus [Silver et al. 1977]. Dies kann bei jeder mechanischen Beanspruchung des Kauorgans geschehen. Dabei genügt neben der Extraktion von Zähnen und der professionellen Zahnreinigung, die den meisten Zahnärzten als
Bakteriämien verursachende Tätigkeiten geläufig sind, auch jede mechanische Plaque-Entfernung, zum Beispiel das Zähnebürsten sowie die Anwendung von Zahnseiden und Interdentalraumbürsten. Selbst das Kauen kann zu einer Bakteriämie führen. Die Häufigkeit des Auftretens einer Bakteriämie sinkt mit dem Entzündungsgrad der Gingiva und ist daher nicht nur in Abhängigkeit vom Ausmaß der mechanischen Beanspruchung beziehungsweise Traumatisierung der Gingiva zu betrachten [Silver et al. 1977]. Einige parodontalpathogene Keime besitzen außerdem die Fähigkeit, direkt in das parodontale Gewebe einzudringen [Allenspach-Petrzilka und Guggenheim 1983, Christersson et al. 1987, Meyer et al. 1991, Riviere et al. 1991] und möglicherweise auch ohne mechanischen Auslöser direkten Zugang zum Gefäßsystem zu erlangen. Bakteriämien sind bei gesunden Personen in der Regel unproblematisch. In Verbindung mit Bedingungen, die zu einer Veränderung der Abwehrlage entweder lokal oder systemisch führen, müssen Bakteriämien hingegen als potentielle Ursache für pathologische Prozesse bis hin zu lebensbedrohlichen Zuständen angesehen werden. Bei Patienten mit vorgeschädigtem Endokard oder Klappenersatz besteht zum Beispiel das Risiko einer Endokarditis, die sowohl akut als auch subakut verlaufen kann [Weinstein und Schlesinger 1974a, 1974b]. Die Mikroorganismen, die am häufigsten bei Endokarditiden gefunden werden, sind orale Streptokokken [Bayliss et al. 1983]. So wurde zum Beispiel im Blut von Patienten mit subakuter Endokarditis Streptococcus sanguis nachgewiesen, der in großer Zahl in supra- und subgingivaler Plaque vorzufinden ist [Kaye 1996]. Diese Mikroorganismen scheinen eine Affinität zu Thrombozytenansammlungen an Herzklappen zu haben. Sie können sich direkt an die Thrombozyten anlagern und durch kalziumunabhängige Mechanismen deren Aggregation fördern [Herzberg 1996, Herzberg und Meyer 1996]. Nach ihrer Adhärenz an Thrombozyten induzieren sie darüber hinaus den kalziumabhängigen Aggregationsmechanismus der Thrombozyten, was sowohl zur Ausbildung von Thromben [Herzberg und Meyer 1996] als auch zur Zunahme der endokardialen Thrombozytenansammlungen führen kann [Herzberg 1996]. Neben gram-positiven sind auch gram-negative Keime in der Lage, Endokarditiden auszulösen [Geraci und Wilson 1982]. Entsprechend der Empfehlungen mehrerer kardiologischer Gesellschaften ist daher vor zahnmedizinischen Eingriffen eine antibiotische Abschirmung bei Risikopatienten vorzunehmen [Barco 1991, Dajani und Taubert 1992]. Allerdings mehren sich die Stimmen, die davor warnen, dass die Antibiotikaprophylaxe lediglich das Ausmaß der Bakteriämie reduziere und nicht eine Bakteriämie vollständig verhindere. Bei Risikopatienten müsse daher vermehrt auf die Prävention oraler Erkrankungen geachtet werden, da dadurch das Bakteriämierisiko am effektivsten reduziert werde [Lockhart 2000].
Diese Zusammenhänge zwischen oralen Entzündungen und dem Risiko für Bakteriämien beziehungsweise Endokarditiden sind seit langem bekannt und gelten als gesichert. Neben diesem "akuten" Effekt besteht jedoch die Vorstellung, dass durch permanentes Eindringen von Keimen aus der mikrobiellen Plaque der Zähne (Abbildung 3) im Sinne einer chronisch rezidivierenden, klinisch nicht erkennbaren Bakteriämie ebenfalls Erkrankungen ausgelöst oder in ihrem Verlauf negativ beeinflusst werden [Beck et al. 1996, Rutkauskas 2000, Garcia et al. 2001].
Dazu zählen der Insulinbedarf bei Diabetikern oder kardiovaskuläre und zerebrovaskuläre Krankheiten. Außerdem werden Zusammenhänge zwischen marginalen Parodontitiden und Komplikationen während der Schwangerschaft beziehungsweise dem Risiko für Frühgeburten und geringes Geburtsgewicht diskutiert.
Diabetes mellitus
Akute Entzündungen führen zu Stoffwechselveränderungen, die bei Diabetikern zum Entgleisen des Blutzuckerspiegels führen können [Rayfeld et al. 1982]. Versuche an Ratten weisen darauf hin, dass bakterielle Infektionen die insulin-vermittelte Glukoseaufnahme der Skelettmuskulatur reduzieren [Lang 1992] und bakterielle Endotoxine sowie Entzündungsmediatoren die Insulinwirkung beeinträchtigen [Ling et al. 1994]. In longitudinalen Studien an Pima-Indianern fanden sich hohe Assoziationen zwischen Parodontitis und schlechten Blutzuckerspiegeln [Taylor et al. 1996, Taylor et al. 1998]. Vier Interventionsstudien, bei denen lediglich eine mechanische Parodontitistherapie durchgeführt wurde, zeigten jedoch übereinstimmend keinen Effekt auf die Kontrolle des Blutzuckerspiegels [Seppälä und Ainamo 1994, Aldridge et al. 1995, Smith et al. 1996, Christgau et al. 1998]. Drei weitere Studien, bei denen zusätzlich zur mechanischen Therapie Antibiotika eingesetzt wurden, berichten übereinstimmend über einen positiven Effekt der Parodontitistherapie auf die Kontrolle des Blutzuckerspiegels bei insulinpflichtigen Diabetikern [Williams und Mahan 1960, Miller et al. 1992, Grossi et al. 1997].
Komplikationen bei der Schwangerschaft
In Bezug auf geringes Geburtsgewicht und das Risiko für Frühgeburten finden sich ebenfalls Hinweise auf eine Assoziation mit Parodontitis. So wurde in einer Fall-Kontroll-Studie, an der 124 Personen teilnahmen, in einem multivariaten Modell eine Risikoerhöhung für geringes Geburtsgewicht bei Parodontitispatienten um den Faktor 7,9 gefunden [Offenbacher et al. 1996]. Allerdings gibt es viele gemeinsame Risikofaktoren für geringes Geburtsgewicht und Frühgeburt auf der einen und Parodontitis auf der anderen Seite, so dass eine kausale Beziehung derzeit nicht gesichert ist [Williams et al. 2000, Lopez et al. 2000]. Andere Studien finden keine Assoziation zwischen klinischen Zeichen der Parodontitis und dem Risiko für Frühgeburten [Curtis et al. 2001, Holbrook et al. 2001], wohl aber erhöhte Pegel von Bacteroides forsythus und Campylobacter rectus [Dasanayake et al. 2001a, Dasanayake et al. 2001b, Mitchell-Lewis et al. 2001].
Kardiovaskuläre Erkrankungen
Die erste systematische Studie, die sich mit dieser Thematik befasste, geht auf das Jahr 1963 zurück. In dieser Untersuchung wurden 60 Patienten mit Diabetes mellitus, 64 Personen mit Verdacht auf Diabetes mellitus, 54 Patienten ohne Diabetes mellitus aber mit Arteriosklerose und 74 gesunde Kontrollpersonen in Hinblick auf ihre oralen Verhältnisse analysiert. Die Autoren fanden, dass in der Gruppe der Arteriosklerose-Patienten 62 Prozent der Personen mehr Knochenabbau aufwiesen als die Kontrollpersonen. Der Unterschied war auf Grund der geringen Stichprobengröße nicht statistisch signifikant [Mackenzie und Millard 1963].
Eine finnische Arbeitsgruppe verglich 40 an Schlaganfall erkrankte Personen mit einem Alter unter 50 Jahren mit 40 zufällig ausgewählten, altersentsprechenden, gesunden Kontrollpersonen. Sie fand heraus, dass die männlichen Schlaganfall-Patienten einen statistisch signifikant schlechteren Zahnzustand aufwiesen als die männlichen Kontrollpersonen. Bei Frauen war der Unterschied nicht statistisch signifikant, was die Autoren zum einen auf die im Vergleich zu den Männern bessere Mundhygiene und zum anderen auf die viel geringere Stichprobengröße zurückführten. Bei der statistischen Auswertung im Rahmen dieser Studie erfolgte keine Adjustierung der dentalen Befunde für andere kardiovaskuläre oder zerebrovaskuläre Risikofaktoren [Syrjänen et al. 1989].
Im gleichen Jahr wurde eine Untersuchung publiziert, bei der der dentale Status von 100 Myokardinfarkt-Patienten mit 102 zufällig ausgewählten, altersgematchten, gesunden Kontrollpersonen verglichen wurde. Zu Grunde lag ein summativer Score, der Total Dental Index (TDI), der sowohl kariöse Läsionen als auch marginale Parodontitiden, apikale Parodontitiden und Perikoronitiden in sich vereint. Der TDI war bei den Patienten mit Myokardinfarkt statistisch signifikant höher als bei den Kontrollpersonen. Eine lineare logistische Regressionsanalyse wies den TDI als Risikofaktor aus, der unabhängig von Alter, Cholesterin- und Triglyceridspiegel, Bluthochdruck, Diabetes mellitus und Rauchen war [Mattila et al. 1989].
Dieselbe Arbeitsgruppe fand bei 100 Patienten mit Koronarangiographie in der multivariaten Analyse statistisch signifikante Assoziationen zwischen dentalen Infektionen, Triglyceriden sowie Alter und dem Auftreten von Atheromen in den Koronar-Arterien. Andere Risikofaktoren, wie Rauchen, Cholesterinspiegel, Bluthochdruck, Sozialstatus und "body mass index", waren nicht statistisch signifikant [Mattila 1993].
In einer anderen Untersuchung wurden Patienten mit marginaler Parodontitis und parodontal gesunde Kontrollpersonen in Hinblick auf Fibrinogenspiegel und Leukozytenanteile im Blut verglichen. Bei den Parodontitis-Patienten fanden sich statistisch signifikant höhere Fibrinogengehalte und Leukozytenanteile als bei den Kontrollpersonen. In der korrigierten multiplen Regressionsanalyse war der Gingivitis-Index mit Fibrinogen und Leukozytenanteilen im Blut assoziiert [Kweider et al. 1993].
Im selben Jahr wurden die Ergebnisse der ersten National Health and Nutrition Education Survey (NHANES I) publiziert. Die Baseline-Untersuchungen erfolgten in den Jahren 1971 bis 1974. Nach einem mittleren Zeitraum von 14 Jahren wurden 20 749 Personen im Alter zwischen 25 und 75 Jahren nachuntersucht. Die Autoren kamen zu dem Ergebnis, dass Patienten, die bei der Baseline-Untersuchung eine Parodontitis aufwiesen, ein um 25 Prozent erhöhtes Risiko hatten, an einer koronaren Herzkrankheit (KHK) zu erkranken. Bei Männern, die auf Grund ihrer Parodontitis alle Zähne verloren hatten, war das Risiko sogar um 70 Prozent erhöht. Das relative Risiko männlicher Parodontitis-Patienten für KHK betrug nach Adjustierung für Alter, Geschlecht, Rasse, Bildung, Prosperität, Familienstand, Blutdruck, Cholesterin, Diabetes mellitus, "body mass index", körperliche Betätigung, Alkohol- und Tabakkonsum 1,72 [DeStefano et al. 1993].
Diese Ergebnisse blieben jedoch nicht unwidersprochen. Eine andere Arbeitsgruppe fand auf der Basis des selben Datenmaterials durch ein multivariates Modell mit anderer Gewichtung der Risikofaktoren für koronare Herzkrankheit eine nicht statistisch signifikante und in ihrem Ausmaß nicht relevante Risikoerhöhung von 1,1 [Hujoel et al. 2000, Hujoel et al. 2001a, Hujoel et al. 2001b]. Diese Arbeitsgruppe kommt zu dem Schluss, dass keine kausalen Beziehungen zwischen Parodontitis und kardiovaskulären Erkrankungen bestehen und die gefundenen Assoziationen vollständig durch eine nicht angemessene Korrektur für gemeinsame Risikofaktoren, zum Beispiel Rauchen, zu erklären seien [Hujoel et al. 2000]. Das Datenmaterial, das beiden Publikationen zu Grunde liegt, stammt jedoch aus Studien, die in ihrem Design nicht zur Beantwortung dieser Fragestellungen geplant waren. Daher können sie lediglich Hinweise für oder gegen einen Zusammenhang zwischen Parodontitis und kardiovaskulären Erkrankungen geben. Darüber hinaus beruhen die Aussagen auf einem Parodontalbefund, der in keinem zeitlichen Verhältnis zur kardialen Erkrankung stand. Zudem basieren sie auf relativ groben Klassifizierungen sowohl für Parodontitis als auch für das Rauchverhalten. Daher ist die Aussagekraft dieser Publikationen unabhängig vom erzielten Ergebnis als eher gering einzustufen. In einer weiteren Studie wurden 1147 Personen aus der Dental Longitudinal Study (DLS), die im Jahr 1968 begann, retrospektiv nachuntersucht. Der mittlere Nachuntersuchungszeitraum betrug 18 Jahre. Die Autoren teilten die Personen nach ihrem anhand von Röntgenbildern bestimmten relativen Knochenabbau in Gruppen ohne Knochenverlust (n=74), mit Knochenabbau von 20 Prozent der Wurzellänge (n=812), 40 Prozent der Wurzellänge (n=199), 60 Prozent der Wurzellänge (n=31) und 80 Prozent der Wurzellänge (n=2) ein. Sie beschrieben eine kumulative Inzidenz von KHK von unter zehn Prozent in der Gruppe ohne Knochenabbau und bis über 35 Prozent in der Gruppe der Personen mit 60 Prozent relativem Knochenverlust (Abbildung 4). Auf Grund der geringen Stichprobengröße von zwei war die Gruppe mit 80 Prozent relativem Knochenverlust von der Analyse ausgeschlossen. Eine ähnliche kumulative Inzidenz fand sich für tödlich verlaufende KHK, wobei die Werte von zwei Prozent in der Gruppe ohne Knochenabbau bis 22 Prozent in der Gruppe mit 60-prozentigem relativen Knochenabbau reichten [Beck et al. 1996]. Die Autoren fassten in dieser Publikation darüber hinaus die bis zu diesem Zeitpunkt verfügbare Literatur zusammen und formulierten erstmals ein pathogenetisches Erklärungsmodell. Sie postulierten, dass das Vorhandensein eines genetisch bedingten hyperreaktiven Makrophagen-Phänotyps eine überschießende zellulär vermittelte Entzündungsreaktion auslöse, die sowohl den Abbau des marginalen Parodonts beschleunige, als auch intravasal die Destruktion der Gefäßintima bei Bakteriämien vorantreiben würde (Abbildung 5). Dadurch werde die Bildung atherosklerotischer Plaques begünstigt [Beck et al. 1996]. Allerdings gelten ähnliche Einschränkungen für die Interpretation dieser Ergebnisse wie bei der Analyse der Daten aus der NHANES I [DeStefano et al. 1993, Hujoel et al. 2000], so dass derzeit ein kausaler Zusammenhang zwischen Parodontitis und kardiovaskulären Erkrankungen nicht als gesichert eingeschätzt werden kann.
Zerebrovaskuläre Erkrankungen
Die Diskussion über einen potentiellen Zusammenhang zwischen zerebrovaskulären Ischämien und Infektionen ist nicht neu. Bereits 1897 kommt Siegmund Freud zu der Einschätzung, dass "in nahezu einem Drittel aller erworbenen Fälle von hemiplegischer Cerebrallähmung … die Lähmung gleichzeitig mit einer bekannten Infectionskrankheit des kindlichen Alters, auf der Höhe oder nach Ablauf derselben - als Nachkrankheit - aufgetreten" ist [Freud 1897].
Akute bakterielle oder virale Infektionen, wie bakterielle Meningitiden [Leiguarda et al. 1988, Pfister et al. 1992], Neuroborreliosen [May und Jabbari 1990], Herpes zoster am Hals oder im Gesicht [Bourdette et al. 1983], Rickettsien-Infektionen [Miller und Price 1978, Swain 1978] oder das Acquired Immunodeficiency Syndrome (AIDS) [Casado Naranjo et al. 1992], können Vaskulitiden und nachfolgend zerebrovaskuläre Ischämien verursachen. Akute Infektionen der Ohren, des Rachens oder der Nasennebenhöhlen fanden sich bei 72 Prozent von Kindern mit Schlaganfällen bei angiographisch nachgewiesenen Verschlüssen Hirn versorgender Arterien [Shillito 1964]. In einer anderen Untersuchung wurden bei 34 Prozent von Kindern unter 16 Jahren mit ischämischen Insulten Infektionen innerhalb der vorausgegangenen drei Wochen beschrieben, während in einer Kontrollgruppe altersgleicher ambulanter Patienten der Anteil nur elf Prozent betrug [Riikonen und Santavuori 1994].
Bei Fallberichten über mehrere Kinder und junge Erwachsene mit ischämischen Insulten nach Infektionen im Bereich von Tonsillen, Hals und Rachen fanden sich angiografisch Wandunregelmäßigkeiten der Arteria carotis interna und anderer intrakranieller Gefäße, die als Übergreifen der Entzündung auf die Gefäßwand aufgefasst wurden [Bickerstaff 1964]. Eine japanische Studie mit Infektionen bei zehn von 54 untersuchten Kindern mit ischämischen Insulten kommt zu dem Schluss, dass die Infektionen nicht auf den Hals oder Kopf beschränkt sein müssen [Satoh et al. 1991].
Auch bei jungen Erwachsenen finden sich Hinweise auf einen Zusammenhang zwischen ischämischen Insulten und Infektionen. So fanden sich bei 27 von 64 (42 Prozent) Personen mit ischämischen Insulten zwischen 16 und 40 Jahren Hinweise für eine kürzliche Infektion [Hindfelt und Nilsson 1977]. Erhöhte Antikörper-Titer gegen bakterielle Erreger traten in einer Gruppe gesunder Kontrollpersonen bei sechs von 68 (neun Prozent) Fällen auf, während sie bei Personen im Alter von bis zu 45 Jahren mit akutem ischämischem Insult in 15 von 34 (44 Prozent) Fällen gefunden wurden [Syrjänen et al. 1986]. Im Vergleich zwischen 54 konsekutiven Patienten mit ischämischen Insulten und 54 alters- und geschlechtsgematchten zufällig ausgewählten Kontrollpersonen berichtete die gleiche Arbeitsgruppe in der Gruppe der Patienten ein neunfach erhöhtes Auftreten von Infektionen - überwiegend bakterielle Infektionen der Atemwege - in den vier Wochen vor dem Schlaganfall beziehungsweise dem Untersuchungstermin gegenüber der Kontrollgruppe. In einer multivariaten Analyse unter Einbeziehung der Faktoren Serum-Triglyzeride, Hypertonus, Rauchen und vorausgegangene Alkoholintoxikation wurden Infektionen als signifikanter und unabhängiger Risikofaktor identifiziert [Syrjänen et al. 1988]. In zwei Studien konnte gezeigt werden, dass auch ohne Altersbegrenzung für den Einschluss in die Studie in der Gruppe der Patienten mit ischämischen Insulten im Vergleich zu einer Kontrollgruppe vermehrt akute Infektionen in der der Untersuchung vorausgehenden Woche auftraten [Grau et al. 1996, Grau et al. 1998].
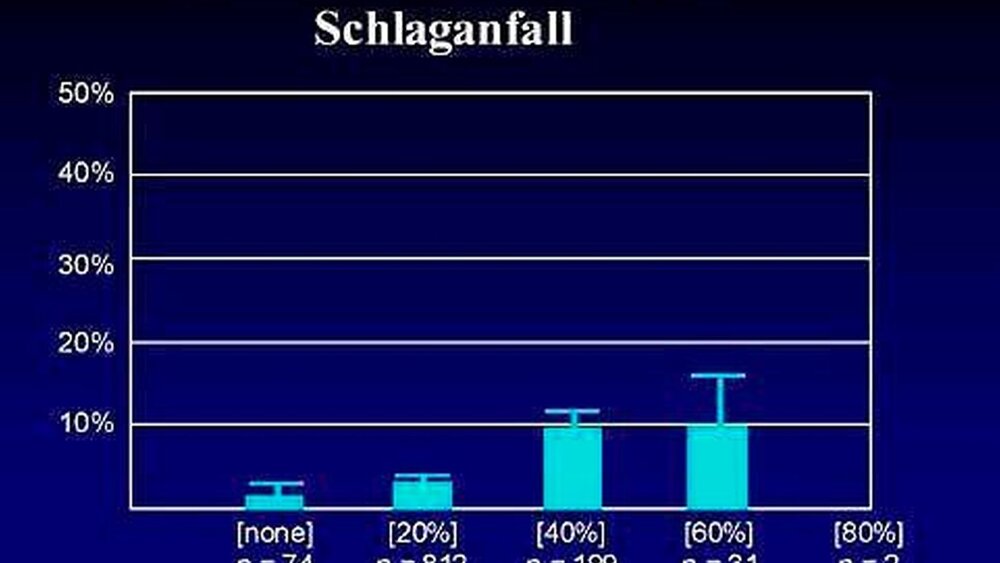
Auf Grund der post hoc Analyse der im Rahmen der NHANES I und ihren Nachfolgeuntersuchungen erhobenen longitudinalen Daten wurde eine Risikoerhöhung von 2,1 für Schlaganfall bei Vorliegen einer Parodontitis zum Zeitpunkt der Erstuntersuchung gefunden [Wu et al. 2000]. Auf der Basis der ebenfalls longitudinalen "National Ageing Study" (NAS) und der "Dental Longitudinal Study" (DLS) ergab sich für Schlaganfall eine maximale Inzidenz von unter zehn Prozent in der Gruppe mit 60-prozentigem relativen Knochenabbau (Abbildung 6). Analog zu den kardiovaskulären Erkrankungen stieg die Inzidenz für Schlaganfall mit steigendem Knochenabbau. Bei mehr als 20 Prozent Knochenabbau war in dieser Analyse das Risiko für einen Schlaganfall um den Faktor 2,8 erhöht [Beck et al. 1996].
In einer Pilotstudie, die 66 Patienten mit akuter zerebraler Ischämie und 60 alters- und geschlechtsgleiche Kontrollpatienten mit nicht-vaskulären neurologischen Erkrankungen umfasste, wurden auch chronische Infektionen des Hals-Nasen-Ohren-Bereichs sowie der Zähne und des Zahnhalteapparates erfasst. Als Maß für den Gesundheitszustand in der Mundhöhle wurde dabei der TDI gewählt, mit dessen Hilfe verschiedene entzündliche und nicht entzündliche Erkrankungen erfasst werden, die dann ungewichtet und unabhängig von ihrer Genese in die Indizierung eingehen [Mattila et al. 1989, Syrjänen et al. 1989]. Während in Bezug auf Infektionen des Nasen- und Rachenraums sowie der Ohren kein Unterschied zwischen den Gruppen ersichtlich war, wiesen die Patienten mit ischämischen Insulten im Vergleich zur Kontrollgruppe einen signifikant schlechteren TDI auf [Grau et al. 1997].
Vorläufige Analysen der auf dieser Pilotstudie aufbauenden Fall-Kontroll-Studie unterstützen ebenfalls die These, dass Parodontitis ein unabhängiger Risikofaktor für Schlaganfall ist [Dörfer et al. 2001]. Darüber hinaus konnte gezeigt werden, dass die Assoziation zwischen Parodontitis und Schlaganfall nicht ausschließlich durch die beiden Erkrankungen zu Grunde liegenden Risikofaktoren, wie Rauchen, zu erklären ist [Dörfer et al. 2002].
Abschließende Bewertung
Die Beurteilung eines möglicherweise kausalen Einflusses einer Parodontitis auf das Auftreten und den Verlauf systemischer Erkrankungen kann derzeit nicht abschließend erfolgen. Die derzeit vorliegenden Daten werden von verschiedenen Autoren teilweise unterschiedlich interpretiert. Darüber hinaus handelt es sich bei den bislang publizierten Untersuchungen um Querschnitts- und Longitudinalstudien, die nicht geeignet sind, einen Kausalzusammenhang aufzuzeigen. Dazu sind so genannte Interventionsstudien erforderlich, bei denen nachgewiesen wird, dass durch eine Parodontitistherapie das Auftreten der entsprechenden Allgemeinerkrankung reduziert oder die Erkrankung in ihrem Verlauf positiv beeinflusst wird. Solche Interventionsstudien sind derzeit nur für Diabetes mellitus publiziert. Sie konnten im Falle von ausschließlich mechanischer Parodontitis-Therapie keinen positiven Effekt auf den Stoffwechsel der Patienten mit Diabetes mellitus aufzeigen. Lediglich in Kombination mit systemischer Antibiotika-Gabe, die Auswirkungen auf den Gesamtorganismus und nicht nur auf das Parodont hat, konnte ein positiver Effekt gefunden werden. Interventionsstudien für kardio- und zerebrovaskuläre Erkrankungen sind ungleich aufwändiger und erfordern wesentlich längere Laufzeiten als für Diabetes mellitus. Daher ist nicht zu erwarten, dass sich bezüglich dieser Erkrankungen der Erkenntnisstand in näherer Zukunft wesentlich verbessern wird. Praktische Konsequenzen aus der Assoziation zwischen Parodontitis und kardio-, beziehungsweise zerebro-vaskulären Erkrankungen für die Patientenversorgung sind daher ebenfalls derzeit nicht zu erwarten. In Bezug auf Bakteriämien ergibt sich allerdings, dass gerade bei Patienten mit einem erhöhten Bakteriämierisiko in besonderer Weise auf Vermeidung intraoraler Entzündungen zu achten ist. Bei ihnen besteht besonders die Notwendigkeit, durch Schulung zu einer optimalen Mundhygiene und konsequenter Individualprophylaxe die intraorale Plaque möglichst gering zu halten und das Bakteriämierisiko auf diese Weise zu minimieren.
Dr. med. dent. Christof Dörfer
Universitätszahnklinik für Mund-, Zahn- und Kieferkrankheiten Heidelberg
Im Neuenheimerfeld 400
69120 Heidelberg
Literaturverzeichnis
Aldridge JP, Lester V, Watts TL, Collins A, Viberti G, Wilson RF (1995). Single-blind studies of the effects of improved periodontal health on metabolic control in type 1 diabetes mellitus. J Clin Periodontol, 22:271-275.
Allenspach-Petrzilka GE, Guggenheim B (1983). Bacterial invasion of the periodontium; an important factor in the pathogenesis of periodontitis? J Clin Periodontol, 10:609-617.
Barco CT (1991). Prevention of infective endocarditis: a review of the medical and dental literature. J Periodontol, 62:510-523.
Bayliss R, Clarke C, Oakley C, Somerville W, Whitfield AG (1983). The teeth and infective endocarditis. Br Heart J, 50:506-512.
Beck J, Garcia R, Heiss G, Vokonas PS, Offenbacher S (1996). Periodontal disease and cardiovascular disease. J Periodontol, 67:1123-1137
Bentley DW (1984). Bacterial pneumonia in the elderly: clinical features, diagnosis, etiology, and treatment. Gerontology:297-307.
Bickerstaff ER (1964). Aetiology of acute hemiplegia in Childhood. Brit Med J, 11:82-87.
Bourdette DN, Rosenberg NL, Yatsu FM (1983). Herpes zoster ophthalmicus and delayed ipsilateral cerebral infarction. Neurology, 33:1428-1432.
Brodala N, Madianos PN, Geva S, Offenbacher S, Beck JD, Fisher T, Smith S, Bellinger DA, Nichols TC (2001). Recurrent Porphyromonas gingivalis bacteremia induces atherosclerosis in susceptible pigs. American Academy of Periodontology and National Institute of Dental and Craniofacial Research.The periodontal-systemic connection: A state-of-the-science symposium, Bethesda, U.S.A.
Casado Naranjo I, Toledo Santos JA, Antolin Rodriguez MA (1992). Ischemic stroke as the sole manifestation of human immunodeficiency virus infection. Stroke, 23:117-118.
Christersson LA, Albini B, Zambon JJ, Wikesjo UM, Genco RJ (1987). Tissue localization of Actinobacillus actinomycetemcomitans in human periodontitis. I. Light, immunofluo-rescence and electron microscopic studies. J Periodontol, 58:529-539.
Christgau M, Palitzsch KD, Schmalz G, Kreiner U, Frenzel S (1998). Healing response to non-surgical periodontal therapy in patients with diabetes mellitus: clinical, microbiological, and immunologic results. J Clin Periodontol, 25:112-124
Chung HJ, Champagne CME, Southerland JH, Geva S, Liu Y, Paquette DW, Madianos PN, Beck JD, Offenbacher S (2000). Effects of P. gingivalis infection on atheroma formation in ApoE(+/-) Mice. J Dent Res, 79 (Spec. Iss.):313 (Abstract Nr. 1358).
Curtis M, Davenport E, Williams C, Sterne J, Murad S (2001). East London study of periodontal disease and preterm low birthweight. American Academy of Periodontology and National Institute of Dental and Craniofacial Research. The periodontal-systemic connection: A state-of-the-science symposium, Bethesda, U.S.A.
Dajani AS, Taubert KA (1992). Re: Letter to the editor by Dr. Steven M. Pollack and author's response from Drs. Thomas J. Pallasch and Jorgen Slots. Committee on Rheumatic Fever, Endocarditis, and Kawasaki Disease of the American Heart Association. J Periodontol, 63:488.
Dasanayake AP, Boyd C, Forster T, Hill E (2001a). Periodontal pathogen sprecific maternal serum immunglobulin level may predict low birth weight. American Academy of Periodontology and National Institute of Dental and Craniofacial Research. The periodontal-systemic connection: A state-of-the-science symposium, Bethesda, U.S.A.
Dasanayake AP, Boyd D, Madianos PN, Offenbacher S, Hills E (2001b). The association between Porphyromonas gingivalis-specific maternal serum IgG and low birth weight. J Periodontol, 72:1491-1497.
DeStefano F, Anda RF, Kahn HS, Williamson DF, Russell CM (1993). Dental disease and risk of coronary heart disease and mortality. Bmj, 306:688-691
Dörfer CE, Kaiser C, Lichy C, Buggle F, Becher H, Grau AJ, Ziegler CM (2002). Association between Periodontitis and Ischemic Stroke in Never Smokers. J Dent Res, 81:(Abstract in press).
Dörfer CE, Kaiser C, Lichy C, Buggle F, Ziegler CM, Becher H, Grau AJ (2001). Association between Periodontitis and Ischemic Stroke. American Academy of Periodontology and National Institute of Dental and Craniofacial Research. The periodontal-systemic connection: A state-of-the-science symposium, Bethesda, U.S.A.
Freud S (1897). Die infantile Cerebrallähmung. In: Specielle Pathologie 9, Teil 3 (1. Hälfte). H N editor. Wien: Holder, pp. 1-327.
Garcia RI, Henshaw MM, Krall EA (2001). Relationship between periodontal disease and systemic health. Periodontology 2000:21-36.
Geraci JE, Wilson WR (1982). Symposium on infective endocarditis. III. Endocarditis due to gram-negative bacteria. Report of 56 cases. Mayo Clin Proc, 57:145-148
Grau AJ, Buggle F, Becher H, Werle E, Hacke W (1996). The association of leukocyte count, fibrinogen and C-reactive protein with vascular risk factors and ischemic vascular diseases. Thromb Res, 82:245-255.
Grau AJ, Buggle F, Becher H, Zimmermann E, Spiel M, Fent T, Maiwald M, Werle E, Zorn M, Hengel H, Hacke W (1998). Recent bacterial and viral infection is a risk factor for cerebrovascular ischemia: clinical and biochemical studies. Neurology, 50:196-203.
Grau AJ, Buggle F, Ziegler C, Schwarz W, Meuser J, Tasman A-J, Bühler A, Benesch C, Becher H, Hacke W (1997). Association between acute cerebrovascula ischemia and chronic and recurrent infection. Stroke, 28:1724-1729.
Grossi SG, Skrepcinski FB, DeCaro T, Robertson DC, Ho AW, Dunford RG, Genco RJ (1997). Treatment of periodontal disease in diabetics reduces glycated hemoglobin. J Periodontol, 68:713-719.
Herzberg MC (1996). Platelet-streptococcal interactions in endocarditis. Crit Rev Oral Biol Med, 7:222-236.
Herzberg MC, Meyer MW (1996). Effects of oral flora on platelets: possible consequences in cardiovascular disease. J Periodontol, 67:1138-1142.
Hindfelt B, Nilsson O (1977). Brain infarction in young adults with particular reference to pathogenesis. Acta Nerol Scand, 55:145-157.
Holbrook WP, Óskarsdóttir Á, Frîjónsson T, Einarsson H, Hauksson A, Geirsson RT (2001). Oral, periodontal, and gynecological findings in pregnant women in Iceland. American Academy of Periodontology and National Institute of Dental and Craniofacial Research. The periodontal-systemic connection: A state-of-the-science symposium, Bethesda, U.S.A.
Hujoel PP, Drangsholt M, Spiekerman C, DeRouen TA (2000). Periodontal disease and coronary heart disease risk. J Am Med Assoc, 284:1406-1410.
Hujoel PP, Drangsholt M, Spiekerman C, Derouen TA (2001a). Examining the link between coronary heart disease and the elimination of chronic dental infections. J Am Dent Assoc, 132:883-889.
Hujoel PP, Drangsholt MT, Spiekerman C, DeRouen TA (2001b). Periodontal disease and risk of coronary heart disease. J Am Med Assoc, 285:40-41.
Jeffcoat MK, Geurs NC, Reddy MS, Cliver SP, Goldenerg RL, Hauth JC (2001). Periodontal infection and preterm birth: results of a prospective study. J Am Dent Assoc, 132:875-880.
Kaye D (1996). Treatment of infective endocarditis. Ann Intern Med, 124:606-608.
Kocher T, Schwahn C, Hensel E, Jüdemann J, John U (2001). Association between periodontal disease and lipoproteins. American Academy of Periodontology and National Institute of Dental and Craniofacial Research. The periodontal-systemic connection: A state-of-the-science symposium, Bethesda, U.S.A.
Kweider M, Lowe GD, Murray GD, Kinane DF, McGowan DA (1993). Dental disease, fibrinogen and white cell count; links with myocardial infarction? Scott Med J, 38:73-74.
Lang CH (1992). Sepsis-induced insulin resistance in rats is mediated by a beta-adrenergic mechanism. Am J Physiol, 263 (Suppl.):E703-E711.
Leiguarda R, Berthier M, Starkstein S, Nogués M, Lylyk P (1988). Ischemic infarction in 25 children with tuberculous meningitis. Stroke, 19:200-204.
Ling PR, Bistrian BR, K.W. M, Istfan NW (1994). Effects of systemic infusions of endotoxin, tumor necrosis factor, and interleukin-1 on glucose metabolism in the rat: relationship to endogenous glucose production and peripheral tissue glucose uptake. Metab Clin Exp, 43:279-284.
Lockhart PB (2000). The risk for endocarditis in dental practice. Periodontol, 23:127-135.
Mackenzie RS, Millard HD (1963). Interrelated effects of diabetes, arteriosclerosis and calculus on alveolar bone loss. J Am Dent Assoc, 66:192-198.
Mattila KJ (1993). Dental infections as a risk factor for acute myocardial infarction. Eur Heart J, 14 Suppl K:51-53.
Mattila KJ, Nieminen MS, Valtonen VV, Rasi VP, Kesämiemi YA, Syrjälä SL, Jungell PS, Isoluoma M, Hietaniemi K, Jokinen MJ, Huttunen JK (1989). Association between dental health and acute myocardial infarction. Brit Med J, 298:779-781.
May EF, Jabbari B (1990). Stroke in Neuroborreliosis. Stroke, 21:1232-1235
Meyer DH, Sreenivasan PK, Fives-Taylor PM (1991). Evidence for invasion of a human oral cell line by Actinobacillus actinomycetemcomitans. Infect Immun, 59:2719-2726.
Miller JQ, Price TR (1978). Tick-borne typhus including Rocky Mountain spotted fever. In: Handbook of neurology Vol 34: Infections of the nervous system. Part II. Vinken PJ, Bruyn GW,Klawans HL editors. Amsterdam: North Holland, pp. 651-658.
Miller LS, Manwell MA, Newbold D, Reding ME, Rasheed A, Blodgett J, Kornman KS (1992). The relationship between reduction in periodontal inflammation and diabetes control: a report of 9 cases. J Periodontol, 63:843-848.
Mitchell-Lewis D, Engebretson SP, Chen J, Lamster IB, Papapanou PN (2001). Periodontal infections and pre-term birth: early findings from a cohort of young minority women in New York. Eur J Oral Sci, 109:34-39.
Offenbacher S, Beck JD, Lieff S, Slade G (1998). Role of periodontitis in systemic health: spontaneous preterm birth. J Dent Educ, 62:852-858.
Offenbacher S, Katz V, Fertik G, Collins J, Boyd D, Maynor G, McKaig R, Beck J (1996). Periodontal infection as a possible risk factor for preterm low birth weight. J Periodontol, 67:1103-1113.
Pfister HW, Borasio GD, Dirnagl U, Bauer M, Einhäupl KM (1992). Cerebrovascular complications in bacterial meningitis in adults. Neurology, 42:1497-1504.
Rayfeld EJ, Ault MJ, Keush GT, Brothers MJ, Nechemias C, Smith H (1982). Infection and diabetes: the case for glucose control. Am J Med, 72:439-450.
Riikonen R, Santavuori P (1994). Hereditary and acquired risk factors for childhood stroke. Neuropediatr, 25:227-233.
Riviere GR, Weisz KS, Adams DF, Thomas DD (1991). Pathogen-related oral spirochetes from dental plaque are invasive. Infect Immun, 59:3377-3380.
Rutkauskas JS (2000). The medical necessity of periodontal care. Periodontology 2000:151-156.
Satoh S, Shirane R, Yoshimoto T (1991). Clinical survey of ischemic cerebrovascular disease in children in a district of Japan. Stroke, 22:586-589.
Scannapieco FA (1998). Position paper of The American Academy of Periodontology: periodontal disease as a potential risk factor for systemic diseases. J Periodontol, 69:841-850.
Scannapieco FA, Genco RJ (1999). Association of periodontal infections with atherosclerotic and pulmonary diseases. J Periodontal Res, 34:340-345.
Scannapieco FA, Mylotte JM (1996). Relationships between periodontal disease and bacterial pneumonia. J Periodontol, 67:1114-1122.
Scannapieco FA, Stewart EM, Mylotte JM (1992). Colonization of dental plaque by respiratory pathogens in medical intensive care patients. Crit Care Med, 20:740-745.
Schwahn C, Kocher T, Hensel E, Jüdemann J, John U (2001). Association between periodontal disease and coronary heart disease. American Academy of Periodontology and National Institute of Dental and Craniofacial Research. The periodontal-systemic connection: A state-of-the-science symposium, Bethesda, U.S.A.
Seppälä B, Ainamo J (1994). A site-by-site follow-up study on the effect of controlled versus poorly controlled insulin-dependent diabetes mellitus. J Clin Periodontol, 21:161-165.
Shillito J (1964). Carotid arteritis: a cause of hemoplegia in childhood. J Nerosurg, 21:540-551.
Silver JG, Martin AW, McBride BC (1977). Experimental transient bacteraemias in human subjects with varying degrees of plaque accumulation and gingival inflammation. J Clin Periodontol, 4.
Slavkin HC, Baum BJ (2000). Relationship of dentall and oral pathology to systemic illness. J Am Med Assoc, 248:1215-1217.
Slots J, Rams TE, Listgarten MA (1988). Yeasts, enteric rods and pseudomonads in the subgingival flora of severe adult periodontitis. Oral Microbiol Immunol, 3:47-52.
Smith GT, Greenbaum CJ, Johnson BD, Persson GR (1996). Short-term responses to periodontal therapy in insulin-dependent diabetic patients. J Periodontol, 67:794-802.
Swain RHA (1978). Rickettsial infections. In: Handbook of neurology Vol 34: Infections of the nervous system. Part II. Vinken PJ, Bruyn GW,Klawans HL editors. Amsterdam: North Holland, pp. 641-649.
Syrjänen J, Peltola J, Valtonen V, Iivanainen M, Kaste M, Huttunen JK (1989). Dental infections in association with cerebral infarction in young and middle-aged men. J Intern Med, 225:179-184.
Syrjänen J, Valtonen VV, Iivanainen M, Hovi T, Malkamäki M, Mäkelä PH (1986). Association between cerebral infarction and increase serum bacterial antibody levels in young adults. Acta Neurol Scand, 73:273-278.
Syrjänen J, Valtonen VV, Iivanainen M, Kaste M, Huttunen JK (1988). Preceding infection as an important risk factor for ischaemic brain infarction in young and middle aged patients. Brit Med J, 296:1156-1160.
Taylor GW, Burt BA, Becker MP, Genco RJ, Shlossman M (1998). Glycemic control and alveolar bone loss progression in type 2 diabetes. Ann Periodontol, 3:30-39.
Taylor GW, Burt BA, Becker MP, Genco RJ, Shlossman M, Knowler WC, Pettitt DJ (1996). Severe periodontitis and risk for poor glycemic control in patients with non-insulin-dependent diabetes mellitus. J Periodontol, 67:1085-1093.
Weinstein L, Schlesinger JJ (1974a). Pathoanatomic, pathophysiologic and clinical correla-tions in endocarditis (first of two parts). N Engl J Med, 291:832-837.
Weinstein L, Schlesinger JJ (1974b). Pathoanatomic, pathophysiologic and clinical correlations in endocarditis (second of two parts). N Engl J Med, 291:1122-1126.
Williams CE, Davenport ES, Sterne JA, Sivapathasundaram V, Fearne JM, Curtis MA (2000). Mechanisms of risk in preterm low-birthweight infants. Periodontol, 23:142-150.
Williams R, Mahan C (1960). Periodontal disease and diabetes in young adults. J Am Med Assoc, 172:776-778.
Wu T, Trevisan M, Genco RJ, Dorn JP, Falkner KL, Sempos CT (2000). Periodontal disease and risk of cerebrovascular disease: the first national health and nutrition examination survey and its follow-up study. Arch Intern Med, 160:2749-2755.