Polymorphes Adenokarzinom des Oberkiefers
Anamnese
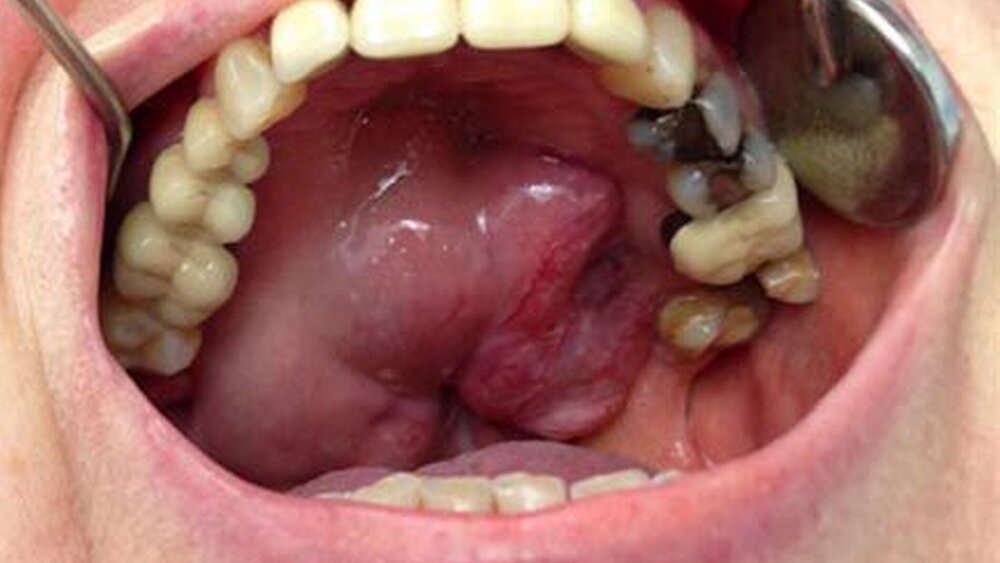
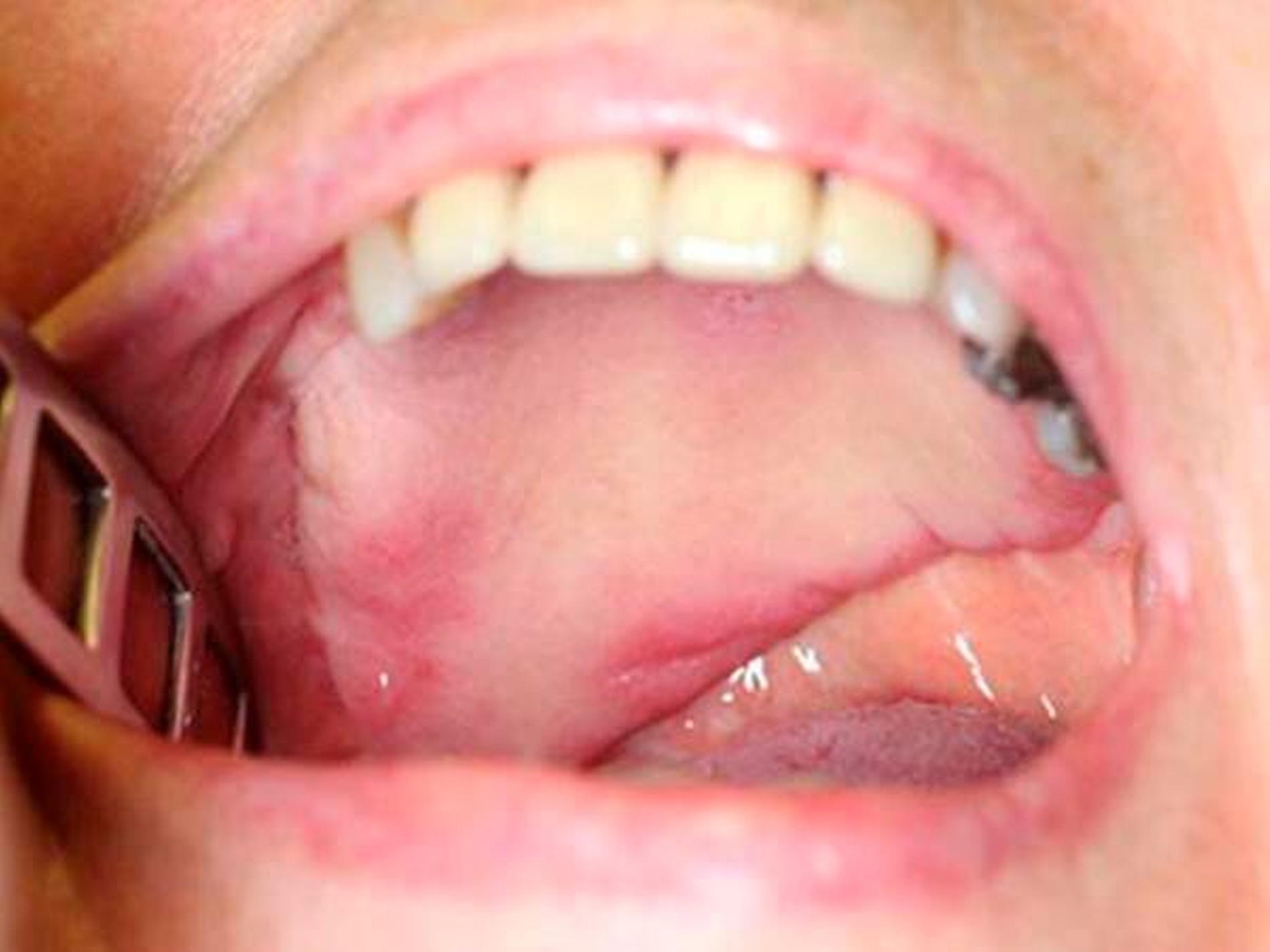
Die Frau stellte sich mit einer großen intraoralen harten, nicht ulcerierenden Vorwölbung des Gaumendachs vor. Sie gab an, bereits vor circa 30 Jahren sei die Diagnose eines kleinen, gutartigen Speicheldrüsentumors im Bereich des harten Gaumens durch eine Gewebeprobe gestellt worden. Damals hatte sie jegliche Therapieoptionen verweigert und auf ein abwartendes Verhalten bestanden.
Mittlerweile war der Tumor verdrängend nach kranial bis in die Nasenhaupthöhle und nach kaudal in die Mundhöhle teilweise bis auf das Niveau der Okklussionsebene gewachsen. Der extraorale Befund war gänzlich unauffällig.
Die Patientin war schmerzfrei, dennoch führte eine zunehmende Nasenatmungsbehinderung sowie eine kloßige Sprache letztendlich zu dem Therapiewunsch der Tumorentfernung.
Diagnostik
Alio loco wurde hierzu eine ausreichend große Biopsie entnommen, welche histologisch ein pleomorphes Adenom ergab.
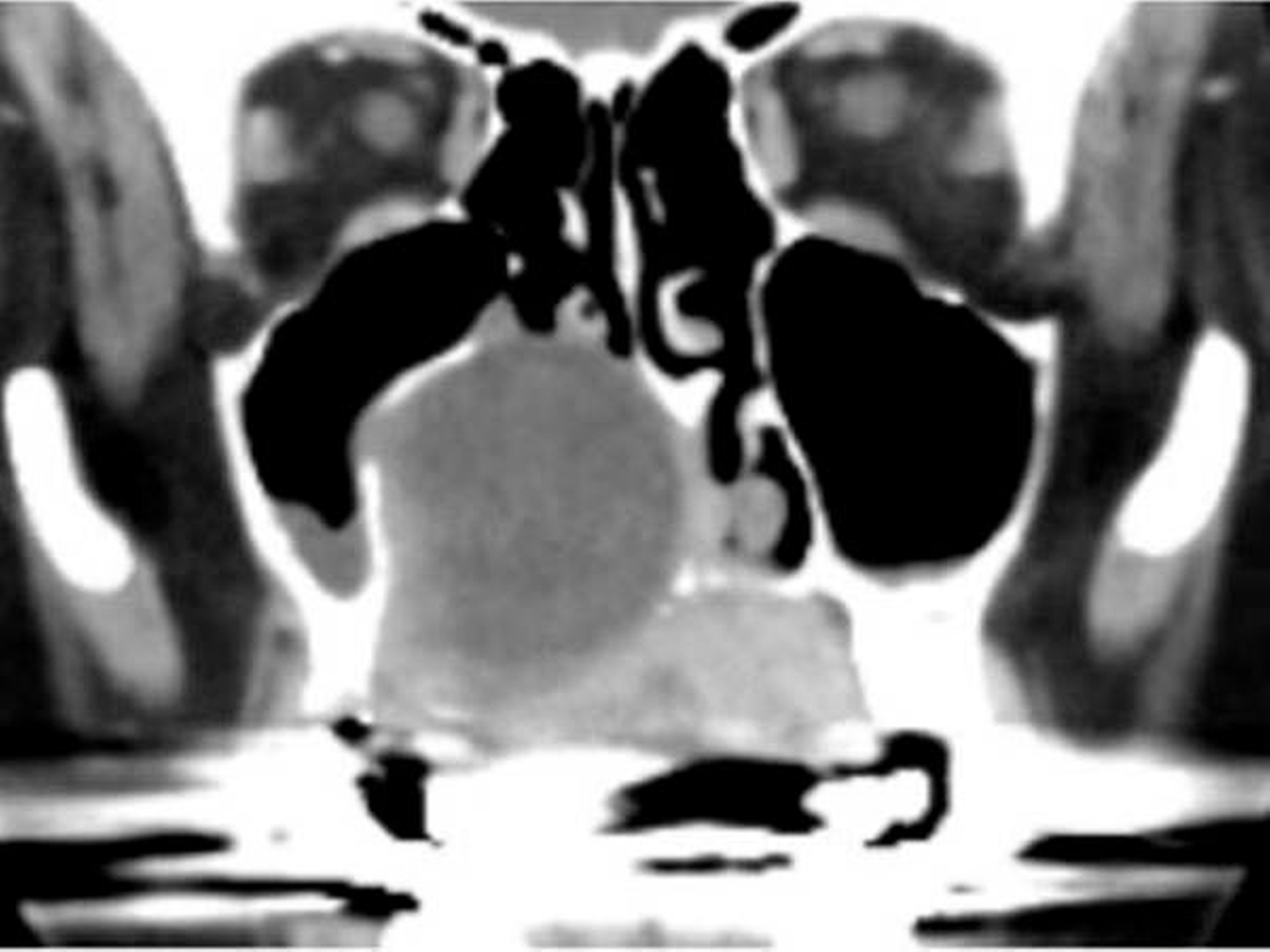
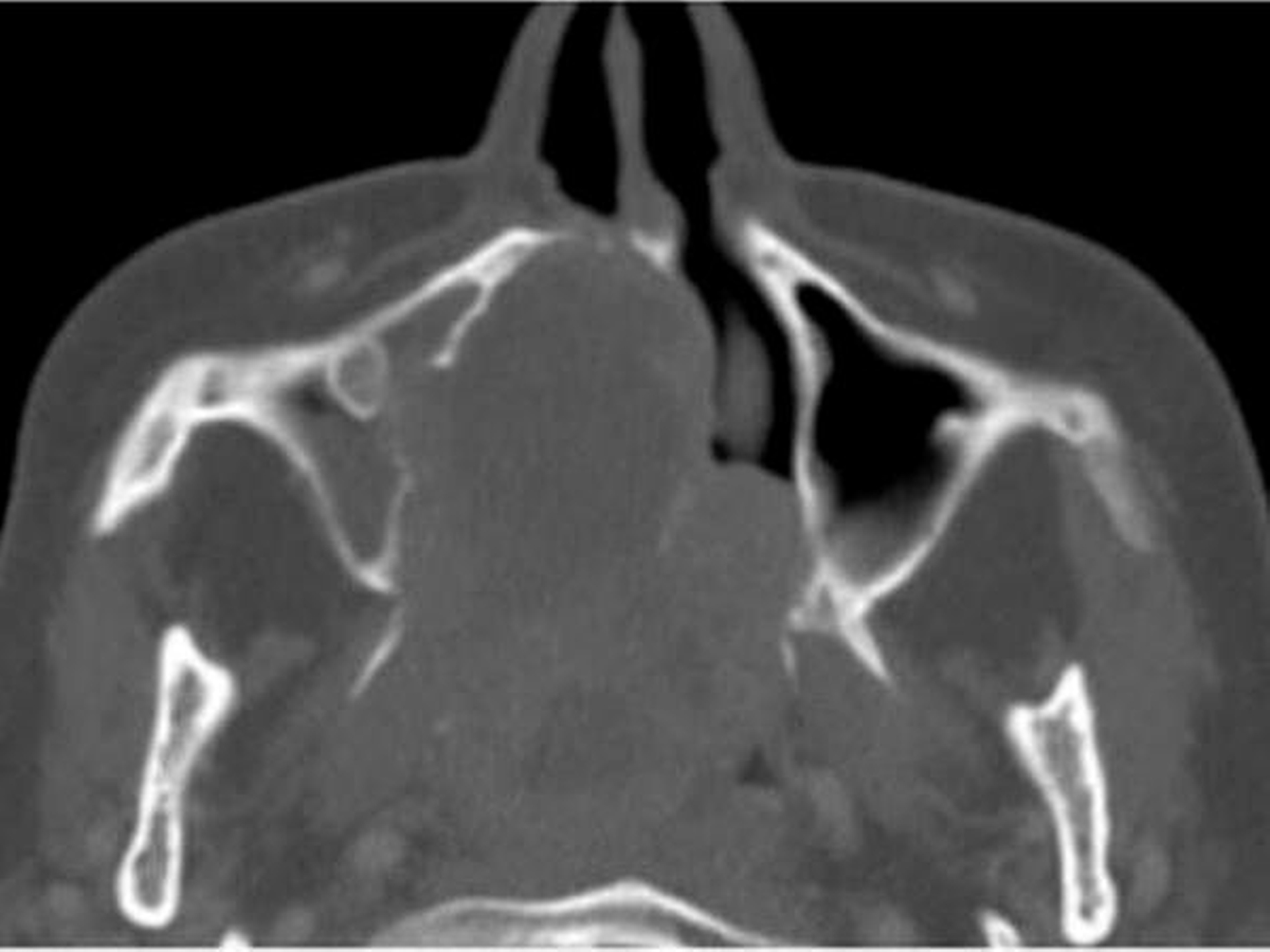
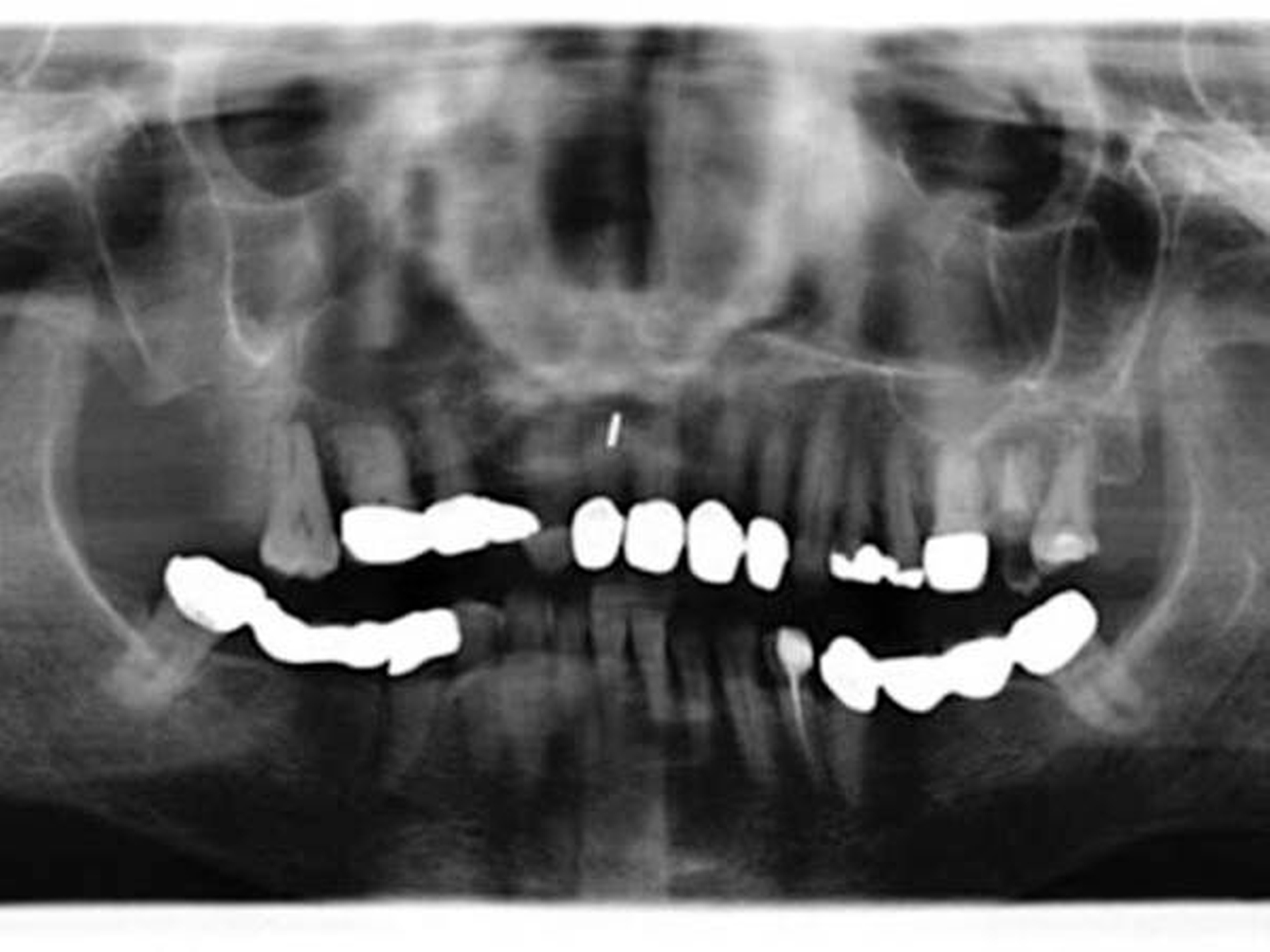
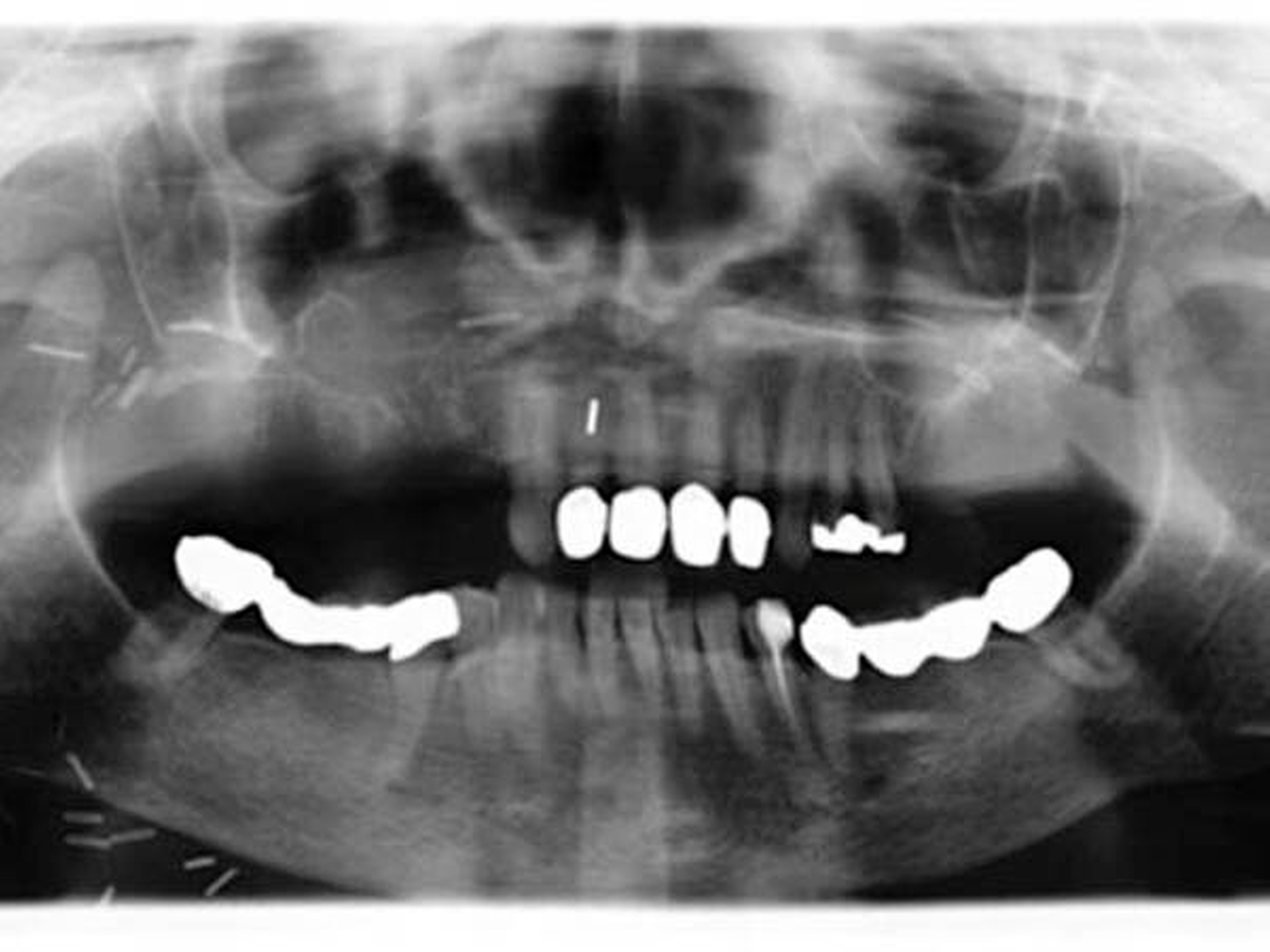
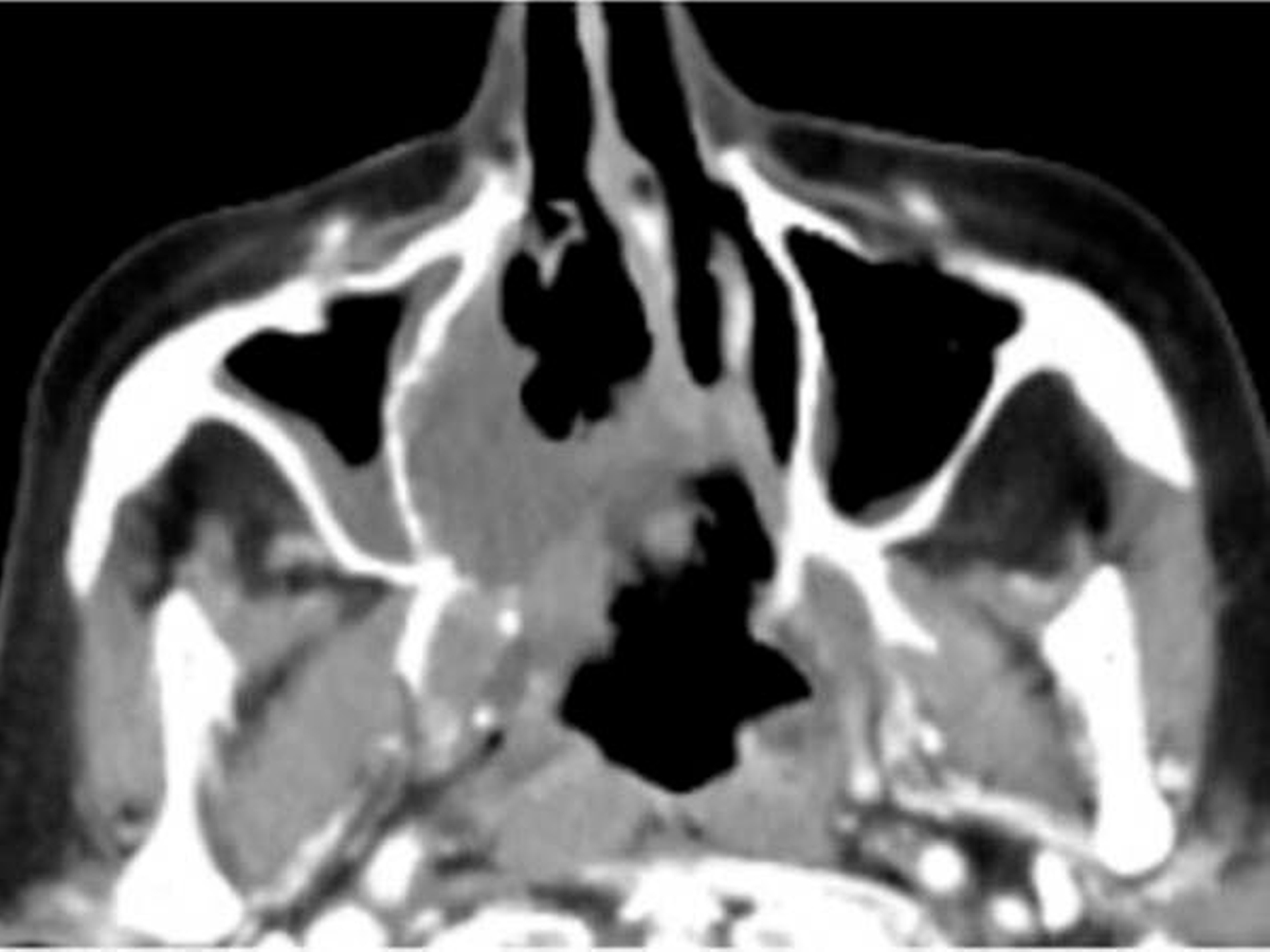
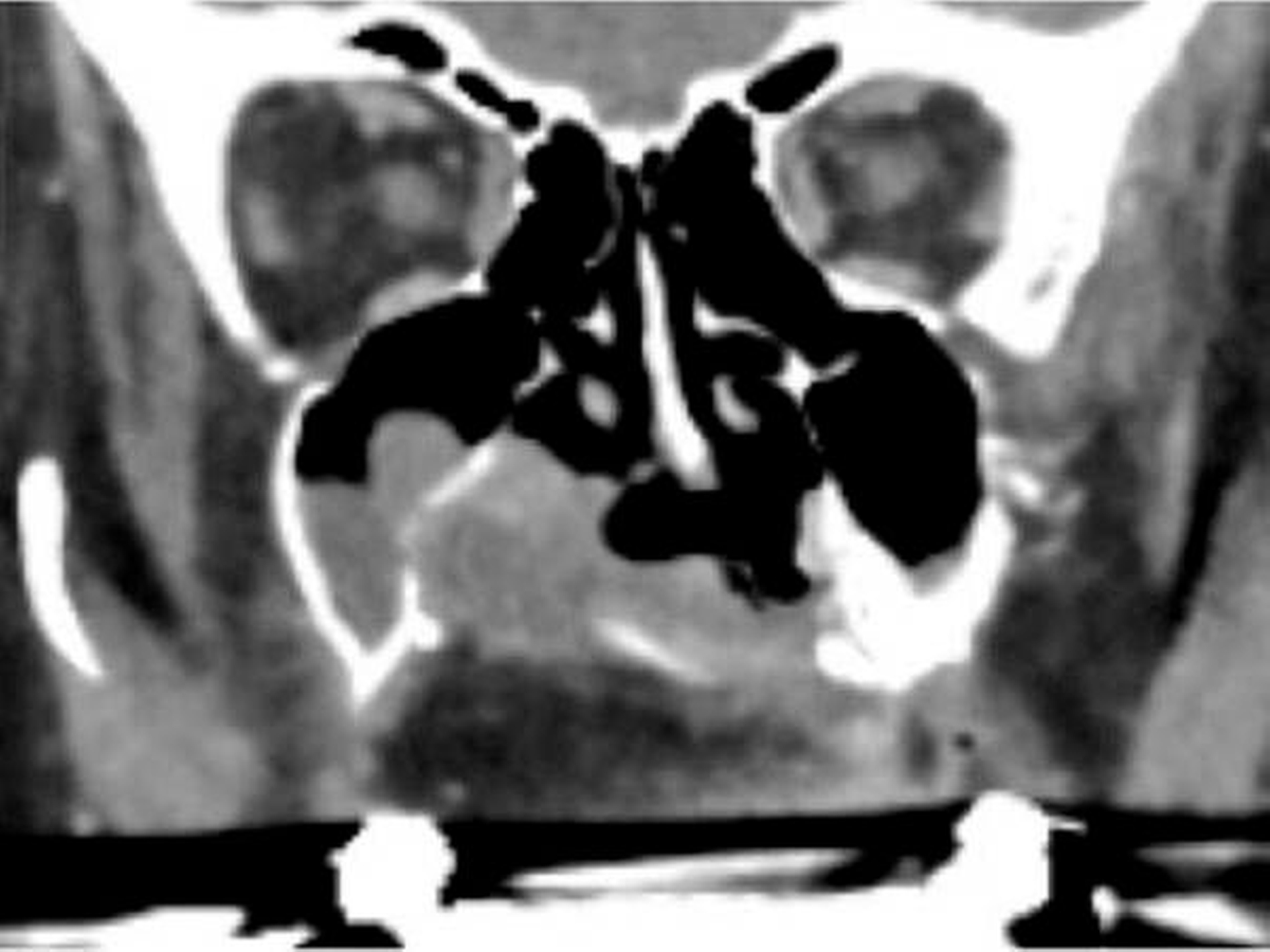
Die computertomografische Bildgebung zeigte eine inhomogene, kontrastmittelanreichernde und mittellinienüberschreitende Raumforderung im Bereich des Gaumens, die kaudal in die Mundhöhle und kranial in das Cavum nasi reichte. Die Größenausdehnung betrug circa axial 67 x 56 x kraniokaudal 52 mm.
Der Tumor wies multiple hypodense Anteile und einzelne Kalzifikationen auf. Die rechte Maxilla war distal der Regio 24 destruiert. Auch das Palatum durum et molle zeigten beidseits (rechtsbetont) Osteolysen bei primär verdrängendem Charakter auf. Der Nasopharynx war subtotal verlegt, die Uvula, der rechte M. constrictor pharyngis superior und beide Choanen nicht mehr abgrenzbar.
Der Tumor ragte durch die mediale Begrenzung des rechten Sinus maxillaris in die Nasenhaupthöhle mit einer hauchdünnen knöchernen Begrenzung. Rechts reichte die Raumforderung bis in die Fossa pterygoidea. Die Processus pterygoidei waren zentral aufgelöst. Rechtsseitig war die Anzahl der Lymphknoten in Level Ib und IIa/b vermehrt und moderat vergrößert, aber ohne klare Malignitätskriterien.
Bei der Patientin bestanden außer einer leichten arteriellen Hypertonie keine weiteren Vorerkrankungen und ebenso keine B-Symptomatik.
Nach Vorstellung im interdisziplinären Tumorboard wurde der Beschluss zur primären Tumoroperation mit Rekonstruktion in Intubationsnarkose getroffen.
Therapie
Nach Anlage eines temporären Tracheostomas und Neck Dissection Level I-III rechts erfolgte die Tumorexzision von transoral via midfacial degloving. So konnte auf eine extraorale Erweiterung des Zugangswegs nach Weber-Dieffenbach verzichtet werden.
Insgesamt wurden die Zähne 15 bis 17 und 26 bis 28 mit entfernt, und die Defektausdehnung umfasste somit eine distale Zweidrittel-Maxillektomie, also rechts ab Zahn 14 und links ab Zahn 26 nach distal mit Resektion bis in die Fossa pterygopalatina.
Es erfolgte die Unterbindung beider Aa. palatinae majores des kaudalen Septums. Nach kranial hin konnte die CT-radiologisch schon sichtbare knöcherne Begrenzung ausgeschält werden, so dass Anteile des kranialen Septums und der medialen Kieferhöhlenwände verbleiben konnten.
Die Defektdeckung erfolgte mit einem mikrovaskulären Radialistransplantat vom linken Unterarm. Arterielles Anschlussgefäß war die rechte A. thyroidea superior. Der venöse Abfluss wurde über eine Anastomose beider Vv. comitantes in einen direkten Venenbaum der V. jugularis interna gewährleistet. Der Defekt am linken Unterarm wurde mit einem Vollhauttransplantat aus der linken Leiste gedeckt und mit einem Vakuumverband über sieben Tage versorgt. Die Entnahmestelle an der Leiste wurde nach moderater Mobilisation primär verschlossen.
Der postoperative Verlauf der Patientin gestaltete sich problemlos. Die Trachealkanüle konnte nach Abschwellen am dritten postoperativen Tag entfernt werden. Schlucken und Sprechen waren sofort gut möglich. Das Lappentransplantat war zu jeder Zeit gut vaskularisiert und seine Grenzen dicht. Die Nasenatmung war nicht mehr gestört.
Die Frage, ob das Karzinom auf dem Boden eines pleomorphen Adenoms entstanden war, ist nicht zuverlässig zu belegen, aber auch nicht völlig auszuschließen.
Bei Ausgang des Tumors von den kleinen Speicheldrüsen im Bereich des harten Gaumens und in Zusammenschau mit den üblichen Staging-Untersuchungen ergibt sich folgende postoperative Tumorklassifikation [TNM 8. Auflage 2017]: pT3, pN1(1/6), M0, L0, V0, Stadium III, Differenzierungsgrad G1, R1.
In einem Resektat der Neck Dissection rechts wurde ein Lymphknoten gefunden, in dem zwei kleinherdige, beginnende und knapp über 1 mm messende gleichartige, teils papilläre Epithelproliferationen wie im Tumorhauptresektat zu sehen waren. Dieser Befund wurde als eine initiale Tumormetastase gewertet. Einzelne Tumorformationen waren im kranialen und pterygomaxillären Nachresektat noch zu finden.
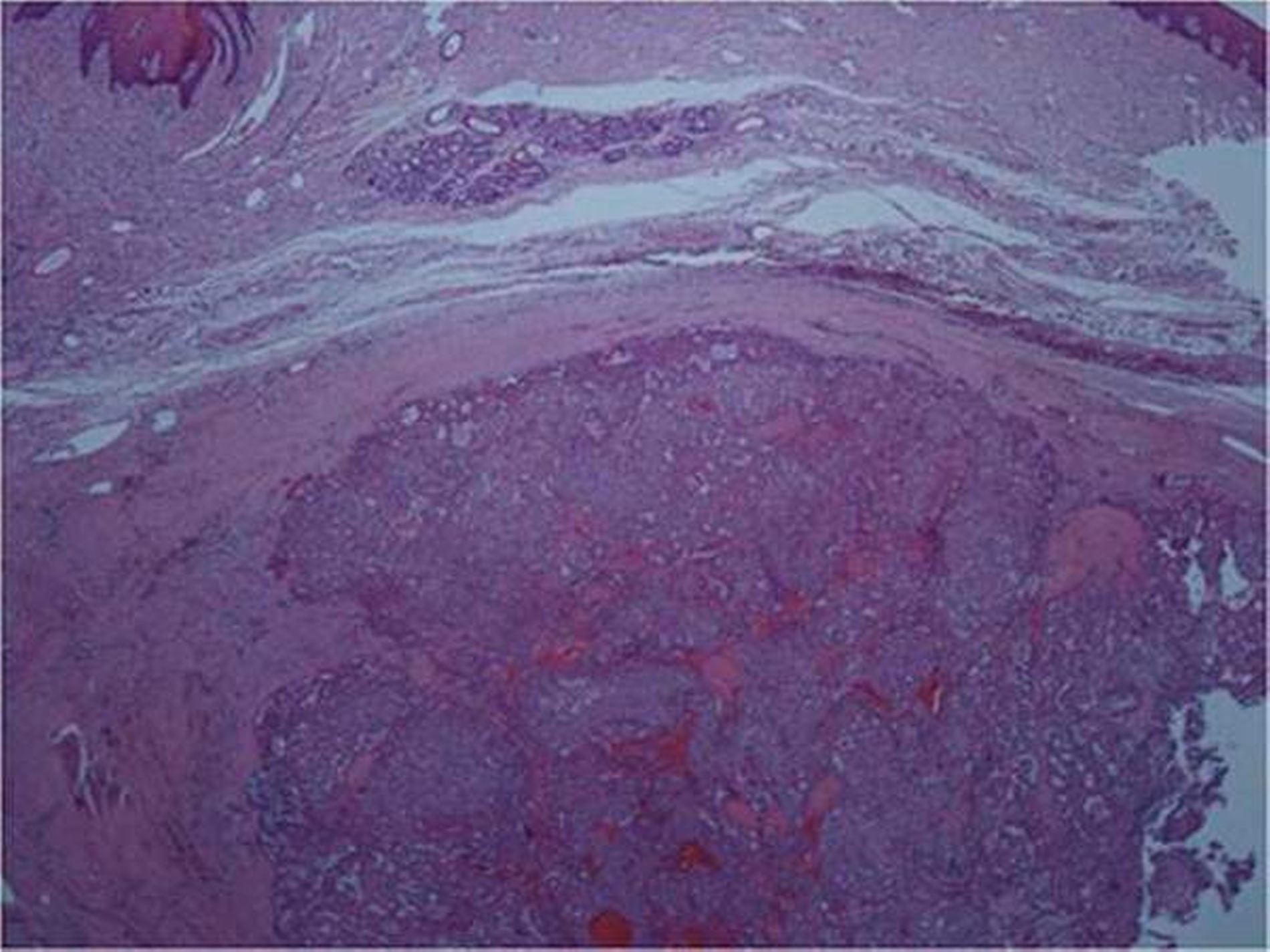
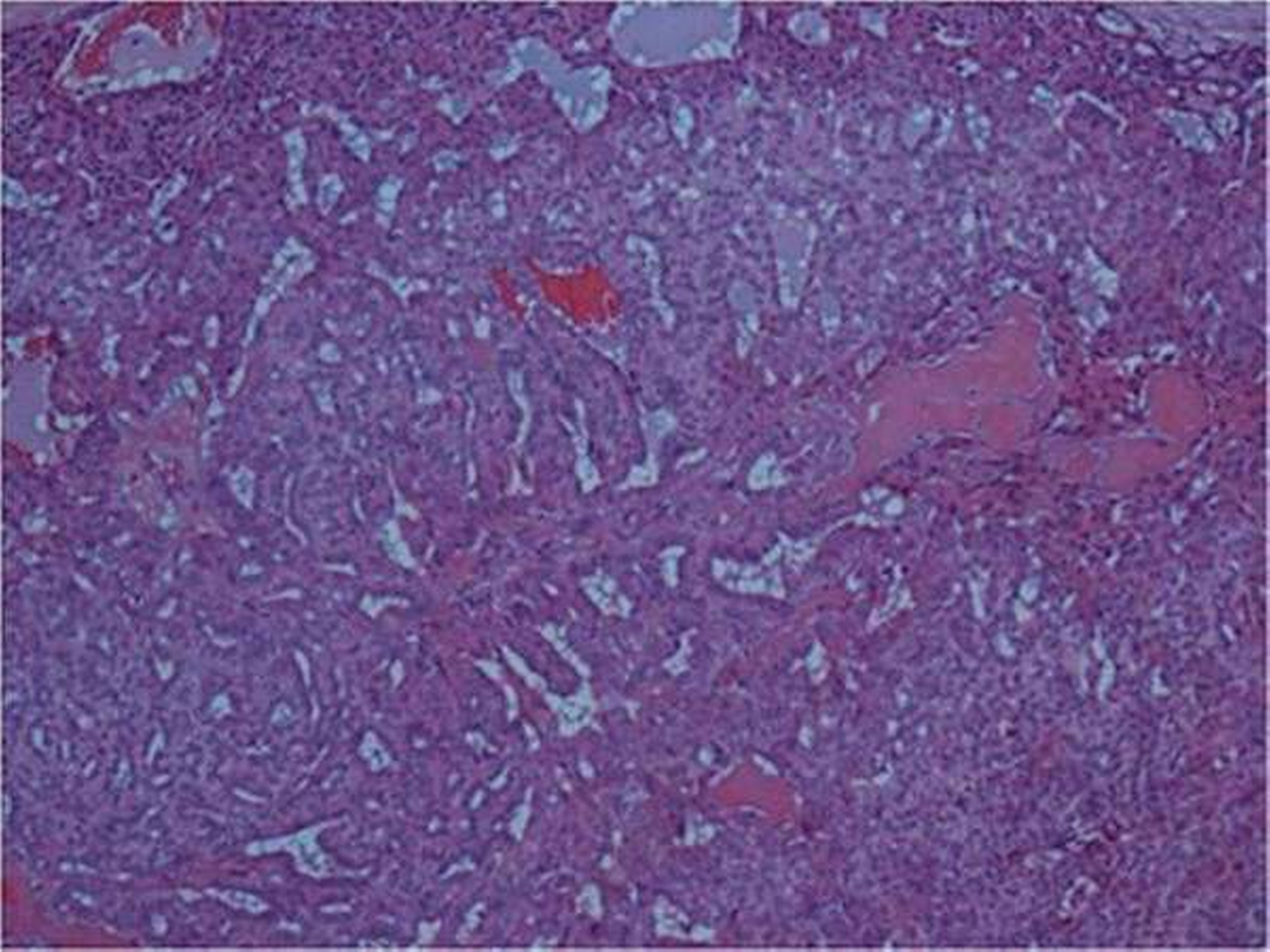
In der interdisziplinären Tumorkonferenz wurde postoperativ als adjuvante Maßnahme eine Bestrahlung empfohlen, diese wurde von der Patientin jedoch abgelehnt. Die histologische Aufarbeitung des Tumorpräparates ergab ein polymorphes Adenokarzinom.
Die Patientin stellt sich regelmäßig und engmaschig in unserer Tumorsprechstunde zur Nachsorge vor, die regelmäßige klinische und radiologische Kontrollen umfasst.
Diskussion
Tumoren der Speicheldrüsen machen etwa fünf Prozent der Kopf-Halstumore aus und können sowohl benigne als auch maligne sein. Der Großteil der Tumore ist mit etwa drei Viertel aller Speicheldrüsentumoren gutartig, nur etwa ein Viertel ist bösartig.
Als Faustregel gilt, je größer die Glandula salivatoria, desto häufiger sind die Raumforderungen gutartig, je kleiner die Drüsen, desto häufiger können sie maligne entarten.
Am häufigsten entstehen Speicheldrüsentumoren in der Glandula parotis (mit etwa 80 Prozent) und der Glandula submandibularis (etwa 15 Prozent). Tumoren der kleinen Speicheldrüsen, insbesondere des Gaumens sind selten. Der häufigste gutartige Tumor der Speicheldrüsen ist das pleomorphe Adenom. Es ist meist im lateralen Teil der Glandula parotidea oder am Übergang vom harten zum weichen Gaumen lokalisiert. Der Tumor an sich bereitet in der Regel keine Schmerzen und ist lange asymptomatisch. Seine progrediente Größenzunahme kann allerdings zu Verdrängungssymptomatiken, Schluckbeschwerden und Schwellungsgefühl führen.
Histologisch handelt es sich um einen epithelial-mesenchymalen Mischtumor, der von einer Pseudokapsel umgeben ist. Therapie der Wahl ist die Exstirpation. Kommt es hierbei zu Verletzungen der Kapsel und bleiben dadurch auch mikroskopische Tumorreste im Körper, ist häufiger mit Rezidiven zu rechnen.
Je länger ein pleomorphes Adenom besteht, desto höher wird sein Entartungsrisiko zum Karzinom ex pleomorphem Adenom [Brauner et al., 2016; Chen et al., 2010; Zbaren, Zbaren, Caversaccio, & Stauffer, 2008].
Zu den zahlreichen malignen Tumorarten der Speicheldrüsen zählt das in unserem Fall beschriebene polymorphe Adenokarzinom. Bei Diagnosestellung sind bereits circa 30 bis 50 Prozent dieser Tumore cervical in Lymphkoten metastasiert. Epidemiologisch ist er etwas häufiger bei Frauen zu finden, wobei der Altersgipfel im 6. Lebensjahrzehnt liegt.
Insgesamt ist seine Häufigkeit unter den intraoralen Speicheldrüsentumoren unter einem Prozent [Buchner, Merrell, & Carpenter, 2007; Evans & Luna, 2000; Hunter, Smith, & Brandwein-Gensler, 2008; Tsang, Tung, & Chan, 1991]. Er geht zumeist von den kleinen Speicheldrüsen des Gaumens aus. In der Parotis ist dieser Tumor eher selten zu finden, entsteht jedoch gelegentlich durch Entartung eines pleomorphen Adenoms.
Bei polymorphen Adenokarzinomen kommen Fernmetastasen nur in einem bis vier Prozent der Fälle vor. Die Zehn-Jahres-Überlebensrate liegt bei rund 96 Prozent [Castle, Thompson, Frommelt, Wenig, & Kessler, 1999; Patel et al., 2015].
Das polymorphe Adenokarzinom wird zu den niedrig malignen Tumoren gezählt. Eine wichtige histopathologische Differenzialdiagnose ist das adenoid-zystische Karzinom, welches ein deutlich aggressiveres Verhalten zeigt. Eine weitere bedeutende Differenzialdiagnose ist das nicht invasiv wachsende pleomorphe Adenom.
Bei einer kleinen Biopsie kann eine Unterscheidung zwischen beiden auch unmöglich werden. Ferner können bei einem polymorphen Adenokarzinom sowohl benigne wie maligne Anteile nebeneinander vorkommen, wie auch dieses Fallbeispiel zeigt [Kämmerer, Kreft, Toyoshima, Al-Nawas, & Klein, 2009]. In seltenen Fällen kann es zu einer high-grade-Entartung kommen [Simpson, Pereira, Ribeiro, Abdulkadir, & Reis-Filho, 2002].
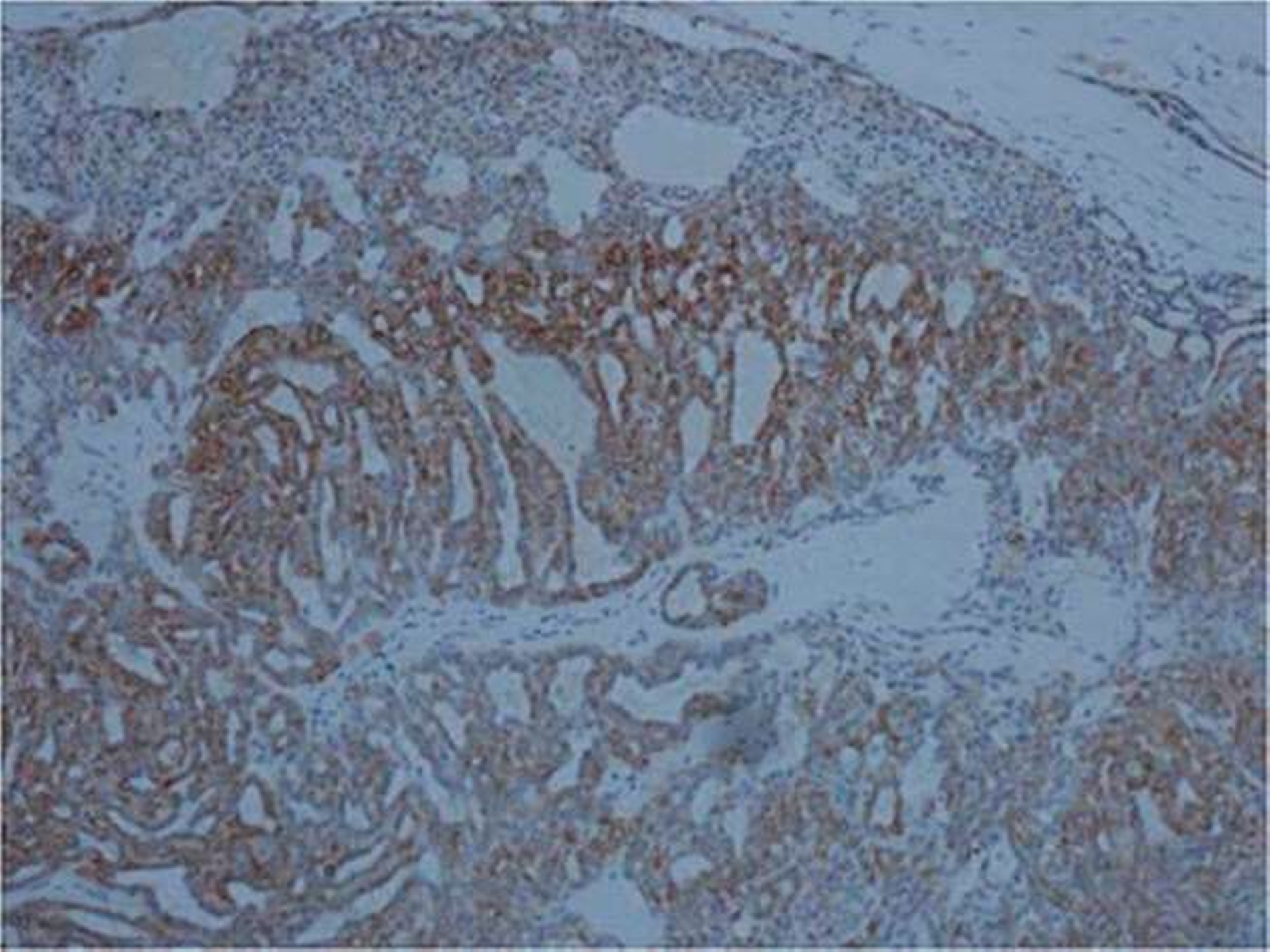
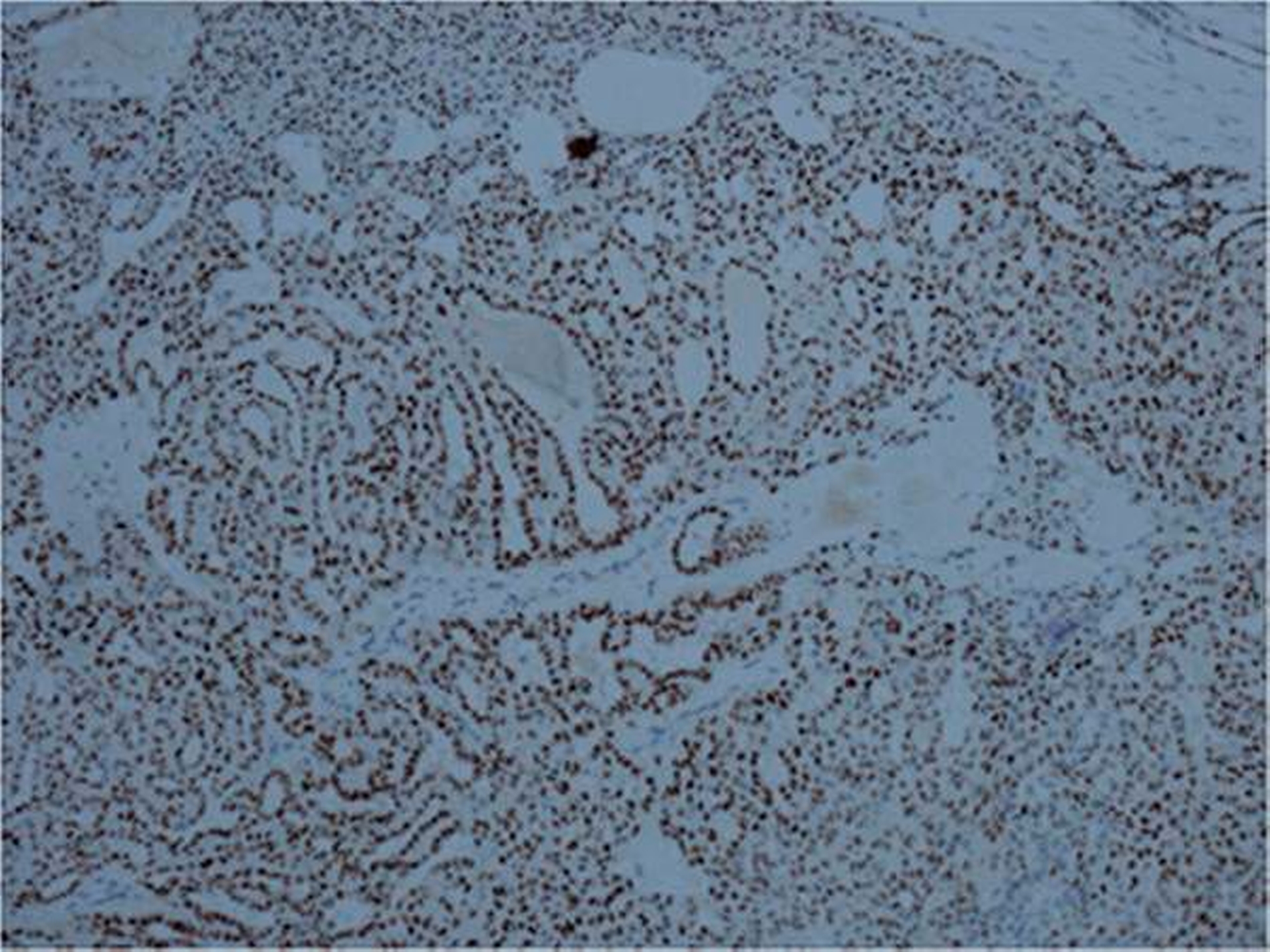
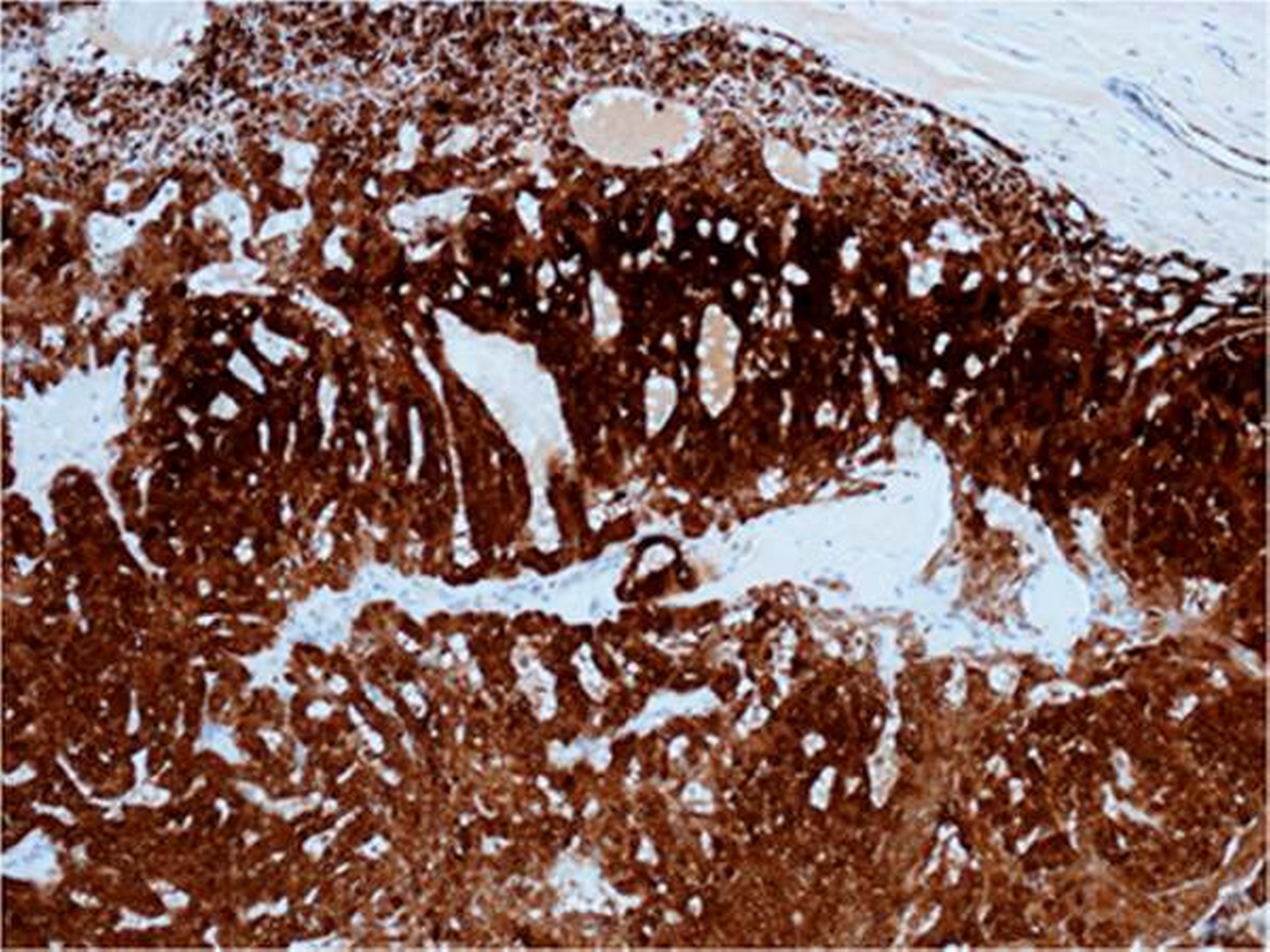
Der histologische Aufbau von Speicheldrüsen besteht generell aus unterschiedlichen Zelltypen (azinär, duktal, myoepithelial). Je nach Histogenese exprimieren deswegen Speicheldrüsentumore unterschiedliche immunhistochemische Marker. Beim polymorphen Adenokarzinom findet man epitheliale Antigene wie Zytokeratine, vor allem Zytokeratin 7 (100 Prozent der Fälle), p63 (100 Prozent der Fälle), Protein S-100 (97 Prozent der Fälle), BCL-2, gelegentlich CEA, alpha_SMA und Vimentin Cardesa, Mentzel, Rudolph, & Slootweg, 2009; Varun et al., 2015; El-Naggar et al., 2017].
Therapie der Wahl ist die radikale Tumorresektion mit anschließender Rekonstruktion oder prothetischer Obturatortherapie. Sind die Resektionsränder nicht sicher tumorfrei oder hat der Tumor bereits lokal in die Halslymphknoten gestreut, wird in der Literatur eine adjuvante Radiatio empfohlen [Crean, Bryant, Bennett, & Harris, 1996; Hunter et al., 2008; Le et al., 1999].
Allerdings wurde in Studien gezeigt, dass die Strahlentherapie keinen wesentlichen Einfluss auf regionale sowie Fernmetastasierung und das Überleben hat [Evans & Luna, 2000; Sathyanarayanan, Suresh, & Therese Thomas, 2016].
Zusammenfassend lässt sich sagen, dass in diesem Fall aufgrund der Lokalisation, der Histologie und des Tumorverhaltens am ehesten als Differenzialdiagnose das pleomorphe Adenom und das adenoid-zystische Karzinom in Betracht kommen würden. Nur durch eine ausreichend große Biopsie oder Aufbereitung des Präparats kann eine solch schwere diagnostische Unterscheidung letztendlich getroffen werden.
Folgen für diese Patientin ohne Therapie wären gewesen: weitere Wachstumsprogredienz sowie eine Fernmetastasierung. Irgendwann wäre ein inoperables Stadium erreicht und eine zufriedenstellende Therapie nicht mehr möglich gewesen. Die Alternative wäre eine reine Bestrahlung mit insgesamt schlechter Prognose gewesen.
Offen bleibt, ob sich das Karzinom auf dem Boden eines Adenoms gebildet hat und die Entartung nicht zustande gekommen wäre, wenn der Tumor bereits bei Erstdiagnose vor 30 Jahren therapiert worden wäre.
Fazit für die Praxis:
Fazit für die Praxis:
Adenokarzinome der kleinen Speicheldrüsen sind selten.
Histologische Sicherung - auch bei klinischem Verdacht auf pleomorphes Adenom
Ausführliche Aufklärung des Patienten über Erkrankung und frühzeitige Therapie
Therapie der Wahl ist die vollständige Tumorresektion.
Bei größeren Tumoren kann die Defektdeckung mittels mikrovaskulärem Transplantatlappen oder Obturator erfolgen.
Tamara Katharina Kakoschke
Klinik und Poliklinik für Mund-, Kiefer- und Gesichtschirurgie
Universität München
Lindwurmstraße 2a, 80337 München
tamara.kakoschke@med.uni-muenchen.de
Dr. Ulrike Speth
Klinik für Mund-, Kiefer- und Plastische Gesichtschirurgie
HELIOS Klinikum München West
Steinerweg 5, 81241 München
Prof. Dr. Christopher Poremba
Pathologie München Nord
Ernst-Platz-Straße 2, 80992 München
PD Dr. Dr. Denys J. Loeffelbein
Klinik für Mund-, Kiefer- und Plastische Gesichtschirurgie
HELIOS Klinikum München West
Steinerweg 5, 81241 München
Literatur
Brauner, E., Jamshir, S., Guarino, G., Ciolfi, A., Valentini, V., Pompa, G., & Di Carlo, S. (2016). Pleomorphic adenoma rehabilitative treatment in growing up patient: a 20-years follow-up. Eur Rev Med Pharmacol Sci, 20(17), 3523-3527.
Buchner, A., Merrell, P. W., & Carpenter, W. M. (2007). Relative frequency of intra-oral minor salivary gland tumors: a study of 380 cases from northern California and comparison to reports from other parts of the world. J Oral Pathol Med, 36(4), 207-214. doi:10.1111/j.1600-0714.2007.00522.x
Cardesa, A., Mentzel, T., Rudolph, P., & Slootweg, P. J. (2009). Pathologie: Kopf-Hals-Region, Weichgewebstumoren, Haut. Berlin Heidelberg, Deutschland: Springer-Verlag.
Castle, J. T., Thompson, L. D., Frommelt, R. A., Wenig, B. M., & Kessler, H. P. (1999). Polymorphous low grade adenocarcinoma: a clinicopathologic study of 164 cases. Cancer, 86(2), 207-219.
Chen, H. H., Lee, L. Y., Chin, S. C., Chen, I. H., Liao, C. T., & Huang, S. F. (2010). Carcinoma ex pleomorphic adenoma of soft palate with cavernous sinus invasion. World J Surg Oncol, 8, 24. doi:10.1186/1477-7819-8-24
Crean, S. J., Bryant, C., Bennett, J., & Harris, M. (1996). Four cases of polymorphous low-grade adenocarcinoma. Int J Oral Maxillofac Surg, 25(1), 40-44.
El-Naggar, A.K., Chan, J.K.C., Grandis, J.R., Takata, T., & Slootweg, P.J. (Eds.) (2017). WHO Classification of Head and Neck Tumours (4th edition). IARC Lyon, 167-168.
Evans, H. L., & Luna, M. A. (2000). Polymorphous low-grade adenocarcinoma: a study of 40 cases with long-term follow up and an evaluation of the importance of papillary areas. Am J Surg Pathol, 24(10), 1319-1328.
Hunter, J. B., Smith, R. V., & Brandwein-Gensler, M. (2008). Low-grade papillary adenocarcinoma of the palate: the significance of distinguishing it from polymorphous low-grade adenocarcinoma. Head Neck Pathol, 2(4), 316-323. doi:10.1007/s12105-008-0082-1
Kämmerer, P. W., Kreft, A., Toyoshima, T., Al-Nawas, B., & Klein, M. O. (2009). Misleading initial histological diagnosis of a polymorphous low-grade adenocarcinoma in situ ex pleomorphic adenoma-a case report. Oral Maxillofac Surg, 13(2), 99-103. doi:10.1007/s10006-009-0150-z
Le, Q. T., Birdwell, S., Terris, D. J., Gabalski, E. C., Varghese, A., Fee, W., Jr., & Goffinet, D. R. (1999). Postoperative irradiation of minor salivary gland malignancies of the head and neck. Radiother Oncol, 52(2), 165-171.
Patel, T. D., Vazquez, A., Marchiano, E., Park, R. C., Baredes, S., & Eloy, J. A. (2015). Polymorphous low-grade adenocarcinoma of the head and neck: A population-based study of 460 cases. Laryngoscope, 125(7), 1644-1649. doi:10.1002/lary.25266
Sathyanarayanan, R., Suresh, V., & Therese Thomas, B. A. (2016). Polymorphous Low-Grade Adenocarcinoma of the Palate: A Rare Case Report. Iran J Cancer Prev, 9(1), e3447. doi:10.17795/ijcp-3447
Simpson, R. H., Pereira, E. M., Ribeiro, A. C., Abdulkadir, A., & Reis-Filho, J. S. (2002). Polymorphous low-grade adenocarcinoma of the salivary glands with transformation to high-grade carcinoma. Histopathology, 41(3), 250-259.
Tsang, Y. W., Tung, Y., & Chan, J. K. (1991). Polymorphous low grade adenocarcinoma of the palate in a child. J Laryngol Otol, 105(4), 309-311.
Varun, C., Dineshkumar, T., Jayant, V. S., Rameshkumar, A., Rajkumar, K., Rajashree, P., Arunvignesh, R. K. (2015). Salivary Her2/neu Levels in Differentiation of Oral Premalignant Disorders and Oral Squamous Cell Carcinomas. Asian Pac J Cancer Prev, 16(14), 5773-5777.
Zbaren, P., Zbaren, S., Caversaccio, M. D., & Stauffer, E. (2008). Carcinoma ex pleomorphic adenoma: diagnostic difficulty and outcome. Otolaryngol Head Neck Surg, 138(5), 601-605. doi:10.1016/j.otohns.2008.01.013