UAW-Meldungen zu Clindamycin erstmals rückläufig
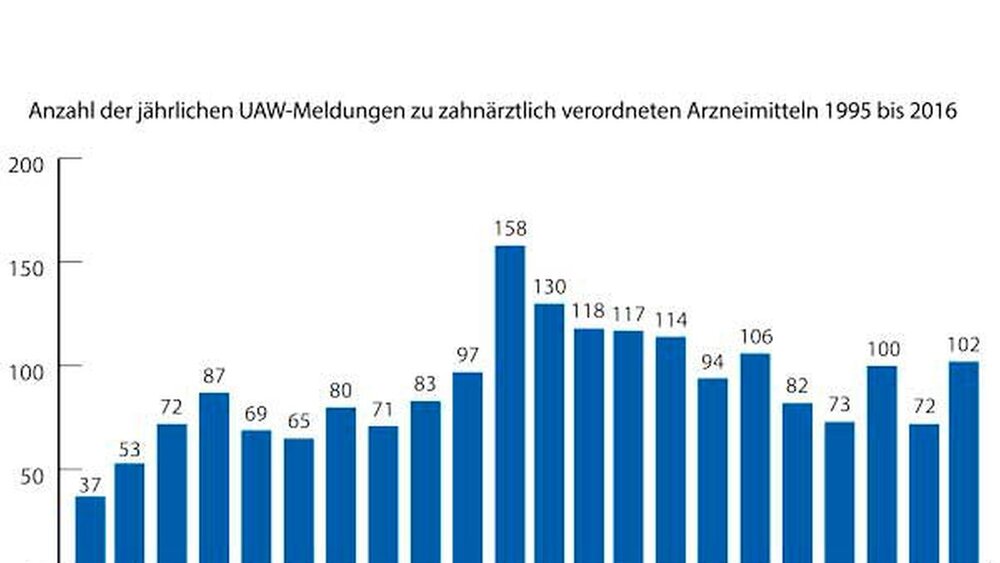
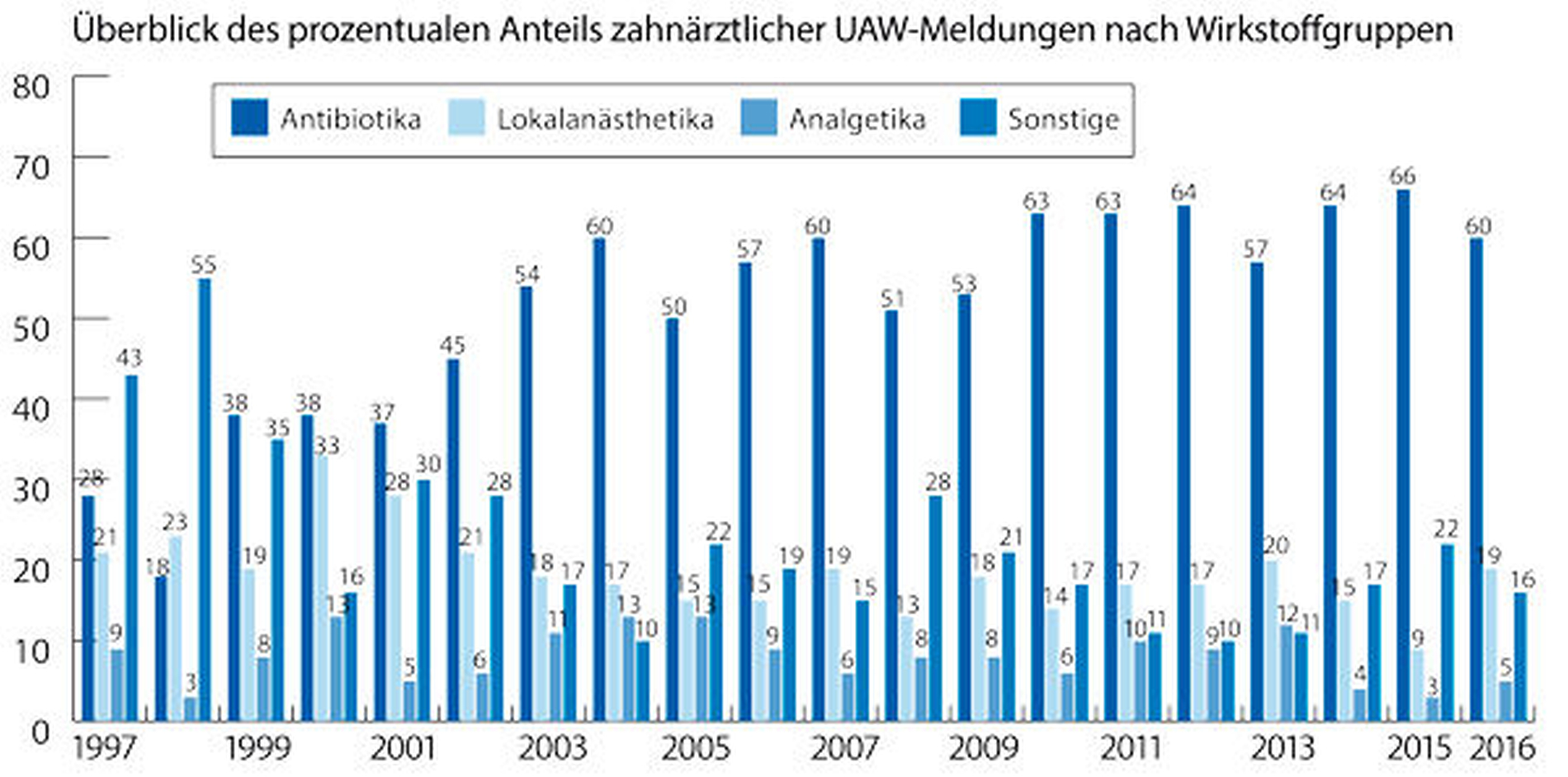
Die Gesamtanzahl an UAW-Meldungen an die AKZ ist im Kalenderjahr 2016 im Vergleich zu den Vorjahren wieder leicht angestiegen auf 102 Meldungen. Als mögliche Ursachen der beobachteten Nebenwirkung wurden teilweise mehrere Arzneimittel in einer Meldung angegeben. Das Spektrum unerwünschter Arzneimittelwirkungen (UAWs) zahnärztlich verordneter Arzneimittel ist inzwischen sehr gut bekannt und hat sich in den vergangenen 20 Jahren kaum verändert, was dazu führt, dass es von verordnenden Kollegen vielmals gar nicht mehr als notwendig erachtet wird, auch eine schwerer verlaufende unerwünschte Wirkung explizit zu melden. Dies erschwert die Beurteilung des Sicherheitsspektrums zahnärztlich angewendeter Arzneimittel. An dieser Stelle sei daher darauf hingewiesen, dass insbesondere schwer verlaufende UAWs (wie spezifische medizinische Behandlung aufgrund der UAW erforderlich, Notarzteinsatz, stationärer Aufenthalt) immer gemeldet werden sollten – auch dann, wenn der Kausalzusammenhang bereits in der Fachinformation des Präparats beschrieben und gut bekannt ist. Der relative Anteil der Meldungen zu unerwünschten Wirkungen zahnärztlich verordneter Antibiotika (bezogen auf das Gesamtspektrum zahnärztlich verordneter Arzneimittel) ist von 66 Prozent im Jahr 2015 auf 60 Prozent im Jahr 2016 gesunken (Abbildung 2).
UAWs zu Clindamycin in 2016 erstmals rückläufig
Innerhalb der Wirkstoffgruppe der Antibiotika war der Anteil zahnärztlicher UAW-Meldungen zu Clindamycin erstmals rückläufig: 2016 wurden nur noch 19 Meldungen (28 Prozent aller gemeldeten Antibiotika) zu Clindamycin abgegeben. Im Jahr 2015 waren es noch 31 Meldungen. Der Gesamtanteil von Clindamycin an den UAW-Meldungen zahnärztlich eingesetzter Antibiotika betrug 2015 noch 59 Prozent. Die Spitzenstellung der am häufigsten zahnärztlich gemeldeten Antibiotika hat im Jahr 2016 erstmals das Betalaktamantibiotikum Amoxicillin übernommen. Im Jahr 2016 wurden 41 Meldungen (60 Prozent ) zu Amoxicillin, davon in drei Fällen in Kombination mit Clavulansäure, abgegeben (2015: n = 15 (28 Prozent); 2014: n = 25 (37 Prozent), 2013: n = 16 (36 Prozent), Kombinationspräparate mit Clavulansäure mitgezählt. Mit großem Abstand folgt Metronidazol im Jahr 2016 mit vier Meldungen (6 Prozent), nahezu unverändert zu 2015: n = 3 (15 Prozent); 2014: n = 7 (10 Prozent); 2013: n = 3 (7 Prozent) in der UAW-Statistik.
Andere Antibiotika spielten auch im Jahr 2016 (zusammen insgesamt n = 4 (6 Prozent)) wie in den Vorjahren in der zahnärztlichen UAW-Statistik praktisch keine Rolle.
Zur Wirkstoffgruppe der Chinolone („Gyrasehemmer“) wurde im Jahr 2016 nur eine Meldung zu Moxifloxacin abgegeben. Dies entspricht der niedrigen zahnärztlichen Verordnungsrate von Chinolonen, die zwar ein sehr breites Wirkspektrum besitzen, aber seit einiger Zeit in der Kritik stehen. Das Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) hat im Februar 2017 ein europäisches Risikobewertungsverfahren für Antibiotika aus der Gruppe der Fluorchinolone und Chinolone angestoßen. Ziel ist eine umfassende Bewertung seltener, aber schwerwiegender und oftmals persistierender Nebenwirkungen, die hauptsächlich Muskeln, Gelenke und das Nervensystem betreffen. Der Ausschuss für Risikobewertung im Bereich der Pharmakovigilanz (PRAC) hat zwischenzeitlich entschieden, dass im Juni 2018 während der Tagung des Ausschusses eine öffentliche Anhörung durchgeführt wird.
In drei Fällen wurden UAWs zu Sultamicillin beschrieben. Bezüglich der berichteten UAWs von Antibiotika überwiegen wie in den Vorjahren vor allem allergische Hautreaktionen (Urtikaria, makulopapulöse Exantheme am ganzen Körper, Gesichtsschwellungen) sowie gastrointestinale Beschwerden (Übelkeit, Diarrhoe, Bauchschmerzen, Ösophagitis, Oberbauchschmerzen) und Unverträglichkeitsreaktionen. Sehr vereinzelt traten zentralnervöse Nebenwirkungen wie Kopfschmerzen, Müdigkeit und Schwindel bis hin zu Symptomen einer neuromuskulären Blockade (unter Clindamycin) auf. Clindamycin kann pharmakologisch aufgrund seiner neuromuskulär-blockierenden Eigenschaften die Wirkung von Muskelrelaxanzien verstärken (wie Tubocurarin, Pancuroniumhalogenid). Hierdurch können bei Operationen unerwartete, lebensbedrohliche Zwischenfälle auftreten. In einem Fall wurde unter der Einnahme von Clindamycin über das Auftreten von Halluzinationen berichtet. Fast alle Antibiotika können grundsätzlich auch Funktionsstörungen des peripheren und des zentralen Nervensystems verursachen. Eine Übersicht zu neurotoxischen Nebenwirkungen von Antibiotika hat die AKZ in der zm 11/2016 veröffentlicht [Stahlmann/Schindler zm, 2016].
Einsatz von Antibiotika in der zahnärztlichen Praxis
Zwar ist die Anzahl der abgegebenen UAW-Meldungen zu Clindamycin mit insgesamt nur noch 19 Meldungen (28 Prozent in der Antibiotikagruppe) im Jahr 2016 seit Jahren erstmals rückläufig. Doch leider korreliert dieser beobachtete Rückgang an UAW-Meldungen zu zahnärztlich verordneten Antibiotika nicht mit einem Rückgang zahnärztlicher Verordnungen von Clindamycin, das immer noch zu häufig zahnärztlich verordnet wird und mit 10,2 Mio. DDD (entspricht 29 Prozent aller zahnärztlich verordneten Antibiotika-DDD) im Jahr 2016 nach den Aminopenicillinen immer noch das von Zahnärzten am zweithäufigsten verordnete Antibiotikum war, wobei weiterhin 60 Prozent aller Clindamycin-Verordnungen in Deutschland von Zahnärzten stammen [Halling, 2017]. Die AKZ hat wiederholt auf die untergeordnete therapeutische Stellung von Clindamycin in der Zahnmedizin hingewiesen [Schindler et Stahlmann, 2014]. Diese muss an dieser Stelle abermals unterstrichen werden.
In der Zahnmedizin werden nach wie vor primär Betalaktamantibiotika aufgrund guter Wirksamkeit auf orale Pathogene und hoher therapeutischer Breite als Mittel der ersten Wahl empfohlen.
Die Kombination Amoxicillin/Clavulansäure ist gegenüber odontogenen Keimen als gut wirksam dokumentiert und sollte zum Einsatz kommen, wenn eine erhöhte Resistenzlage zu befürchten ist. Die Tatsache, dass im Jahr 2016 innerhalb der Wirkstoffgruppe der Antibiotika erstmals Amoxicillin am häufigsten UAWs verursacht hat, bestätigt, dass die UAWs von Amoxicillin/Clavulansäure auch im direkten Vergleich mit Clindamycin nicht unterschätzt werden dürfen. Diese betreffen insbesondere allergische Unverträglichkeitsreaktionen aller Schweregrade, meist Hautreaktionen und die besonders für Clavulansäure beschriebene Leberunverträglichkeit mit ausgeprägten Transaminasenerhöhungen.
Clindamycin wird aufgrund seines ausgeprägten gastrointestinalen Nebenwirkungsprofils explizit als Mittel der zweiten Wahl empfohlen, zum Beispiel bei Penicillin-Allergie. Es gibt keinen hinreichenden Grund, Clindamycin gegenüber der Kombination Amoxicillin/Clavulansäure zu bevorzugen. Als weitere therapeutische Alternative in Zahnmedizin und MKG-Chirurgie kann die Kombination aus Ampicillin und Sulbactam, beziehungsweise bei oraler Therapie Sultamicillin, die Esterverbindung dieser Wirkstoffe, angesehen werden, auch wenn es keine explizite Zulassung für den zahnmedizinischen Anwendungsbereich gibt [Schindler/Stahlmann, 2014]. Durch den Betalaktamaseinhibitor Sulbactam ist die antibakterielle Wirkung des Aminopenicillins verstärkt und sein Spektrum erweitert. Von Bedeutung für die Zahnheilkunde ist insbesondere die Aktivität des Präparats gegen anaerobe Bakterien. Bacteroides-Arten sowie Clostridien und Peptokokken werden bereits bei niedrigen Konzentrationen gehemmt. Ferner ist auf die gute Knochengängigkeit der beiden Bestandteile von Sultamicillin, Ampicillin und Sulbactam, hinzuweisen. Zusammenfassend stellt die Gabe von Sultamicillin im zahnmedizinischen Bereich bei richtiger Indikationsstellung aus pharmakologischer Sicht eine sinnvolle therapeutische Alternative zu einer Behandlung mit Amoxicillin/Clavulansäure oder mit Clindamycin dar.
Einsatz von Analgetika
Der prozentuale Anteil an UAW-Meldungen zu Analgetika lag im Jahr 2016 bei 5 Prozent und bleibt somit auf dem seit 2014 beobachteten insgesamt niedrigen Niveau. Ibuprofen ist nach Verordnungszahlen mit Abstand das am häufigsten zahnärztlich eingesetzte Analgetikum. Die vier Meldungen zu Ibuprofen in Form von allergischen Unverträglichkeitsreaktionen, teilweise mit Kreislaufreaktion, Exanthem, Lippen- und Halsschwellung waren nach Absetzen des Präparats allesamt reversibel und liegen im zu erwartenden Nebenwirkungsspektrum der Substanz. In einem Fall wurde unter Einnahme von Dexketoprofen über Schlaflosigkeit, Rückenschmerzen und einen erhöhten Harndrang berichtet. Schlaflosigkeit wird gelegentlich unter Einnahme von Dexketoprofen beschrieben. Bezüglich der pharmakodynamischen Wirksamkeit von Dexketoprofen bei Zahnschmerzen ist festzustellen, dass in der wissenschaftlichen Literatur weder Wirksamkeits- noch Verträglichkeitsvorteile zugunsten von Dexketoprofen gegenüber Standardanalgetika beschrieben werden. Insgesamt verursachte die zahnärztliche Therapie mit Analgetika kaum Komplikationen. Die insgesamt weiter abnehmende und auch absolut extrem geringe Zahl an UAW-Meldungen zu dieser Arzneimittelgruppe spricht für einen insgesamt sicheren Umgang der Zahnärzteschaft mit Analgetika.
Einsatz von Lokalanästhetika
In der Gruppe der Lokalanästhetika ist im Jahr 2016 ein leichter Anstieg in der Anzahl von Berichten zu unerwünschten Arzneimittelwirkungen auf 19 Prozent zu verzeichnen, verglichen mit neun Prozent im Jahr 2015. Wie in den Vorjahren wurden 2016 vor allem Meldungen zu Articain (n = 17), meist in Kombination mit dem Vasokonstringens Epinephrin registriert, was auf die breite Anwendung des Präparats zurückzuführen ist. Das gemeldete UAW-Spektrum umfasste allergische Unverträglichkeitsreaktionen wie lokale Schwellungen und Rötungen, Emphyseme, Herz-Kreislauf-Probleme mit Herzfrequenz- und Blutdruckanstieg bis hin zu einem Angina-pectoris-Anfall. Ansonsten wurden mittelschwere zentralnervöse Symptome (wie zum Beispiel Kopfschmerzen, systemischer Tremor, Schwindel, Unruhe und Druckgefühl im Kopf) gemeldet, die mit der Gabe von Lokalanästhetika in Zusammenhang stehen können und am ehesten für einen zentralnervös toxischen Effekt des Präparats sprechen, der oftmals auf eine trotz sorgfältiger Aspiration unbemerkte akzidentelle intravasale Applikation beziehungsweise auf eine erhöhte Resorptionsgeschwindigkeit des Lokalanästhetikums zurückgeführt werden kann. Zentralnervöse Effekte nach Lokalanästhetika-Applikation sind dosisabhängig: Zunächst kommt es zu exzitatorischen zentralen Symptomen wie Erregung, Unruhe, Schwindel, akustischen und visuellen Störungen, perioralem Kribbeln, einer verwaschenen Sprache, Übelkeit, Erbrechen, Zittern und Muskelzuckungen als Vorzeichen eines drohenden Krampfanfalls. Wir empfehlen, bei einem erneuten zahnärztlichen Eingriff bei betroffenen Patienten die zu applizierende Gesamtdosis niedriger zu wählen. Insgesamt werden Lokalanästhetika sicher und ohne größere Komplikationen angewendet.
Sonstige Medikamente
Der Anteil der Meldungen in der Gruppe „Sonstige“ liegt im Jahr 2016 mit 16 Prozent nahezu gleichauf mit dem Jahr 2014 (17 Prozent ). In dieser inhomogenen Gruppe werden alle Präparate zusammengefasst, die primär oftmals nicht vom Zahnarzt verordnet wurden. Dies erklärt sich aus der Tatsache, dass eine vom Zahnarzt beobachtete unerwünschte Arzneimittelwirkung nicht immer eindeutig dem vom Zahnarzt applizierten Präparat zuzuordnen ist und daher die vom Haus- oder Facharzt verschriebene Medikation ebenfalls mitgemeldet wird.
Amlodipin:
Neben vereinzelten Meldungen mit nicht gesichertem Kausalzusammenhang wurden vier Fälle typischer Gingivahyperplasien unter Therapie mit Amlodipin gemeldet. Das histologische Bild stellt eine exzessive Vermehrung von Fibroblasten und eine Steigerung der Kollagensynthese im Bereich der Gingiva dar. Vor allem in Gegenwart eines bakteriellen Entzündungsprozesses der Gingiva können Calciumkanalblocker die Kollagenproduktion durch Fibroblasten erhöhen und gleichzeitig den Abbau von Kollagen verlangsamen, was zu einer gingivalen Hypertrophie führt. Insbesondere bei Calciumkanalblocker-induzierter Gingivahypertrophie scheint der Entzündungsprozess pathophysiologisch eine wesentliche Rolle zu spielen [Mishra, 2011; Sucu, 2011]. Der Zusammenhang zwischen einer Therapie mit einem Calciumkanalblocker und dem Parodontium ist in der wissenschaftlichen Literatur schon lange bekannt und sehr gut beschrieben.
Chlorhexidingluconat:
Ferner wurden 2016 gleich in mehreren Fällen allergische Reaktionen auf Chlorhexidin beschrieben. Es ist seit Längerem bekannt, dass der Wirkstoff Chlorhexidingluconat seltene schwere allergische Reaktionen bis hin zur Anaphylaxie hervorrufen kann. Das Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) hat bereits im September 2013 eine entsprechende Warnung herausgegeben. Darin war auf die Gefahr von Überempfindlichkeitsreaktionen unter Chlorhexidin hingewiesen worden. Zum damaligen Zeitpunkt lagen dem BfArM 147 Berichte aus Deutschland über anaphylaktische Reaktionen im Zusammenhang mit der Anwendung von Chlorhexidin vor, die meisten davon bei der Anwendung von Chlorhexidin-haltigen Mundspüllösungen. Auch die US-amerikanische FDA warnt inzwischen vor schweren allergischen Reaktionen unter Chlorhexidin. Zahnärzte sollten bei ihren Patienten grundsätzlich vor jeder Verordnung von Chlorhexidin erfragen, ob jemals eine allergische Reaktion auf Chlorhexidin aufgetreten ist. Im positiven Fall kann zum Beispiel auf Octenidin als Antiseptikum ausgewichen werden.
Faktor-Xa-Antagonisten, NOAKs:
In der UAW-Statistik der AKZ taucht im Jahr 2016 nur eine einzige Meldung zur Gruppe der neuen gerinnungshemmenden Wirkstoffe auf, zu denen die neu entwickelten, hochselektiven Faktor-Xa-Antagonisten (Rivaroxaban, Apixaban und Edoxaban) sowie der Thrombinantagonist Dabigatran gehören. Unter Rivaroxaban wurde eine massive Nachblutung sechs Tage nach Extraktion gemeldet. Es ist aber davon auszugehen, dass in der zahnärztlichen Praxis weit mehr Nachblutungen unter Behandlung mit einem der neuen oralen Antikoagulantien auftreten. Diese werden aber offensichtlich nicht an die AKZ, sondern höchstwahrscheinlich an die Arzneimittelkommission der deutschen Ärzteschaft gemeldet. Unter Federführung der DGZMK wird derzeit eine AWMF S3-Leitlinie zum zahnärztlichen Umgang mit Patienten unter Antikoagulantientherapie entwickelt (siehe:
Bisphosphonate oder Denosumab:
Zu den antiresorptiven Substanzen, zu denen der IgG2-anti-RANKL-Antikörper Denosumab gehört, wurde im Jahr 2016 nur eine Meldung über die Nekrotisierung des unbezahnten Kieferknochens abgegeben. Diese unerwünschte Wirkung ist inzwischen gut bekannt. Die wichtigste Präventivmaßnahme besteht daher vor Ansetzen dieser Substanzen in einer zahnärztlichen Untersuchung und gegebenenfalls der Durchführung einer prätherapeutischen Mundhöhlensanierung.
Ausgedehnte zahnärztlich-chirurgische Eingriffe sollten bei Patienten, die intravenös Bisphosphonate oder Denosumab erhalten oder erhalten haben, nach Möglichkeit vermieden werden. Für operative Eingriffe und Zahnentfernungen bei diesem Patientenkreis empfiehlt die AWMF S3-Leitlinie „Bisphosphonat-assoziierte Kiefernekrose (BP-ONJ) und andere Medikamenten-assoziierte Kiefernekrosen“ folgende Maßnahmen: prolongierte perioperative, systemische antibiotische Abschirmung, atraumatische Operation mit sparsamer Periost-Denudierung, sorgfältige Abtragung scharfer Knochenkanten und eine·primär plastische Deckung [AWMF 007/091, 2012].
Olaflur, Pyranthel und Moxonidin:
Ebenfalls unter Sonstige werden die Präparate Olaflur, Pyranthel und Moxonidin in der UAW-Statistik 2016 geführt. Olaflur ist ein Aminfluorid und wird in der Zahnmedizin zur Prophylaxe von Karies und Parodontitis eingesetzt. Das Auftreten von Atemnot nach Anwendung von Olaflur spricht für eine typische Unverträglichkeitsreaktion, die am ehesten auf die ebenfalls im Präparat enthaltenen Hilfsstoffe Pfefferminz-Aroma, Krauseminzöl und Levomenthol zurückzuführen ist. Entsprechend sensibilisierte beziehungsweise disponierte Patienten sollten das Präparat nicht mehr erhalten. Pyranthel ist ein Anthelminthikum und wirkt gegen Maden-, Spul-, Haken- und Fadenwürmer. Die Substanz wirkt depolarisierend und führt über eine neuromuskuläre Blockade und Hemmung der Cholinesterase zu einer spastischen Lähmung in der Muskulatur des Parasiten. Die gemeldeten unerwünschten Wirkungen in Form von gastrointestinaler Unverträglichkeit und leichten zentralnervösen Wirkungen sind über den Wirkmechanismus der Substanz gut erklärbar. Das zentral wirksame Antihypertensivum Moxonidin bindet im Hirnstamm selektiv an Imidazol-Rezeptoren vom Typ 1. Diese Imidazol-Rezeptoren liegen konzentriert im rostralen ventrolateralen Anteil der Medulla oblongata, einem Areal das eine entscheidende Bedeutung für die zentrale Regulation der peripheren Sympathikus-Aktivität hat. Ein Kausalzusammenhang mit Gingivitis wurde bisher in der wissenschaftlichen Literatur nicht beschrieben und erscheint unwahrscheinlich.
Thiazide:
Die unter Einnahme des Thiazid-Diuretikums Hydrochlorthiazid beschriebenen Sehstörungen können mit der Einnahme des Präparats in Zusammenhang stehen und können für eine relative Überdosierung sprechen.
Eisen(II)glycinsulfat:
Die hierfür beschriebene Hypersensibilität aller Zähne kann indirekt mit der Einnahme des Medikaments in Zusammenhang stehen. Verfärbungen der Zähne können bei einer Behandlung mit oralen Eisenpräparaten auftreten. Entsprechend der wissenschaftlichen Literatur können sich diese Zahnverfärbungen nach Absetzen des Arzneimittels spontan zurückbilden oder müssen durch Verwendung einer schleifenden Zahnpasta oder durch eine professionelle Zahnreinigung entfernt werden. Möglicherweise ist die beschriebene Hypersensibilität reaktiv durch verstärkte Zahnreinigungsmaßnahmen entstanden.
Organbezogenheit der Nebenwirkungen
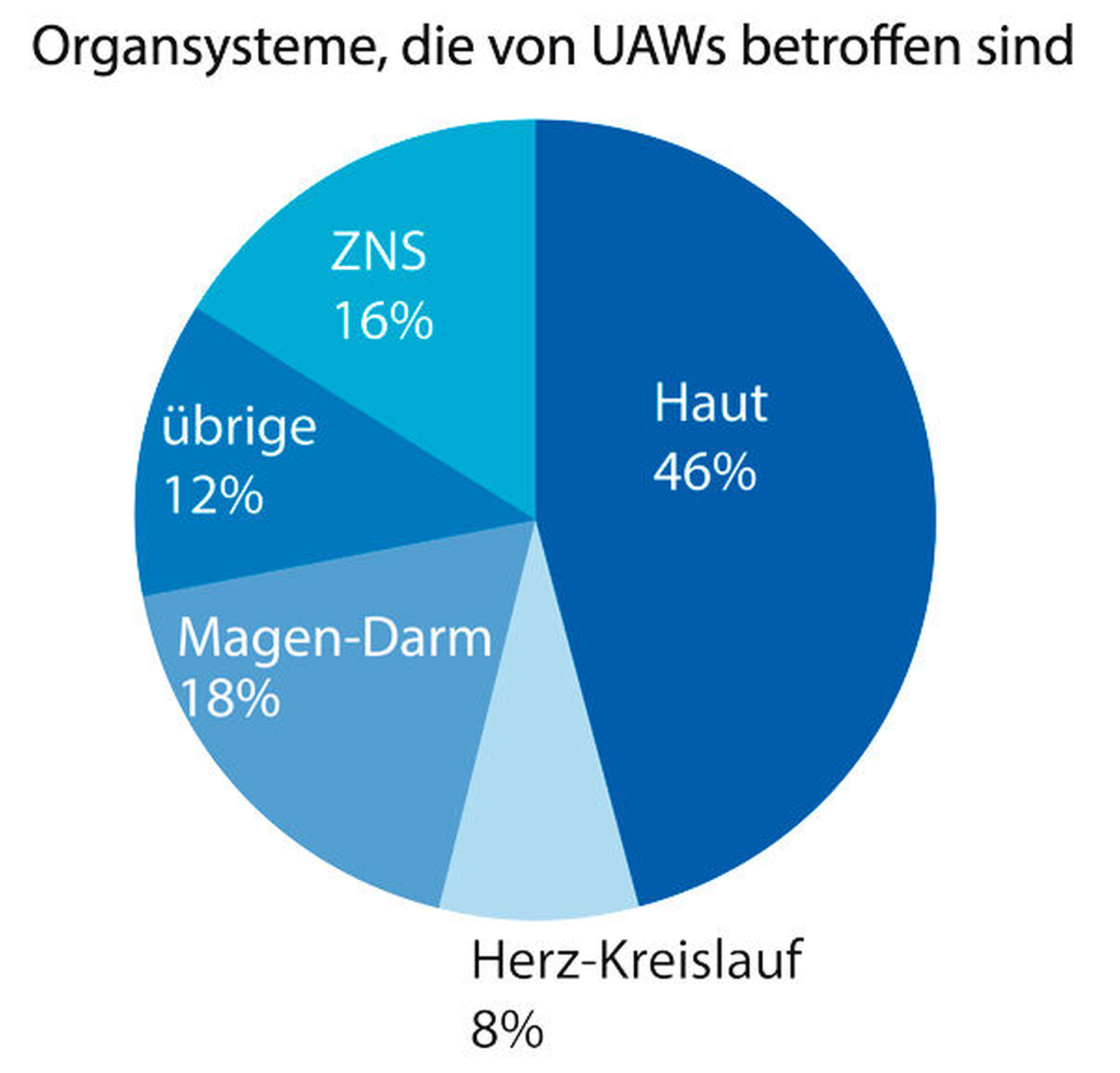
Die mit Abstand meisten der gemeldeten unerwünschten Arzneimittelwirkungen im Jahr 2016 manifestierten sich mit 46 Prozent an Haut und Schleimhäuten, meist in Form von allergischen Exanthemen, Urtikaria, Schwellungen, Juckreiz und Ödemen. Mit 18 Prozent am zweithäufigsten manifestierten sich UAWs am beziehungsweise im Gastrointestinaltrakt in Form von Bauchschmerzen, Übelkeit und Diarrhoe (Abbildung 3). Beeinträchtigungen des Gastrointestinaltrakts wurden hauptsächlich im Zusammenhang mit Antibiotikatherapie und hier insbesondere unter Behandlung mit Amoxicillin und Clindamycin beobachtet. Leider ist das gastrointestinale Verträglichkeitsprofil von Amoxicillin nur unwesentlich besser als das von Clindamycin. Um die gastrointestinale Verträglichkeit zu verbessern, sollte die Einnahme der Medikation mit ausreichend Flüssigkeitszufuhr (mindestens 200 bis 250 ml Wasser) und zu den Mahlzeiten erfolgen. Über ZNS-Störungen wurde 2016 in 16 Prozent der Fälle berichtet, wobei diese am häufigsten im Zusammenhang mit Lokalanästhetika beziehungsweise antibiotischer Therapie beschrieben wurden. Während unter Therapie mit Lokalanästhetika meistens eine relative Überdosierung ursächlich für zentralnervöse Nebenwirkungen ist, können Antibiotika per se neurotoxische Nebenwirkungen verursachen, die häufig fehlgedeutet werden. Während Penicilline, Cephalosporine und Chinolone hauptsächlich über eine Inhibition der GABAA-Rezeptoren neurotoxisch wirken, ist der Mechanismus für Metronidazol, Makrolide, Clindamycine und Tetrazykline weitgehend ungeklärt [Stahlmann, 2016]. Vorhandene neuropsychiatrische Grunderkrankungen, eine entsprechende Begleitmedikation sowie eine vorhandene Niereninsuffizienz bei renal eliminierten Antibiotika sind als zusätzliche Risikofaktoren anzusehen. Eine Beachtung dieser Gegebenheiten kann zu einer insgesamt besseren Verträglichkeit der Antibiotikatherapie beitragen. Unerwünschte Herz-Kreislauf-Effekte machten 2016 nur einen Anteil von acht Prozent am Gesamtanteil aller UAW-Meldungen aus, wobei Kreislaufprobleme öfter im Zusammenhang mit der Anwendung von Antibiotika gesehen wurden und am ehesten im Zusammenhang mit therapiebedingten Durchfällen und entsprechenden Flüssigkeitsverlusten zu interpretieren sind.
Resümee
Das Spektrum der Arzneimittel, die im Zusammenhang mit UAW-Meldungen an die AKZ genannt werden, umfasst hauptsächlich Analgetika, Lokalanästhetika und Antibiotika und hat sich in den vergangenen zehn Jahren nicht verändert. Auch im Jahr 2016 verursachte wieder die Wirkstoffgruppe der Antibiotika mit Abstand am häufigsten eine UAW-Meldung an die Arzneimittelkommission Zahnärzte. Positiv hervorzuheben ist die Tatsache, dass erstmals Clindamycin die UAW-Statistik nicht mehr als Spitzenreiter anführt, wobei die Gesamtanzahl zahnärztlicher Verordnungen für Clindamycin im Meldezeitraum leider nicht rückläufig ist. Die gemeldeten Nebenwirkungen waren insgesamt leicht bis mittelgradig ausgeprägt. Für alle UAWs wurde eine restitutio ad integrum verzeichnet. Schwere Verläufe wurden nicht beobachtet.
Prof. Dr. med. Christoph Schindler
Medizinische Hochschule Hannover
Zentrum für Pharmakologie & Toxikologie
Carl-Neuberg-Str. 1
30625 Hannover
Dr. med. dent. Jens Nagaba
Bundeszahnärztekammer
Chausseestr. 13
10115 Berlin
Prof. Dr. med. Ralf Stahlmann
Charité Universitätsmedizin Berlin
Institut für Klinische Pharmakologie und Toxikologie
Luisenstr. 7
10117 Berlin
So melden Sie Nebenwirkungen
Die Verpflichtung zur Meldung unerwünschter Arzneimittelwirkungen durch den Zahnarzt ergibt sich aus der zahnärztlichen Berufsordnung in ihrer aktuellen Fassung vom 11.11.2017: Gemäß § 2 Absatz 6 ist der Zahnarzt verpflichtet, die ihm aus seiner zahnärztlichen Behandlungstätigkeit bekannt werdenden unerwünschten Arzneimittelwirkungen der Arzneimittelkommission Zahnärzte zu melden. Vorkommnisse, die im Rahmen der Diagnostik oder Behandlung von mit Medizinprodukten versorgten Patienten bekannt werden, sind dem Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) und der Arzneimittelkommission der deutschen Zahnärzteschaft bei der Bundeszahnärztekammer zu melden. Insbesondere unerwartete UAWs, UAWs zu neuen Arzneimitteln sowie klinisch besonders schwere beziehungsweise prolongierte Verläufe sollten gemeldet werden. Hierzu ist lediglich das Ausfüllen und Absenden des im Internet unter www.bzaek.de/fuer-zahnaerzte/arzneimittelkommission/nebenwirkungsmeldungen.html zum Download bereitstehenden Formulars erforderlich. Bitte vermerken Sie unbedingt den Handelsnamen, den Wirkstoff und die angewendete Dosis beziehungsweise die Applikationsart (zum Beispiel oral, s.c., i.v.) des verdächtigten Präparats und die Dauer der Anwendung in diesem Formular sowie in kurzen Stichworten die beobachtete unerwünschte Symptomatik des Patienten. Bitte vermerken Sie ebenfalls Ihren Namen und die Praxisadresse als Absender. Der Meldebogen ist so ausgelegt, dass der für den Zahnarzt erforderliche Zeitaufwand für das Ausfüllen des Formulars 3,5 Minuten nicht überschreiten sollte. Es besteht zusätzlich die Möglichkeit, den individuell gemeldeten Fall in Form eines kurzen Beratungsbriefes unabhängig durch die AKZ bewerten zu lassen. Die Anforderung eines Beratungsbriefes wird insbesondere dann empfohlen, wenn es sich um eine schwere unerwünschte Arzneimittelwirkung handelt beziehungsweise wenn eine bisher in der Fachinformation des entsprechenden Präparats noch nicht beschriebene unerwünschte Arzneimittelwirkung vermutet wird.
Die Arzneimittelkommission Zahnärzte (AKZ)
Um die Arzneimittelsicherheit auch nach der Zulassung eines Arzneimittels gewährleisten zu können ist es notwendig, Einzelberichte zu Verdachtsfällen von unerwünschten Arzneimittelwirkungen (UAWs) und Wechselwirkungen, die im Zusammenhang mit der Anwendung eines Arzneimittels in der klinischen Praxis bekannt werden, von zentraler Stelle systematisch zu erfassen und auszuwerten. Für den zahnärztlichen Bereich wird diese Aufgabe von der Arzneimittelkommission Zahnärzte (AKZ) wahrgenommen. Die AKZ ist ein gemeinsamer Ausschuss von BZÄK und KZBV. Sie besteht aus acht bis zehn Experten unterschiedlicher Fachrichtungen, darunter Pharmakologen, Toxikologen, Werkstoffkundler, Spezialisten für Implantologie und niedergelassene Zahnärzte, die sich auf Teilgebiete der zahnärztlichen Arzneimitteltherapie spezialisiert haben. Die AKZ führt die Bezeichnung Pharmakovigilanzzentrum als Anerkennung ihres Beitrags zur Qualität und Sicherheit von Arzneimitteln und Medizinprodukten.
Meldestatistik der AKZ
Seit 1995 wurden bis zum 31.12.2016 von Zahnärzten insgesamt 1.980 Meldungen an die AKZ abgegeben (Abbildung 1). Die Anzahl der jährlich gemeldeten Nebenwirkungen schwankt zwischen minimal 37 (1995) und maximal 158 (2005) Meldungen. Im Jahr 2016 gingen bei der AKZ insgesamt 102 Meldungen zu zahnärztlich verordneten Arzneimitteln, mehrheitlich von niedergelassenen Zahnärzten, ein. Der Anteil der von Zahnärzten in Deutschland gemeldeten Verdachtsfälle unerwünschter Arzneimittelwirkungen (UAWs) ist mit 0.9 Prozent insgesamt gering: Beim BfArM in Bonn wurden im gleichen Zeitraum insgesamt 64.108 Berichte über UAWs registriert [BfArM, 16.5.2017]. Davon stammten 52.007 Meldungen (81 Prozent ) direkt von pharmazeutischen Unternehmen. Die übrigen 12.101 Meldungen (19 Prozent ) wurden zum überwiegenden Teil von den Arzneimittelkommissionen der Ärzte (AkdÄ) (37,1 Prozent), der Apotheker (AMK) (21,7 Prozent) und anderer Heilberufe (15,5 Prozent) beziehungsweise sonstiger Meldequellen (24,8 Prozent) an das BfArM weitergeleitet.
Literatur
AWMF 007/091 – Bisphosphonat-assoziierte Kiefernekrose (BP-ONJ) und andere medikamentenassoziierte Kiefernekrosen 04/2012
Musterberufsordnung der BZÄK vom 11.11.2017
BfArM: Ergebnisprotokoll der 80. Routinesitzung nach § 63 AMG am 16.5.2017: Eingänge zu UAW-Berichten Sachstand BfArM
Halling F: Zahnärztliche Arzneiverordnungen. In: Schwabe U, Paffrath D, Ludwig WD, Klauber J: Arzneiverordnungs-Report 2017; DOI 10.1007/978–3–662–54630–7_47;
Schindler C, Stahlmann R: Sultamicillin als therapeutische Alternative zu Amoxicillin und Clavulansäure. ZM 2014 Nr 104, 13A
Stahlmann R, Schindler C: Antibiotika in der Zahnmedizin – denken Sie an die neurotoxischen Nebenwirkungen? ZM 11 2016
Mishra MB, Khan ZY, Mishra S: Gingival overgrowth and drug association: a review. Ind J Med Sci 2011; 65: 73–82
Sucu M, Yuce M, Davitoglu M: Amlodipine-induced massive gingival hypertrophy. Can Fam Physician 2011; 57: 436 – 7