Rezidiv einer Keratozyste im Unterkiefer eines kardial vorbelasteten Patienten
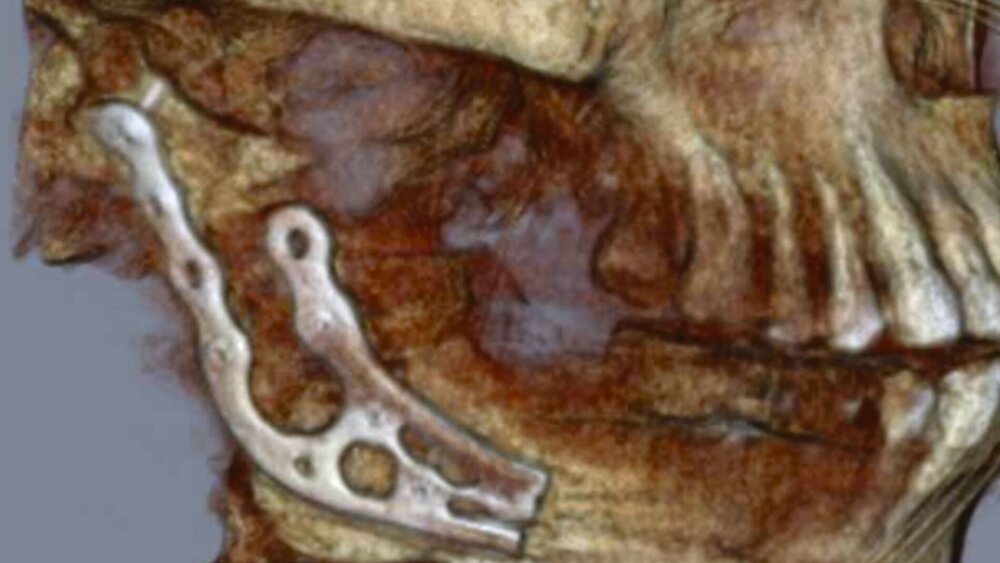
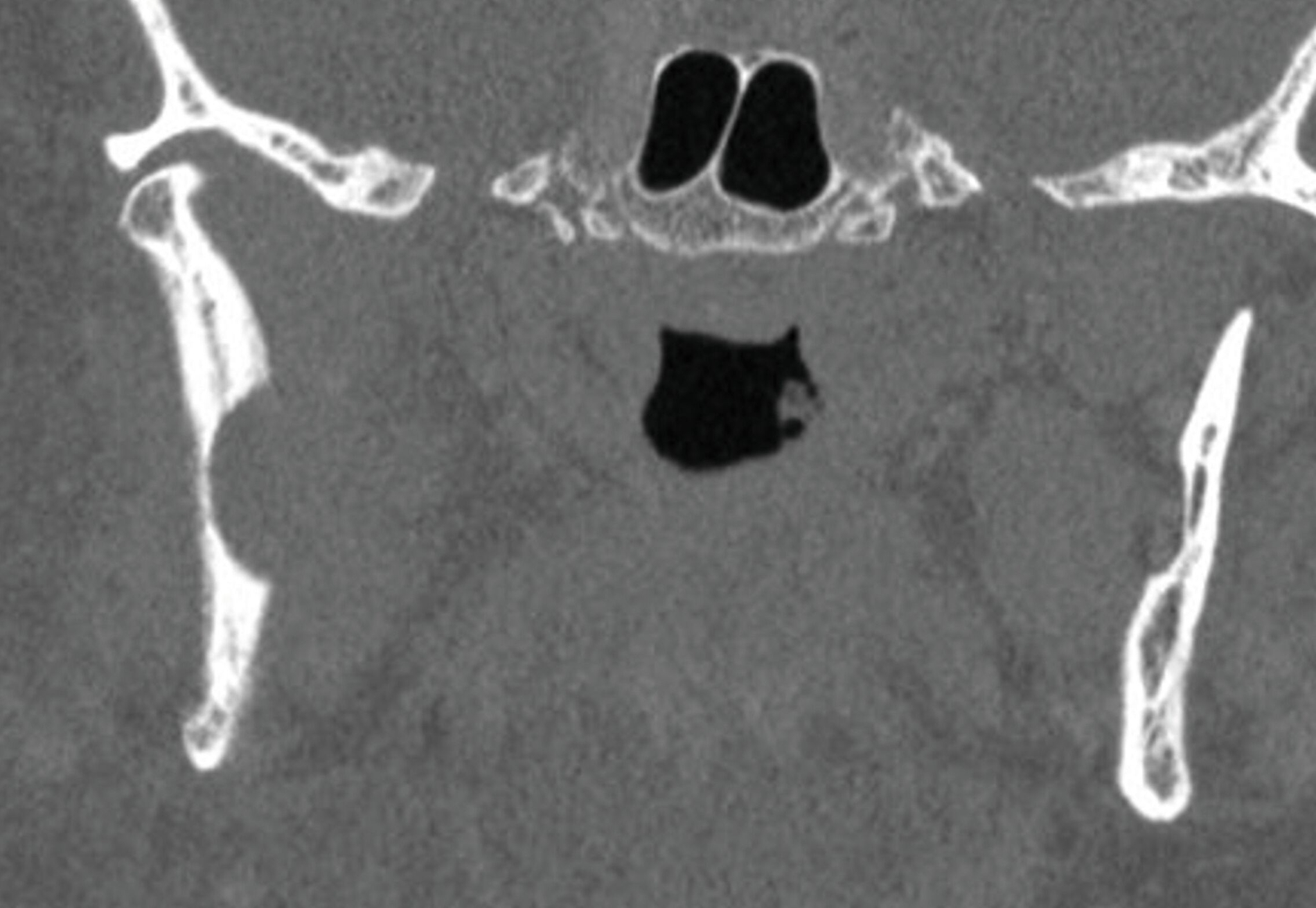
Ein 75-jähriger Patient stellte sich zur Nachkontrolle nach der Entfernung einer Keratozyste im rechten Unterkiefer vor, die vor mehr als fünf Jahren in einer anderen Einrichtung durchgeführt worden war. In der Zwischenzeit war aufgrund eines perimandibulären Abszessgeschehens in derselben Region eine extraorale Inzision vorgenommen worden. Die Panoramaschichtaufnahme zeigte im Vergleich zur Voruntersuchung eine fortschreitende multifokale Osteolyse des rechten aufsteigenden Unterkieferasts, was sich durch die ergänzende Computertomografie bewahrheitete (Abbildung 1). Eine enoral durchgeführte Probeentnahme bestätigte die Arbeitsdiagnose eines Rezidivs der zuvor diagnostizierten Keratozyste.
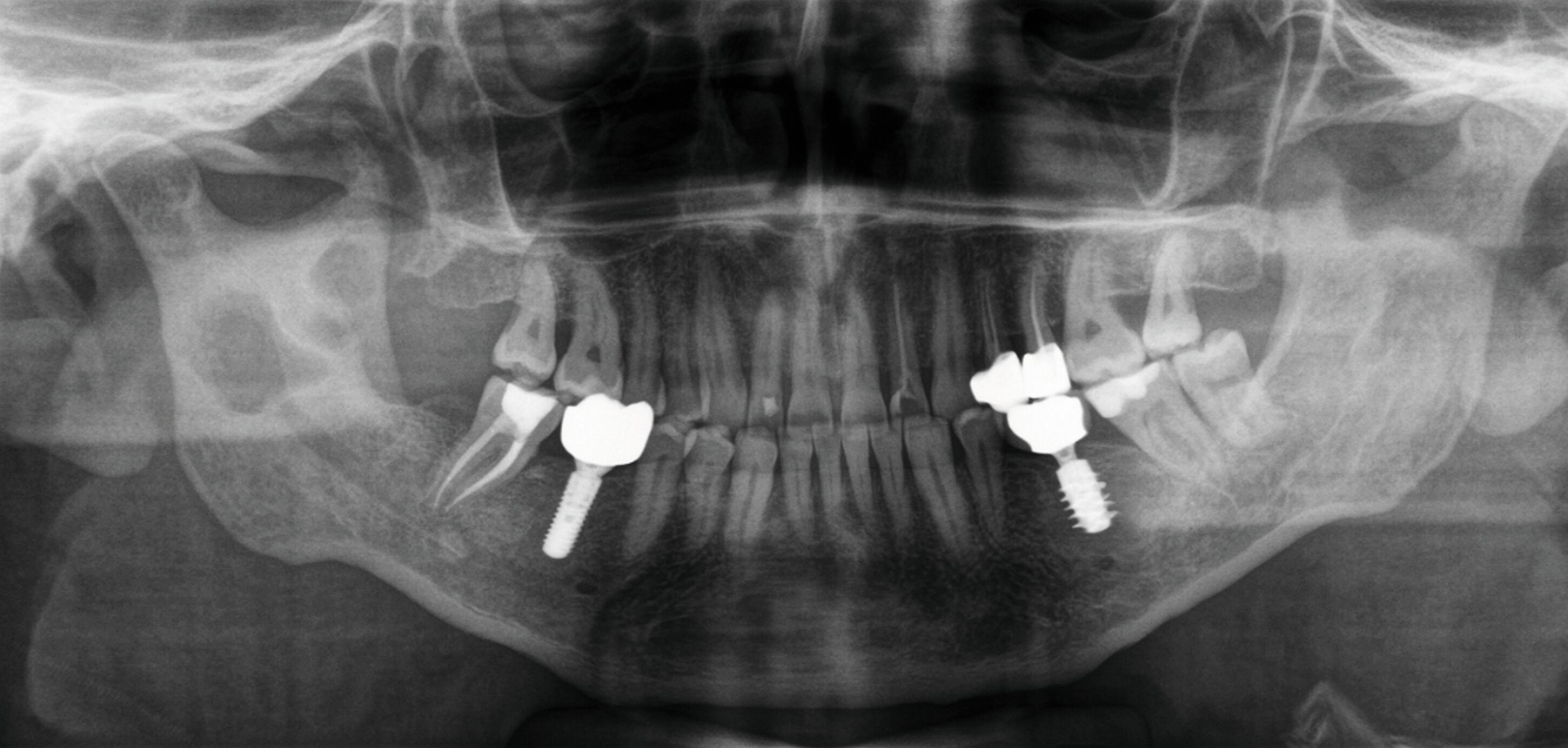
In der allgemeinen Anamnese fiel eine signifikante kardiale Vorbelastung auf, einschließlich des Zustands nach Implantation eines Einkammer-Defibrillators sowie einer transfemoralen Mitralklappenrekonstruktion aufgrund einer schweren primären Mitralklappeninsuffizienz. Vor acht Jahren war zudem ein Kolonkarzinom diagnostiziert und primär operativ behandelt worden. Die Dauermedikation umfasste unter anderem eine orale Antikoagulation mit Rivaroxaban 20 mg p.o. 1-0-0. Bei der klinischen Untersuchung zeigte sich bei der Aufnahme eine Kribbelparästhesie des Nervus mentalis rechts, bei sonst intakter peripherer Durchblutung, Motorik und Sensibilität. Die Mundöffnung war auf 1,5 cm eingeschränkt. Die prothetisch und konservierend unvollständig versorgte Bezahnung sowie die übrige Mundschleimhaut wiesen keinen pathologischen Befund auf.
Mit dem Patienten wurden die verschiedenen Therapieoptionen ausführlich erörtert. Dabei wurden insbesondere die Zugangsmodalitäten (extraoral, enoral oder kombiniert extra- und enoral), das Ausmaß der chirurgischen Intervention (erneute erweiterte Zystektomie versus Kontinuitätsresektion) sowie die Rekonstruktionsmöglichkeiten (alloplastische versus autologe Rekonstruktion, mikrovaskuläres versus avaskuläres Knochentransplantat) mit den entsprechenden Risiken und möglichen Komplikationen besprochen.
Aufgrund der Rezidivsituation entschied man sich im gemeinsamen Konsens für eine Kontinuitätsresektion. Die ursprünglich anvisierte mikrovaskuläre Rekonstruktion wurde aufgrund der erwarteten verlängerten Operationszeit, des hohen kardialen Risikos und des in angiologischen Voruntersuchungen als insuffizient eingeschätzten Gefäßstatus sowie der gegensätzlichen Entscheidung des Patienten zugunsten eines avaskulären autologen Beckenkammtransplantats geändert. Präoperativ wurde die Resektion entsprechend an einem gedruckten 3-D-Modell geplant und durchgeführt. Eine Rekonstruktionsplatte wurde präformiert und die Ausmaße des autologen Beckenkammtransplantats wurden festgelegt.
Intraoperativ wurde die Kontinuitätsresektion des Unterkiefers gemäß der präoperativen Planung vom Kieferwinkel bis knapp unterhalb der Incisura semilunaris über einen rein extraoralen Zugang durchgeführt, wobei der Nervus alveolaris inferior dargestellt und geschont wurde. Entscheidend war in diesem Fall, dass es zu keinem Zeitpunkt zu einer Eröffnung des Operationssitus nach enoral kam, wodurch eine Kontamination des avaskulären Knochens durch Speichel oder Speisereste vollständig vermieden werden konnte. Unsere klinische Erfahrung zeigt, dass eine solche Perforation, ebenso wie die Notwendigkeit einer Hautinsel, eine mikrovaskuläre Rekonstruktion dringend erforderlich gemacht hätte.
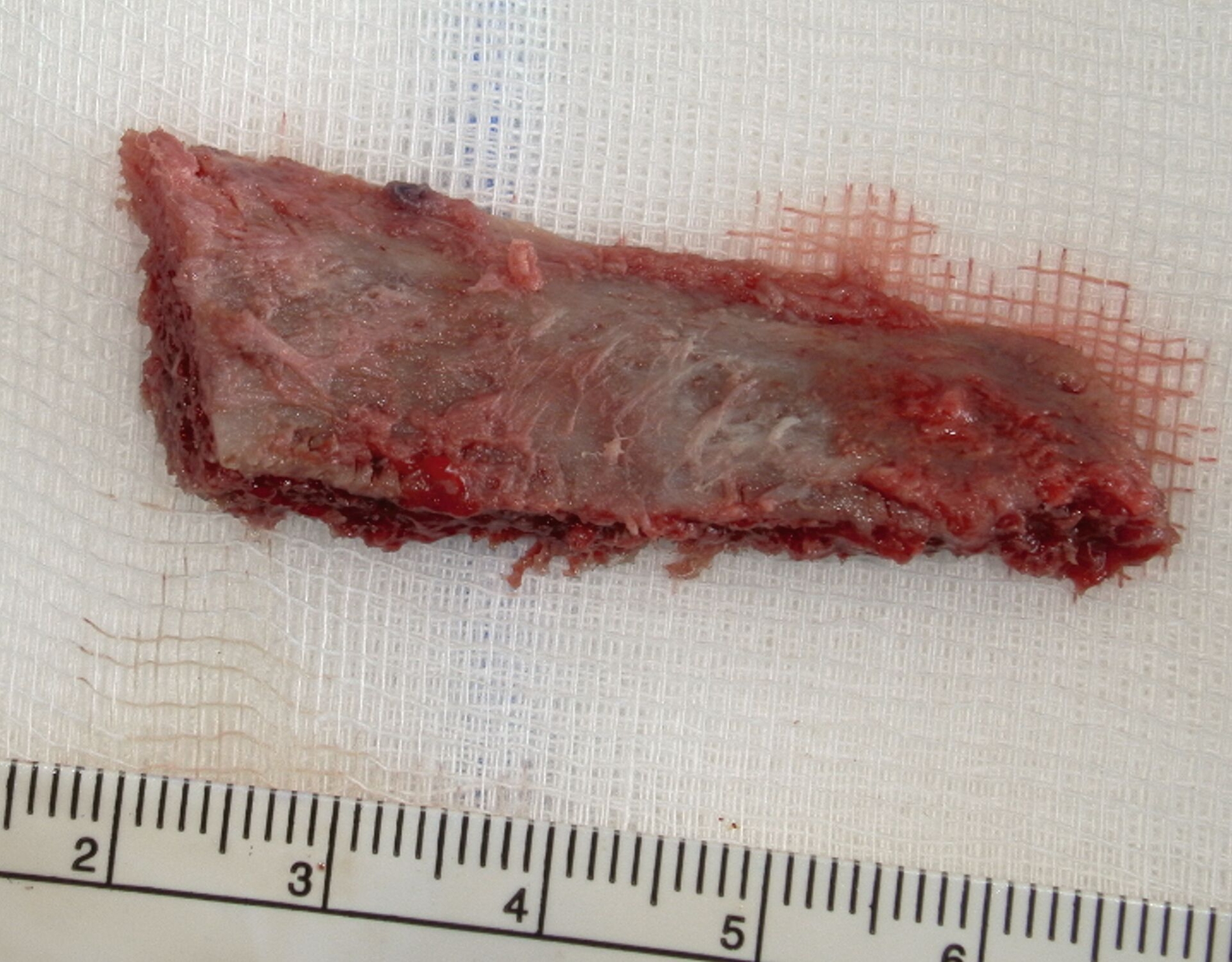
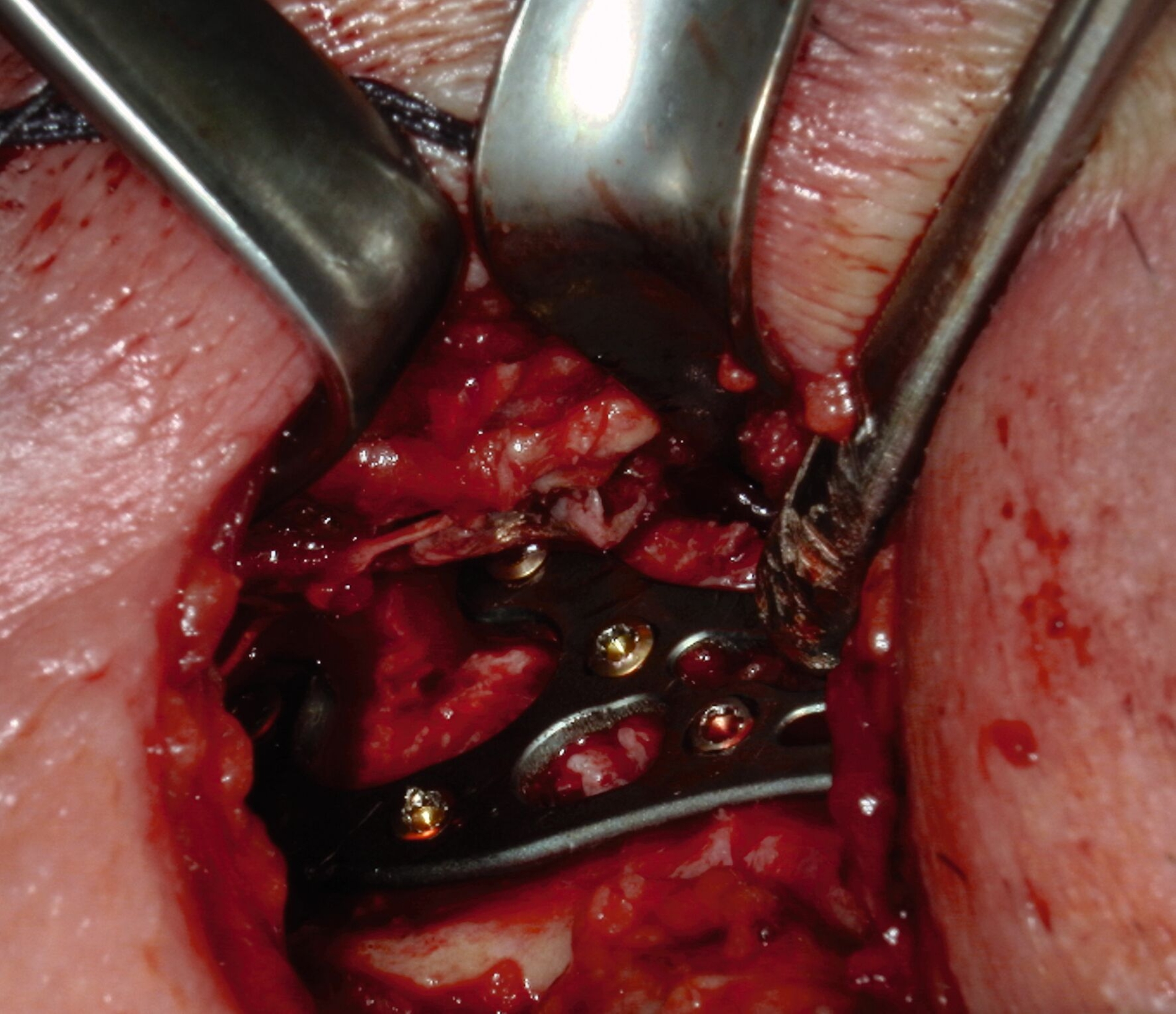
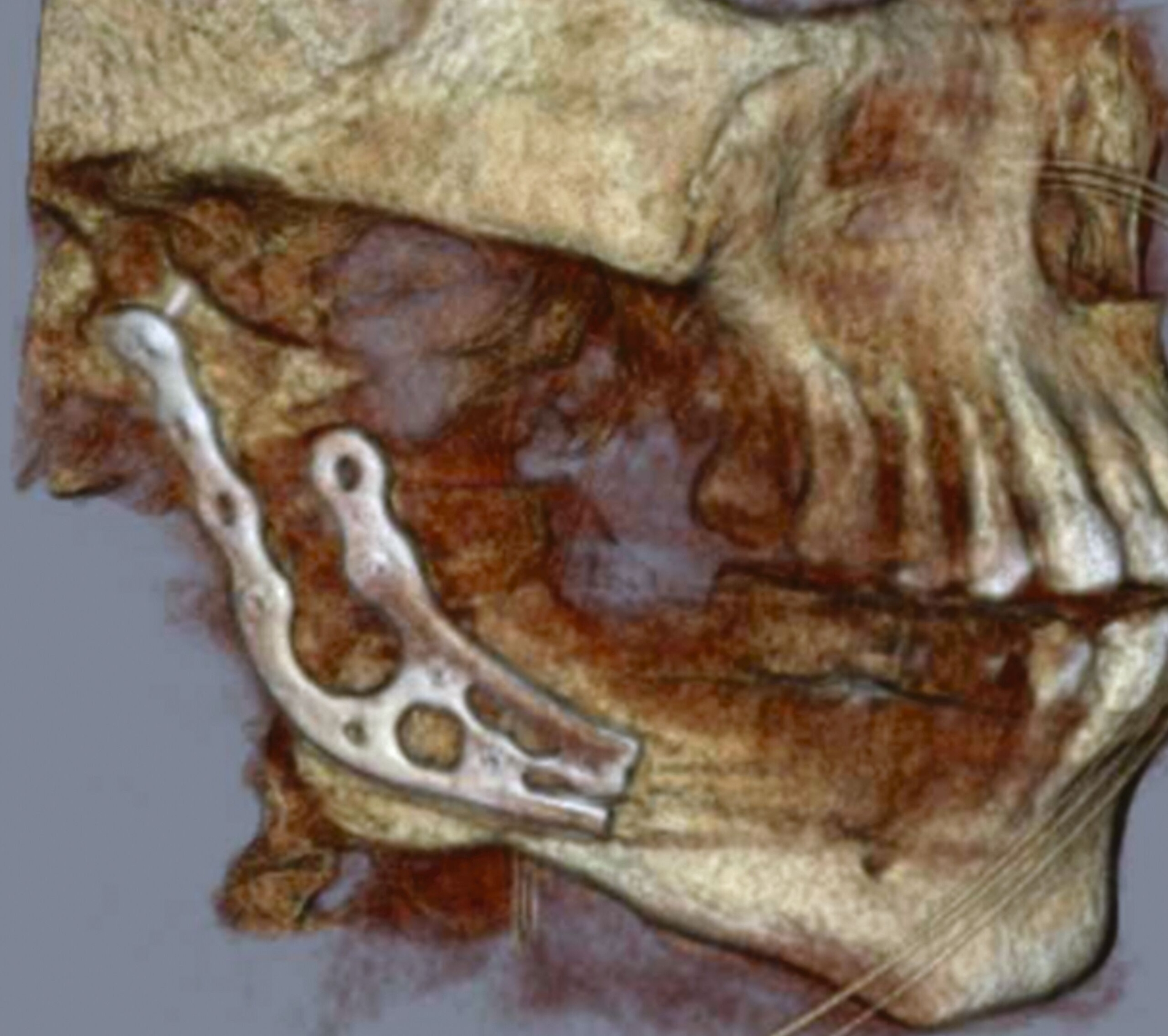
Danach wurde ein avaskuläres Beckenkammtransplantat vom rechten Becken entnommen. Die Auswahl eines avaskulären Knochentransplantats wurde aufgrund der klinischen Umstände und der präoperativen Planung bevorzugt, um eine möglichst schonende und risikoarme Vorgehensweise zu gewährleisten. Das Transplantat wurde anschließend in regelhafter Okklusion mittels präformierter Rekonstruktionsplatte eingebracht und osteosynthetisch fixiert. (Abbildungen 2 und 3).
Die histopathologische Untersuchung bestätigte die Verdachtsdiagnose eines in toto entfernten Rezidivs der Keratozyste.
Der Heilungsverlauf gestaltete sich unter antibiotischer und analgetischer Abdeckung sowie der Umstellung auf nasogastrale Sondenernährung komplikationslos. Der Patient konnte nach ausführlicher Aufklärung über postoperative Verhaltensweisen am fünften postoperativen Tag in die ambulante Nachsorge entlassen werden. Nach zwei und vier Wochen post operationem zeigte sich eine stadiengerechte Wundheilung bei stabilen Wundverhältnissen. Das präoperativ diagnostizierte sensible Defizit am ipsilateralen Nervus alveolaris inferior erholte sich komplett.
Diskussion
Im vorliegenden Fall handelte es sich um ein Rezidiv einer Keratozyste, das eine Unterkieferkontinuitätsresektion erforderlich machte. Die Keratozyste gehört zu den entwicklungsbedingten Zysten und zählt neben den follikulären und den entzündlich bedingten radikulären Zysten zu den häufigsten Kieferzysten. Epidemiologisch sind Männer häufiger betroffen als Frauen, mit einem Häufigkeitsgipfel in der dritten Lebensdekade. Die bevorzugte anatomische Region ist der Unterkiefer, insbesondere im Bereich des Kieferwinkels und des aufsteigenden Unterkieferastes [Thiem et al., 2019; Dioguardi et al., 2024].
Die Diagnose basiert meist auf einem radiologischen Zufallsbefund, der eine klar begrenzte uni- oder multilokuläre Radioluszenz zeigt. Die Zyste kann mit retinierten Zähnen, insbesondere impaktierten Unterkieferweisheitszähnen, assoziiert sein. Resorptionsvorgänge an Zahnwurzeln oder den retinierten Zähnen sind selten. Große Keratozysten können sich symptomatisch mit Schmerzen, Schwellungen und je nach Lokalisation mit nervalen Einschränkungen manifestieren [de Castro et al., 2018]. Multiple Keratozysten können auch im Rahmen des autosomal-dominant vererbbaren Gorlin-Goltz-Syndroms auftreten und mit dermalen Basalzellkarzinomen, Kalzifizierung der Falx cerebri sowie weiteren skelettalen und entwicklungsbedingten Pathologien einhergehen [Bresler et al., 2016].
Differenzialdiagnostisch müssen neben den eingangs erwähnten Kieferzysten auch weitere osteolytische Prozesse des Kiefers, wie das odontogene Myxom, das Ameloblastom, das zentrale Riesenzellgranulom und das Osteosarkom, ausgeschlossen werden [Römer et al., 2020; Tandon et al., 2024].
Mit der 4. Auflage der WHO-Klassifikation der Kopf-Hals-Tumoren von 2017 wird die Keratozyste wieder den Kieferzysten zugeordnet. Der Begriff des keratozystisch-odontogenen Tumors und die semantische Klassifikation als Knochentumor wurden verlassen [Speight und Takata, 2018]. Dies wird auch in der 2022 erschienenen 5. Auflage bestätigt. Der Hintergrund der Diskussion um eine neoplastische Entität der Zyste liegt in der klinisch häufig zu beobachtenden aggressiven Wachstumstendenz mit einer hohen Rezidivrate. Auch eine „echte“ maligne Entartung ist in seltenen Fällen beschrieben. Molekularpathologisch sind diese Phänomene durch Mutationen in Tumorsuppressorgenen wie dem PTCH1-Gen und anderen erklärbar [Soluk-Tekkesin und Wright, 2022]. Zusätzlich weist die epitheliale Begrenzung der Keratozyste einen hohen Mitoseindex auf [Slusarenko da Silva et al., 2021].
Neben der histopathologischen Zuordnung zu den Zysten oder Neoplasien wird auch die entsprechende chirurgische Therapie weiterhin diskutiert, da sie maßgeblich die Rezidivrate beeinflusst. Die Ansätze reichen von konservativen Maßnahmen wie Enukleation oder Marsupialisation bis hin zur (Kontinuitäts-)Resektion. In einem kürzlich erschienenen Review evaluierten die Autoren die unterschiedlichen operativen Vorgehensweisen bei Vorliegen einer Keratozyste in Bezug auf die Rezidivrate. Aufgrund der heterogenen Datenlage konnte jedoch keine klare Therapieempfehlung ausgesprochen werden [Dioguardi et al., 2024]. Somit bleibt das Ausmaß der chirurgischen Intervention derzeit eine individuelle Therapieentscheidung.
Additive Maßnahmen wie die Anwendung der Carnoy'schen Lösung haben aufgrund ihrer potenziellen Neurotoxizität ihren Stellenwert bei chirurgischen Eingriffen verloren. Aktuelle Studien sehen jedoch die topische Anwendung von 5-Fluorouracil nach Enukleation als vorteilhaft an, um die Rezidivrate zu senken [Barua et al., 2023].
Im vorliegenden Fall wurde aufgrund der Rezidivsituation und der anatomischen Lage der Pathologie eine Kontinuitätsresektion gewählt. Zur Wiederherstellung solcher Defekte stehen prinzipiell alle Möglichkeiten der rekonstruktiven Leiter zur Verfügung. Als Goldstandard gilt die Rekonstruktion mittels mikrovaskulär-anastomierten ossären oder osseomyokutanen Transplantaten, je nach Defektsituation [Gallegos-Hernández et al., 2019; Gielisch et al., 2023; Thiem et al., 2024]. Bei Vorliegen einer schweren Komorbidität, wie in diesem Fall, und insbesondere bei einer trotz ausführlicher Aufklärung ablehnenden Haltung der betroffenen Patienten, müssen alternative Behandlungsstrategien wie avaskuläre Transplantate oder alloplastische Rekonstruktionen als Therapiealternativen in Betracht gezogen werden.
Fazit für die Praxis
Trotz der Merkmale einer Neoplasie (infiltratives Wachstum, hohe Rezidivrate und molekularpathologische Marker) wird die Keratozyste wieder der Entität der Kieferzysten zugeordnet.
Die Keratozyste zählt nach der radikulären und follikulären Zyste zu den häufigsten Kieferzysten.
Oft handelt es sich um einen radiologischen Zufallsbefund, eine histopathologische Sicherung zur Abgrenzung von den wichtigsten Differenzialdiagnosen wie Ameloblastom oder Osteosarkom ist zwingend notwendig.
Das Ausmaß der chirurgischen Therapie bleibt eine individuelle Entscheidung.
Eine engmaschige und langfristige klinische und radiologische Nachsorge ist zwingend indiziert.
Zusammenfassend verdeutlicht der Fall einerseits die Sonderstellung der Keratozyste mit ihrer aggressiven Wachstums- und Rezidivtendenz, die eine langfristige und engmaschige Nachsorge erforderlich macht. Andererseits bleiben die Therapieentscheidung sowie das chirurgische Ausmaß der Intervention und die mögliche Wiederherstellung eine individuelle Entscheidung, abhängig von der Pathologie, ihrer anatomischen Lage sowie der Patientenkonstitution und Komorbiditäten.
Literaturliste
Barua CG, I Ali, A Tripathi, A Malakar and PK Singha: The Role of 5-Fluorouracil in Preventing Recurrence After Enucleation of Odontogenic Keratocyst: A Case Report. Cureus 15:e44777, 2023.
Bresler SC, BL Padwa and SR Granter: Nevoid Basal Cell Carcinoma Syndrome (Gorlin Syndrome). Head and Neck Pathology 10:119-124, 2016.
de Castro MS, CA Caixeta, ML de Carli, NV Ribeiro Júnior, M Miyazawa, AAC Pereira, FF Sperandio and JAC Hanemann: Conservative surgical treatments for nonsyndromic odontogenic keratocysts: a systematic review and meta-analysis. Clin Oral Investig 22:2089-2101, 2018.
Dioguardi M, C Quarta, D Sovereto, GA Caloro, A Ballini, R Aiuto, A Martella, L Lo Muzio and M Di Cosola: Factors and management techniques in odontogenic keratocysts: a systematic review. Eur J Med Res 29:287, 2024.
Gallegos-Hernández JF, A Martínez-Miramón and A Reyes-Vivanco: Fibular free flap in mandible reconstruction, a long-term follow-up. Cir Cir 87:267-271, 2019.
Gielisch MW, F Siegberg, DGE Thiem, S Blatt, D Heimes and PW Kämmerer: A novel alloplastic grid reconstruction plate for the mandible - Retrospective comparative clinical analysis of failure rates and specific complications. J Craniomaxillofac Surg 51:448-453, 2023.
Römer P, F Schnaith and PW Kämmerer: Der besondere Fall mit CME: Keratozyste oder Ameloblastom? Zahnärztliche Mitteilungen 110:76-79, 2020.
Slusarenko da Silva Y, PJW Stoelinga, R Grillo and M da Graça Naclério-Homem: Cyst or Tumor? A systematic review and meta-analysis on the expression of p53 marker in Odontogenic Keratocysts. Journal of Cranio-Maxillofacial Surgery 49:1101-1106, 2021.
Soluk-Tekkesin M and JM Wright: The World Health Organization Classification of Odontogenic Lesions: A Summary of the Changes of the 2022 (5th) Edition. Turk Patoloji Derg 38:168-184, 2022.
Speight PM and T Takata: New tumour entities in the 4th edition of the World Health Organization Classification of Head and Neck tumours: odontogenic and maxillofacial bone tumours. Virchows Arch 472:331-339, 2018.
Tandon A, S Juneja, F Verma and R Raina: Odontogenic myxoma of the mandible: An update on pathogenesis and differential diagnosis. J Oral Maxillofac Pathol 28:146-150, 2024.
Thiem DGE, F Siegberg, S Vinayahalingam, S Blatt, M Krüger, B Lethaus, B Al-Nawas, R Zimmerer and PW Kämmerer: The Perfect Timing-Immediate versus Delayed Microvascular Reconstruction of the Mandible. Cancers (Basel) 16:2024.
Thiem DGE, BK Straub, M Krüger and PW Kämmerer: Der besondere Fall mit CME: Keratozyste im Oberkiefer. Zahnärztliche Mitteilungen 109:56-59, 2019.