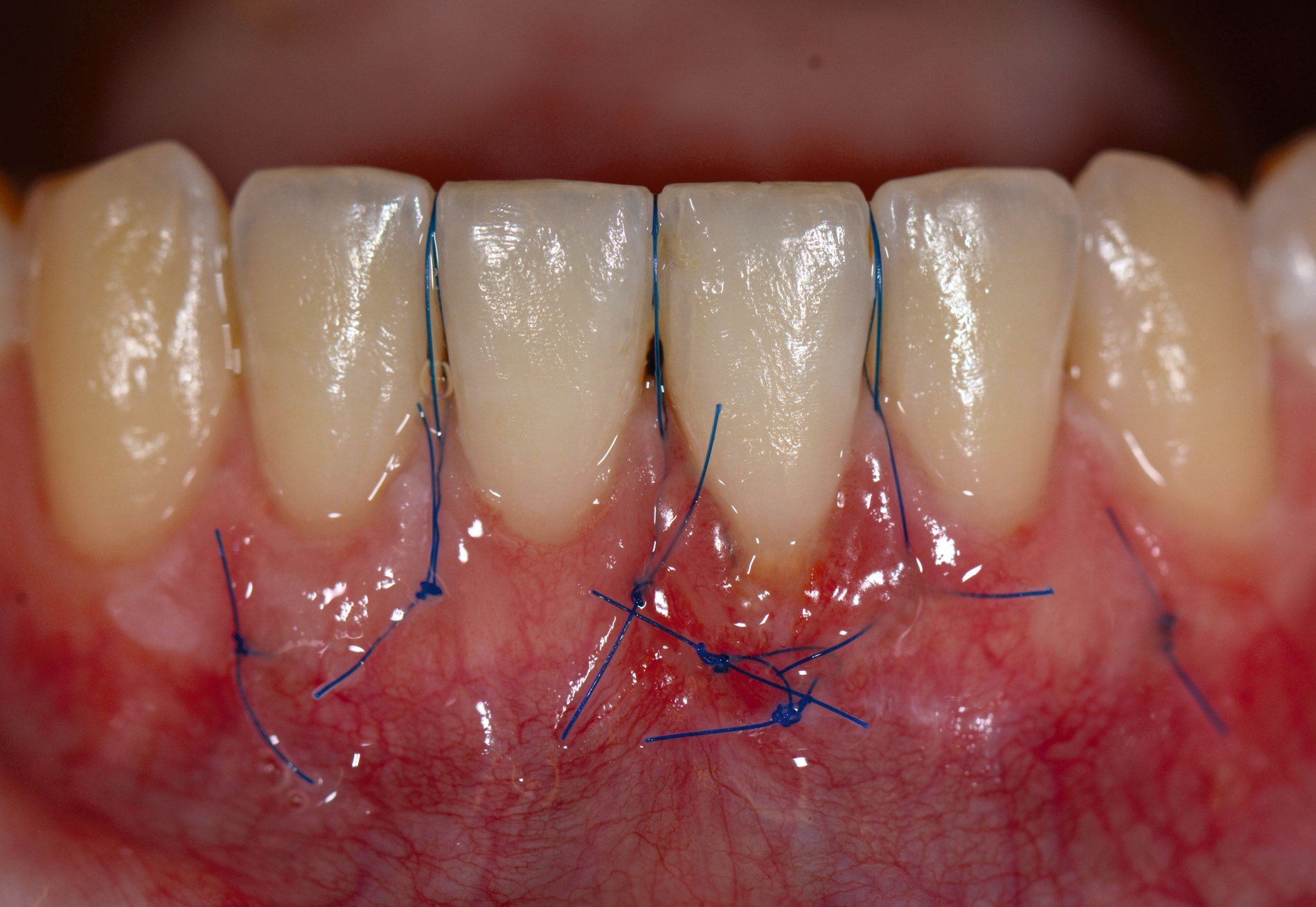
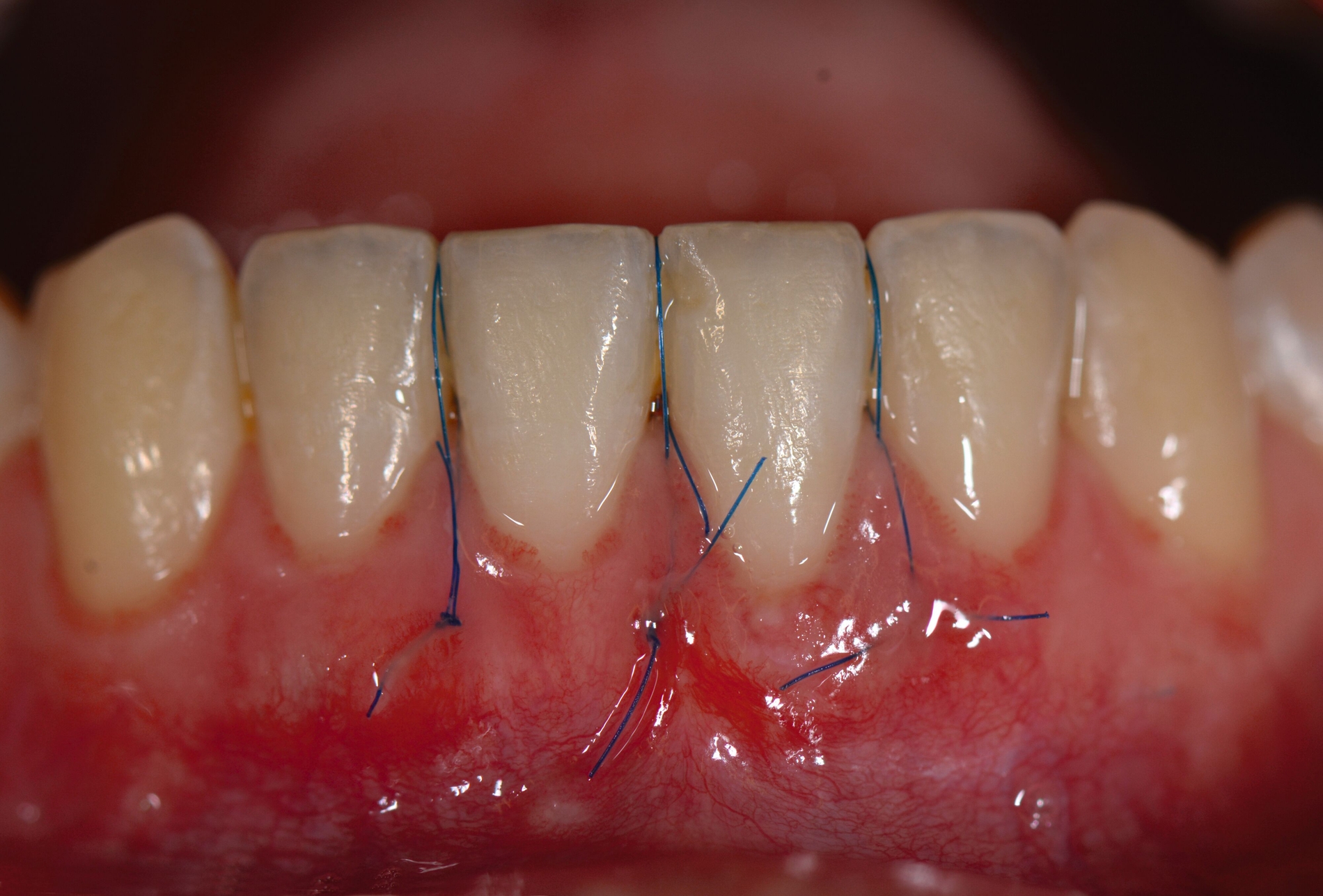
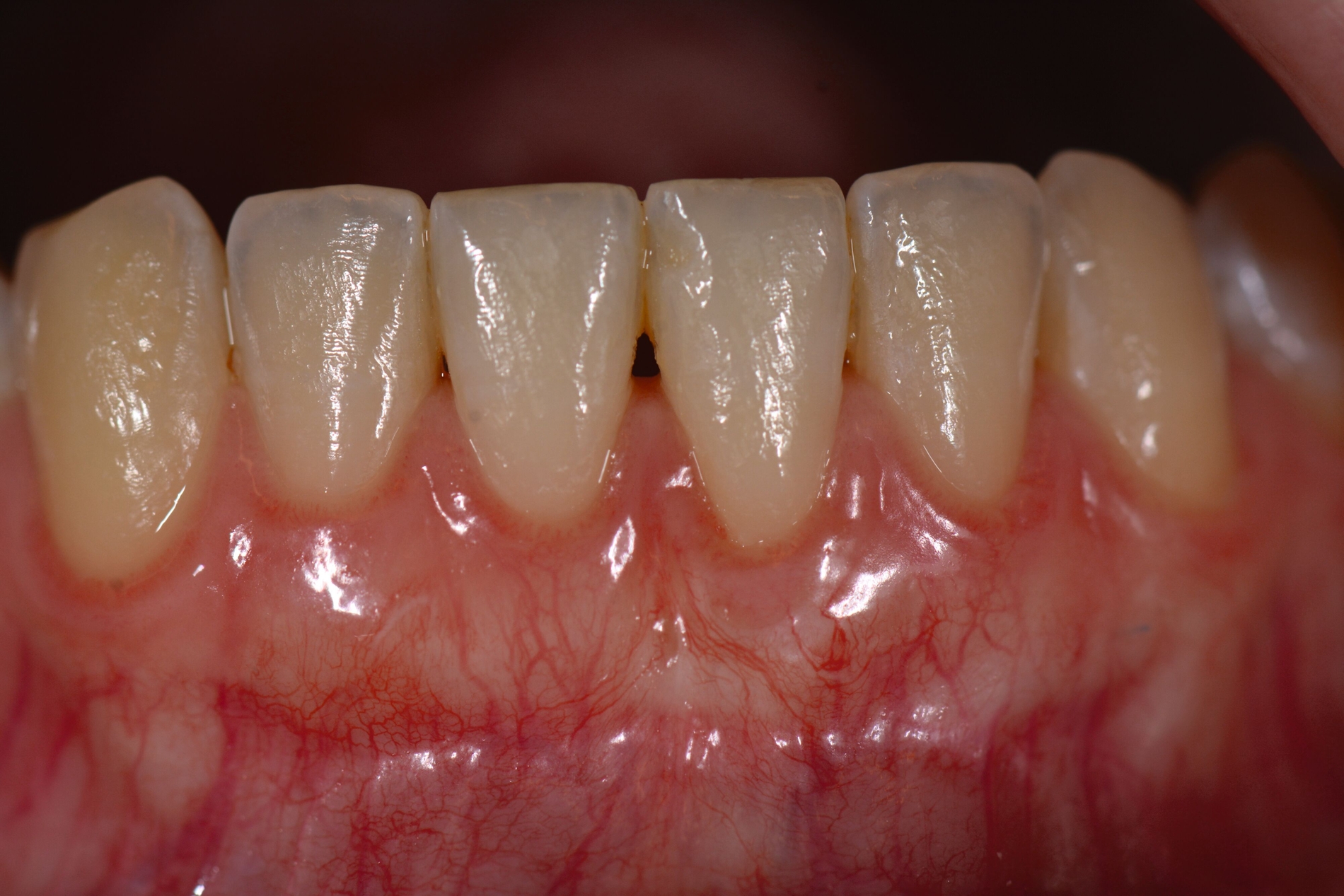
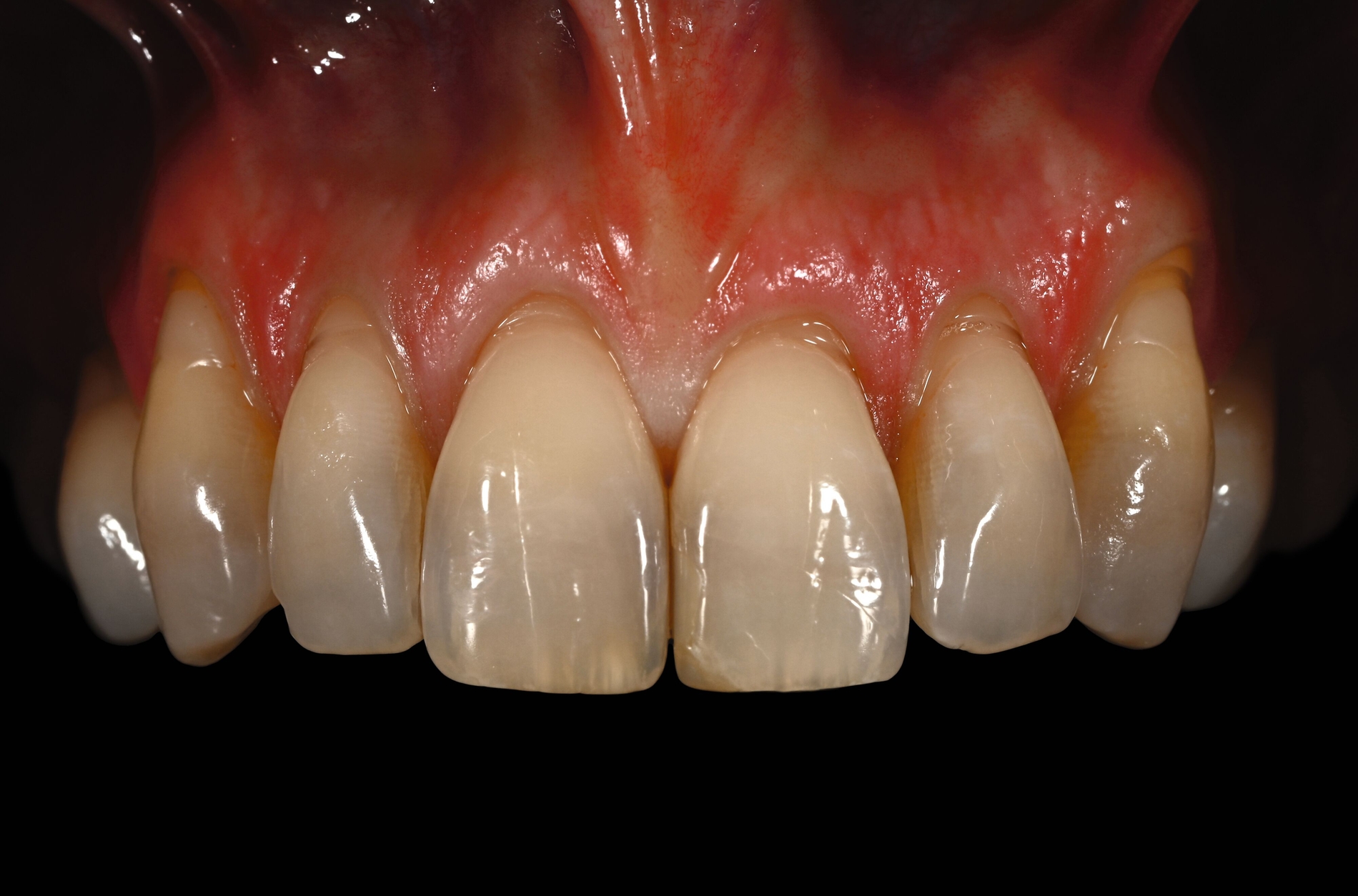
Update plastische Parodontalchirurgie: Transplantate & Heilungsbooster
Bindegewebstransplantate haben sich als eine der wirksamsten Methoden zur Behandlung von Rezessionen, Weichgewebsdefekten und zur Verbesserung der periimplantären Ästhetik etabliert und gelten als der Goldstandard. Ziel dieses Updates ist es, die unterschiedlichen Entnahmetechniken von autogenen Bindegewebstransplantaten zu vergleichen und die Vor- und Nachteile dieser Methoden zu bewerten. Zusätzlich werden xenogene Alternativen sowie Biologika zur Verbesserung und Beschleunigung der Wundheilung diskutiert und mit dem Goldstandard verglichen.
Autogene Bindegewebstransplantate
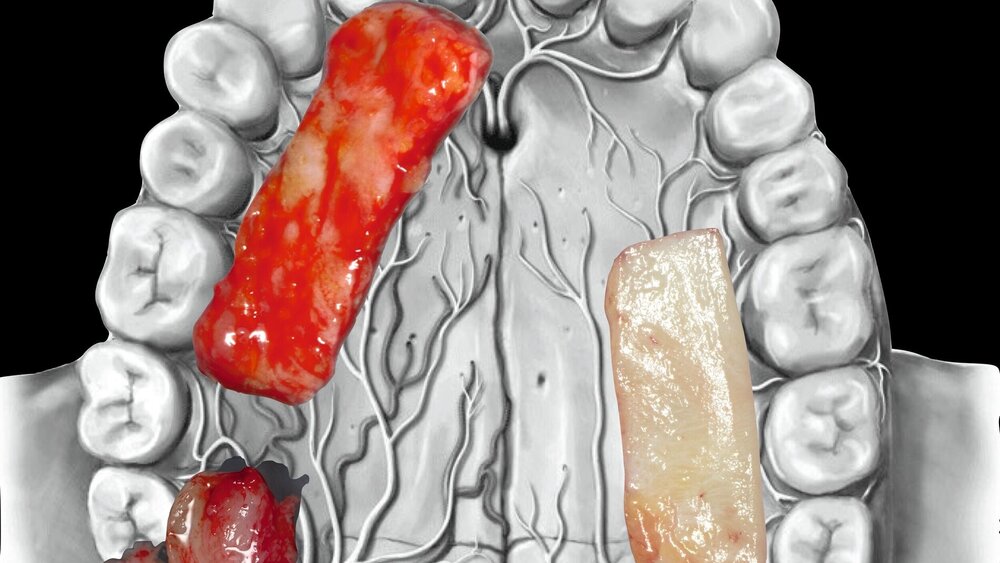
Bindegewebstransplantate (BGT) sind auf Basis aller systematischen Übersichtsarbeiten der vergangenen Jahre der Goldstandard zur Deckung von gingivalen Rezessionen um Zähne [Chambrone et al., 2022], aber auch Mittel der Wahl zur Korrektur von Gewebsdefekten um Implantate und überall dort, wo das primäre Ziel eine Volumenvermehrung ist [Tavelli et al., 2021]. So eindeutig die Literatur mit Blick auf den Vergleich mit anderen Optionen wie dermalen Matrizes oder den später noch beschriebenen Biologika ist, so wenige Daten gibt es zum Vergleich verschiedener Spenderregionen innerhalb der Mundhöhle, wobei die Entnahmestelle und -technik einen signifikanten Einfluss auf die Struktur des Transplantats hat.
Subepitheliales Bindegewebstransplantat (sBGT)
Das „klassische“ BGT wurde bereits in den 1970er-Jahren beschrieben und ist besonders verbreitet bei der Behandlung von gingivalen Rezessionen und der Weichgewebsaugmentation um Implantate. Das Transplantat wird durch eine sorgfältige Präparation unterhalb des Epithels vom lateralen und eher anterioren Gaumen gewonnen. Durch den Erhalt des bedeckenden Gewebes soll eine primäre Heilung sichergestellt werden. Die Höhe des Gaumendachs und somit die Entfernung zur Arteria palatina sowie die Dicke der Schleimhaut, vor allem über den palatinalen Wurzeln der Molaren zusammen mit den Rugae des anterioren Gaumens, sind die limitierenden Faktoren bei dieser Technik.
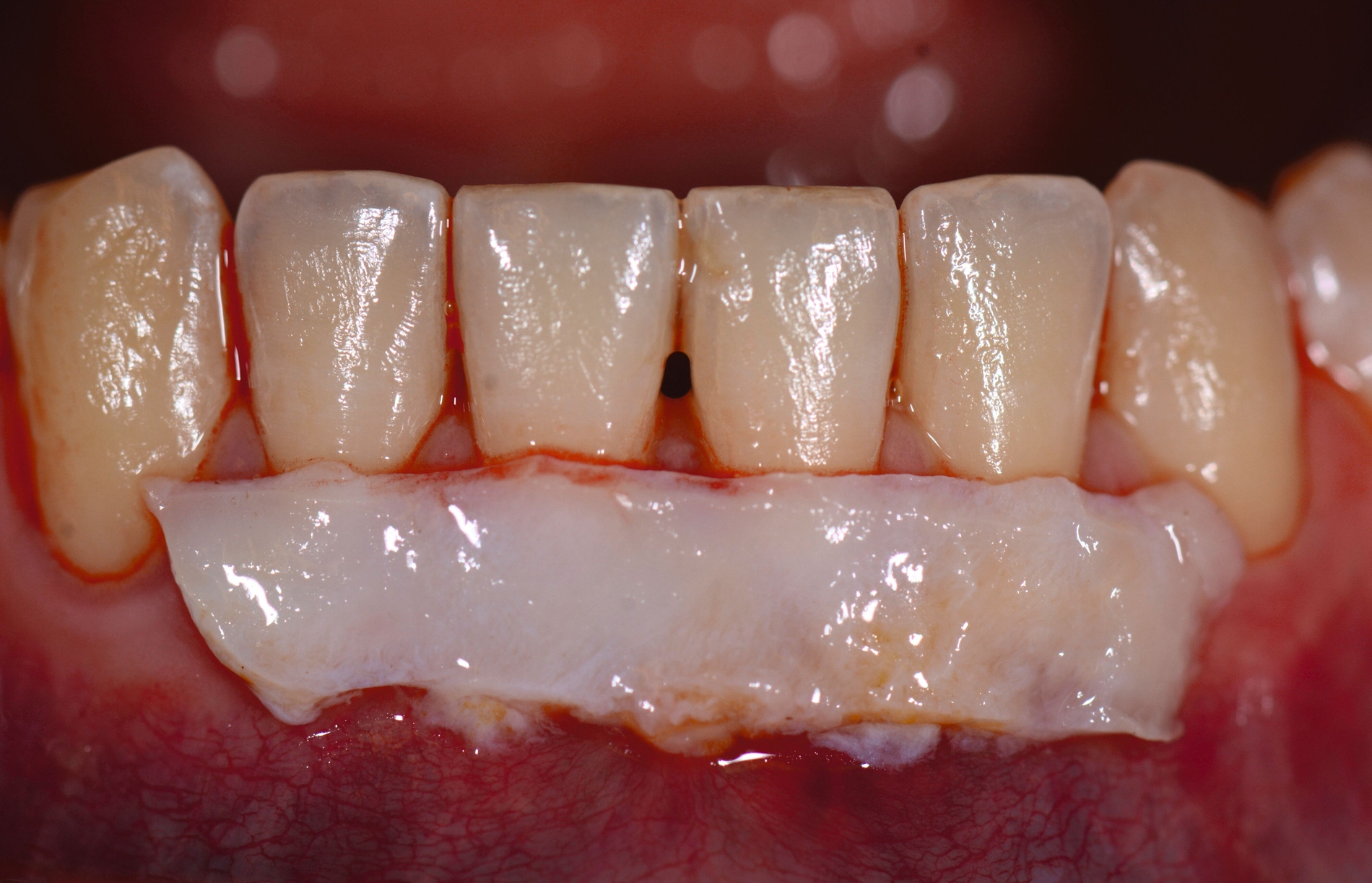
Trotz des Verbleibs des Epithels kann es zu sekundärer Wundheilung mit entsprechender Morbidität postoperativ kommen, besonders bei Techniken, die mehrere Inzisionen beinhalten, wie den sogenannten Trap-Door-Techniken, so dass sich die „Single-Incision-Technik“ durchgesetzt hat [Fickl et al., 2014]. Gegen eine übermäßige Blutung und postoperative Morbidität empfiehlt sich klinisch die routinemäßige Anwendung einer Verbandplatte, entweder in der Tiefziehtechnik oder präoperativ mittels eines Thermoplasts, so dass sich früh ein stabiles Blutkoagel bildet und die Wundheilung an der Entnahmestelle ungestört ablaufen kann. Dadurch wird die Morbidität klinisch deutlich reduziert. Das sBGT zeigt ästhetisch sehr gute Ergebnisse mit Blick auf Oberflächenstruktur sowie Farbe und kann unter anderem im Rahmen der Envelope- oder Tunneltechnik oder auch über einer Extraktionsalveole bewusst exponiert belassen werden, um zusätzlich befestigte Gingiva zu gewinnen.
Deepithelialisiertes Bindegewebstransplantat (dBGT)
Diese Technik hat in den vergangenen Jahren an Popularität gewonnen und beinhaltet die Entfernung des Epithels intraoral vor oder extraoral nach der Entnahme quasi eines freien Schleimhauttransplantats, wodurch mehr Lamina propria und Bindegewebe sowie weniger Submukosa und Fettgewebe erhalten bleiben, was klinisch auch einfach zu erkennen ist. Dies macht das dBGT besonders geeignet für die Verbreiterung der keratinisierten Mukosa und die Gewebeverdickung [Bertl et al., 2015]. Zusätzlich kann die Entnahme weiter dorsal erfolgen, da bei korrekter, oberflächlicher Entnahme in 1,5 bis 2 mm Dicke das Risiko für eine Gefäßverletzung minimal ist und auf dem Knochen noch Gewebe verbleibt.
Die Wundheilung nach dieser Technik erfolgt anders als beim sBGT immer sekundär, somit wurden bei Vergleichsstudien eine signifikant erhöhte Morbidität, Schwellungen und ein erhöhtes Nachblutungsrisiko beschrieben [Del Pizzo et al., 2002; Griffin et al., 2006], was jedoch bei entsprechender Versorgung des Gaumens umgegangen werden kann [Zucchelli et al., 2010]. Die Versorgung der Spenderregion kann mit Kollagenvlies, Cyanoacrylatkleber, Verbandplatte oder einer Kombination erfolgen. Dies kann die Morbidität deutlich reduzieren [Tavelli et al., 2019b]. Ein Vorteil von dBGT ist die Stabilität der Gewebedicke im Laufe der Zeit, was im Gegensatz zur beschriebenen Schrumpfung von sBGT steht, die häufig beobachtet wird [Zucchelli et al., 2018].
Eine Übersichtsarbeit, die sBGT und dBGT im Rahmen der Rezessionsdeckung verglich, empfahl primär die Anwendung des dBGT. So lag die mittlere Wurzelabdeckung nach zwölf Monaten mit dem sBGT bei 89,3 Prozent im Vergleich zu 94 Prozent beim dBGT. Die Daten der dBGT-Gruppe stützten sich jedoch nur auf die Ergebnisse einer einzigen Arbeitsgruppe und die Gruppen mit der höchsten durchschnittlichen Wurzeldeckung wurden für das sBGT berichtet, so dass hier ein gewisser Centereffekt vermutet werden kann. Weiterhin besteht bei dBGT ein gewisses Risiko für ästhetische Komplikationen wie eine keloidartige Narbenbildung, eine unnatürliche Randsituation oder eine deutlich hellere und glattere Oberfläche, wenn das Transplantat nicht korrekt gehandhabt wird, der Decklappen sehr dünn ist oder das Transplantat offen einheilt [Gluckman et al., 2019; Zucchelli et al., 2014b].
Neuere Daten haben weiterhin gezeigt, dass die Durchblutung des Decklappens durch ein dBGT signifikant länger reduziert ist als bei einem sBGT, was in der Folge zu häufiger auftretenden späten Komplikationen wie Zystenbildungen führt [Ragghianti-Zangrando et al., 2021]. Die vollständige Entfernung des Epithels – egal ob intra- oder extraoral – wird nicht immer erreicht [Couso-Queiruga et al., 2023], was letztlich zu Problemen bei der Einheilung mit unvollständiger Verbindung zum Decklappen oder mit der Wundunterlage wie der Wurzeloberfläche führen kann. So wurde von einer deutlich erhöhten Dehiszenzrate in etwa jedem zweiten Fall bei dicken dBGT (> 1,5 mm) mit entsprechend reduziertem ästhetischem Ergebnis berichtet [Zucchelli et al., 2014a].
Tubertransplantat (tBGT)
Das Bindegewebe wird hier aus dem Tuber maxillae entnommen und hat ähnliche Eigenschaften wie das dBGT. Die Entnahme gleicht im Grunde einer Tuberplastik oder distalen Keilexzision im Rahmen der Parodontaltherapie oder präprothetischen Chirurgie. Vorteilhaft ist die weit dorsal liegende Entnahmestelle, was zu einer sehr geringen Morbidität beiträgt, gleichzeitig jedoch die Entnahme anspruchsvoll gestalten kann und das zu gewinnende Volumen im Vergleich zu den oben beschriebenen, gängigeren Transplantaten reduziert. Während vom lateralen Gaumen auch mehrfach entnommen werden kann, ist dies vom Tuber nicht möglich. Studien zeigen, dass bei der Verwendung eines tBGT in einem Mukosalappen im Vergleich zu einem Mukoperiostlappen signifikant mehr keratinisierte Mukosa gewonnen werden kann (4,5 mm vs. 0,5 mm) [Puisys et al., 2021]. Ein Nachteil könnte jedoch die Neigung zu einer übermäßigen Wundreaktion sein, insbesondere wenn dicke Transplantate (> 3 mm) verwendet werden, was zu einer exostoseartigen Erscheinung führen kann [Tavelli et al., 2019a]. Der Versuch, eine derartige überschüssige Gewebeheilung zu entfernen, kann jedoch zu einer noch weiter überschießenden Reaktion führen [Gluckman et al., 2019]. Der genaue Pathomechanismus ist nicht bekannt, jedoch könnten Unterschiede in der Kollagenvernetzung und Fibroblastenreifung ursächlich sein. Ansonsten eignen sich die Transplantate zur gedeckten Einheilung bei singulären Rezessionen an Zahn und Implantat, zum Ponticaufbau oder zur Gewebsverdickung im Rahmen der Sofortimplantation.
Konklusion I
Bindegewebstransplantate spielen eine zentrale Rolle in der plastischen Parodontal- und Implantatchirurgie. Ihre Anwendung ermöglicht die effektive Behandlung von Weichgewebsdefekten und trägt wesentlich zur Verbesserung der ästhetischen Ergebnisse bei. Die Wahl der Entnahmestelle und -technik sollte sorgfältig abgewogen werden, um die besten klinischen und ästhetischen Ergebnisse zu erzielen. Während das sBGT aufgrund seiner Vorhersagbarkeit und ästhetischen Ergebnisse in vielen Fällen aus Sicht des Autors bevorzugt wird, bieten dBGT und tBGT spezifische Vorteile, insbesondere in Bezug auf die langfristige Stabilität, die Zunahme an befestigter Gingiva/Mukosa und die Weichgewebsverdickung. Weitere klinische Vergleichsstudien wären wünschenswert, um die Unterschiede der Transplantate und somit Empfehlungen für deren klinische Anwendungen klarer herauszuarbeiten.
Xenogene Weichgewebsersatzmaterialien
Das Weichgewebsmanagement oder -augmentationen sowohl in der Parodontologie als auch in der dentalen Implantologie werden, wie oben beschrieben, meist mit autogenem Gewebe vom Gaumen durchgeführt. Um die Morbidität der Patienten und das intra-/postoperative Komplikationsrisiko zu reduzieren, kann jedoch auch – wie im Bereich der Knochenaugmentation – auf xenogene Alternativen meist porcinen und dermalen Ursprungs zurückgegriffen werden. Vorteilhaft ist die unlimitierte Verfügbarkeit in Größe und Dicke. Diese Materialien zeigen entweder eine eher schwammartige oder eine kompakte Struktur und sind entweder nativ oder zusätzlich kreuzvernetzt. Somit zeigen die Materialien auch eine unterschiedliche Volumenstabilität mit Blick auf die Druckresistenz, aber auch auf die Resorptionskinetik beziehungsweise die Möglichkeit zur schnellen Besiedelung mit körpereigenen Zellen [Fischer et al., 2014]. Während der Einsatz als freies Schleimhauttransplantat aufgrund der fehlenden genetischen Information zur Keratinisierung nur eingeschränkt oder in Kombination mit autogenem Gewebe möglich ist, ist die gedeckte Verwendung von Kollagenmatrizes als Bindegewebsersatz abhängig von der Defektmorphologie immer besser dokumentiert und zu empfehlen.
Über die vergangenen Jahre sind immer mehr vor allem xenogene Gewebetransplantate auf dem Markt erschienen. Grundsätzlich lassen sich in Deutschland zwei Arten beobachten: zum einen porcine, azelluläre dermale Matrizes (pADM), zum anderen kreuzvernetzte Kollagen-Matrizes (KM).
Deckung gingivaler Rezessionen
Dabei ist aus wissenschaftlicher Sicht zu beachten, dass vor allem die Anwendung von allogenen ADM, die in Deutschland eine untergeordnete Rolle spielen, umfangreicher dokumentiert ist als porcine ADM. So stellt der koronale Verschiebelappen in Kombination mit allogenen ADM (aADM) eine valide Option zur Gingivaverdickung und Wurzeldeckung dar und scheint den KM überlegen zu sein [Chambrone et al., 2022]. In der gleichen Übersichtsarbeit wurde aber zugleich die Bedeutung der befestigten Gingiva für den Erfolg der Ersatzmaterialien und Biologika herausgestellt. Eine andere, kürzlich erschienene Übersichtsarbeit verglich aADM und pADM mit BGT. Sind eine vollständige Wurzeldeckung und langfristige Stabilität das Ziel, ist das BGT weiterhin überlegen. Doch dies wird mit einer längeren Behandlungsdauer und einer höheren Morbidität erkauft [Halim und Sulijaya, 2024]. Eine frühe klinische Studie zur Anwendung einer nativen KM zur Rezessionsdeckung mit Tunneltechnik berichtete von nur 42 Prozent vollständiger beziehungsweise 71 Prozent mittlerer Wurzeldeckung im Vergleich zu 85 Prozent beziehungsweise 90 Prozent mit BGT [Aroca et al., 2013]. Die Anwendung einer kreuzvernetzten, volumenstabilen KM erzielte bessere Ergebnisse (durchschnittliche Wurzeldeckung 75 Prozent), jedoch fehlte eine Vergleichsgruppe [Barootchi et al., 2023].
Periimplantärer Volumenaufbau
In Bezug auf aADM und Volumenaugmentationen wurde klinisch eine erfolgreiche Zunahme in vertikaler Abmessung von 0,62 mm und in horizontaler Breite von 1,72 mm nach sechs Monaten beschrieben, aber zur gleichen Zeit fand man eine Schrumpfung des post-operativen Volumens um mehr als 40 Prozent [Batista et al., 2001]. Bei der Anwendung von pADM zum Gewebeaufbau kommt es abhängig von der Defektform (singulär vs. muliple, Schaltlücke vs. Freiende) zu einem Volumenverlust von durchschnittlich 50 Prozent innerhalb der ersten sechs Monate, das gewonnene Volumen bleibt dann wohl aber bis zu 24 Monate stabil [Fischer et al., 2019]. Daneben wurde gezeigt, dass die vertikale Mukosaverdickung mittels aADM zu einer Reduktion des Knochenabbaus um Implantate führen kann [Puisys et al., 2015]. Eine weitere Arbeitsgruppe behandelte im Hundemodell chronische Kammdefekte mit einer porösen, kreuzvernetzten KM [Thoma et al., 2010]. Sie falteten eine 5 mm dicke KM zweimal und gewannen nach 84 Tagen 1,4 mm an Kammbreite. Dies spricht für eine starke Resorption oder Kompression des Materials. Man könnte spekulieren, dass die Komprimierung der porösen Struktur, das zelluläre Einwachsen und/oder eine zu schnelle Resorption zu diesem eher geringen Volumengewinn geführt haben.
Konklusion II
Kollagenbasierte Weichgewebsersatzmaterialien bieten eine zum Teil gut dokumentierte Alternative zum etablierten Goldstandard des BGT, wenn Volumenverdickung, kürzere Behandlungsdauer sowie reduzierte Morbidität primäres Ziel sind und eine unvollständige Wurzeldeckung langfristig akzeptabel ist. Mit dem derzeitigen Kenntnisstand ist nicht klar, ob die beschriebenen KM oder ADM als reines Gerüst fungieren, das schnell von Fibroblasten, endothelialen und epithelialen Zellen besiedelt werden soll, oder ob die Transplantate nur als Platzhalter dienen, die schließlich resorbiert werden, während neues Gewebe gebildet wird. Eine schwammartige Struktur könnte schneller von Zellen besiedelt werden, jedoch auch unter Druck eher kollabieren. Ein direkter, klinischer Vergleich von ADM und KM liegt aktuell weder für parodontale noch für periimplantäre Defekte vor.
Heilungsbooster
Die plastische Parodontalchirurgie hat aufgrund der Komplexität der Eingriffe, der Morbidität und der Langzeitstabilität nicht immer einen guten Stand in der täglichen Praxis. Die Einführung und Anwendung biologisch aktiver Substanzen wie Hyaluronsäure (HyA), Schmelz-Matrix-Proteine (SMP) und Eigenblutzentrifugaten wie zum Beispiel Platelet-rich Fibrin (PRF) könnte hier ein weiteres Puzzleteil sein, um die Verbreitung der plastischen Parodontalchirurgie weiter voranzutreiben. Diese Substanzen haben das Potenzial, die Heilung und Regeneration parodontaler Gewebe zu fördern, die postoperative Morbidität zu senken und so den Erfolg chirurgischer Eingriffe signifikant zu verbessern.
Hyaluronsäure
Die zusätzliche Anwendung von HyA ist einer der aktuellen Trends in der Zahnmedizin. HyA ist den Patient(inn)en häufig als Inhaltsstoff von Kosmetika oder aus anderen Bereichen der Medizin wie der Orthopädie bekannt. HyA ist ein natürlicher Bestandteil des Bindegewebes und zeichnet sich durch ihre hohe Wasserbindungsfähigkeit aus, was sie zu einem wichtigen Molekül für die Wundheilung macht. HyA fördert die Zellmigration und Proliferation, was zu einer beschleunigten Wundheilung und Narbenreduktion führt [Mueller et al., 2017]. In der Parodontalchirurgie wird HyA aufgrund ihrer entzündungshemmenden, antibakteriellen und wundheilungsfördernden Eigenschaften eingesetzt. Präklinisch konnte nachgewiesen werden, dass nicht nur das Deckungsergebnis durch HyA verbessert werden kann, sondern auch die Bildung von Wurzelzement sowie bindegewebigem Attachement erhöht wird und eine echte parodontale Regeneration stattfindet [Shirakata et al., 2021].
Die alleinige Anwendung einer kreuzvernetzten HyA (xHya) in Kombination mit einem koronalen Verschiebelappen erhöhte signifikant den Anteil der vollständigen Wurzeldeckung (80 Prozent vs. 33,3 Prozent), der mittleren Wurzeldeckung (94 Prozent vs. 73 Prozent) sowie reduzierte die Schwellung und Morbidität innerhalb der ersten Woche post-OP [Pilloni et al., 2019]. Zu einem ähnlichen Ergebnis kam eine Fallserie zur Anwendung von xHyA im Rahmen der Tunneltechnik plus BGT mit einer mittleren Wurzeldeckung von 96 Prozent bei RT1- beziehungsweise RT2-Defekten [Guldener et al., 2020]. HyA scheint zusätzlich einen gewissen Effekt auf den Abbau von Kollagenmembranen zu haben [Eliezer et al., 2019], was sich positiv auf den Abbau und die Langzeitstabilität von Weichgewebsersatzmaterialien auswirken könnte. Für die zusätzliche Anwendung von HyA bei der Entnahme eines BGT sprechen das signifikant verminderte Schmerzempfinden sowie die beschleunigte Epithelisierung der Wunde [Yildirim et al., 2018].
Schmelz-Matrix-Proteine
Schmelz-Matrix-Proteine (SMP) haben sich als effektive Mittel zur Förderung der parodontalen Geweberegeneration in den vergangenen 30 Jahren etabliert. SMP bestehen hauptsächlich aus Amelogeninen, Proteinen, die eine entscheidende Rolle bei der Zahnwurzelentwicklung spielen. Die Proteine in SMP fördern die Zellproliferation, -migration und -adhäsion, was zu einer verbesserten Regeneration von parodontalen Strukturen führt [Miron et al., 2016]. Wie oben beschrieben stellt die Kombination aus koronalem Verschiebelappen und SMPs eine wissenschaftlich sehr gut dokumentierte Option zur Deckung freiliegender Wurzeloberflächen dar und wurde in vielen Übersichtsarbeiten als beste Alternative hinter dem Goldstandard BGT beschrieben, vor allem wenn ausreichend befestigte Gingiva vorhanden ist und somit zumindest ein mittlerer Phänotyp vorliegt [Chambrone et al., 2022]. Außerdem wurden präklinisch neben einem Gewinn an Gewebedicke [Al-Hezaimi et al., 2012] auch ein schnellerer Wundverschluss [Villa et al., 2015] sowie eine gesteigerte Neovaskularisierung und Kollagenfaserbildung beschrieben [Maymon-Gil et al., 2016].
Eigenblutzentrifugate
Einen weiteren Trend der vergangenen Jahre – primär in der Implantattherapie, weniger in der Parodontologie – stellen die Eigenblutzentrifugate wie exemplarisch das Platelet-rich Fibrin (PRF) dar. Die frühe Wundheilung des Weichgewebes wird wie bei HyA und SMP beschleunigt und unterstützt. Im Vergleich zu HyA oder SMP besteht hier ein klinisch (venöse Blutentnahme) sowie instrumentell (Anschaffung Equipment) höherer Aufwand. Die Anwendung von PRF mit einem koronalen Verschiebelappen wurde nur als Option der dritten Wahl im Vergleich zum Goldstandard BGT beschrieben [Chambrone et al., 2022] und ist auch in Kombination mit der Tunneltechnik dem BGT signifikant unterlegen [Carrera et al., 2023].
Konklusion III
Vor allem HyA – hier vor allem die kreuzvernetzte HyA – und SMPs haben sich als wertvolle Additiva in der plastischen Parodontalchirurgie etabliert. Ihre Anwendung ermöglicht eine verbesserte Wundheilung und eine echte Geweberegeneration, was zu besseren klinischen Ergebnissen und zu einer höheren Patientenzufriedenheit führt. Die Kombination dieser beiden Substanzen – vor allem mit aktuellen oder zukünftigen Gewebeersatzmaterialien – könnte die Erfolgsrate mit Blick auf eine komplette Wurzeldeckung, aber auch die Volumenstabilität weiter steigern. Synergistische Effekte wären denkbar und wurden in vitro gezeigt, sind aber noch klinisch zu beweisen.
PD Dr. Kai Fischer
Fachpraxis für Parodontologie & Implantologie
Franz-Ludwig-Str. 9A, 97072 Würzburg
und
Division für Parodontologie & Periimplantäre Erkrankung, Poliklinik für Zahnerhaltung & Präventivzahnmedizin, Zentrum für Zahnmedizin, Universität Zürich
Plattenstr. 11, 8032 Zürich, Schweiz
info@fachpraxis-parodontologie.de
2009: Staatsexamen & Approbation
2010–2012: Wissenschaftlicher Mitarbeiter in der Abteilung für Parodontologie, Universität Würzburg
2011: Promotion
2013: Ernennung zum Spezialisten für Parodontologie (DG PARO)
2013–2014: Honorary Research Associate & Clinical Teaching Fellow, UCL Eastman Dental Institute, London, UK
2014–2016: Oberarzt, Abteilung für Parodontologie, Universität Witten-Herdecke
2017: Ernennung zum Fachzahnarzt für Parodontologie (ZÄKWL)
2018: Ext. Oberarzt, Abteilung für Parodontologie & Periimplantäre Erkrankungen, Universität Zürich
2022: Habilitation
2024: Gründung „Fachpraxis für Parodontologie & Implantologie“, Würzburg
Literaturliste
Al-Hezaimi K, Al-Fahad H, O'Neill R, Shuman L, Griffin T. 2012. The effect of enamel matrix protein on gingival tissue thickness in vivo. Odontology. 100(1):61-66.
Aroca S, Molnar B, Windisch P, Gera I, Salvi GE, Nikolidakis D, Sculean A. 2013. Treatment of multiple adjacent miller class i and ii gingival recessions with a modified coronally advanced tunnel (mcat) technique and a collagen matrix or palatal connective tissue graft: A randomized, controlled clinical trial. J Clin Periodontol. 40(7):713-720.
Barootchi S, Rodriguez MV, Chan HL, Kripfgans OD, Wang HL, Tavelli L. 2023. Coronally advanced flap with xenogeneic collagen matrix for the treatment of gingival recessions at sites presenting with cervical restorations or noncarious cervical lesions: A clinical and ultrasonographic study. Int J Periodontics Restorative Dent. 43(2):146-154.
Batista EL, Jr., Batista FC, Novaes AB, Jr. 2001. Management of soft tissue ridge deformities with acellular dermal matrix. Clinical approach and outcome after 6 months of treatment. J Periodontol. 72(2):265-273.
Bertl K, Pifl M, Hirtler L, Rendl B, Nurnberger S, Stavropoulos A, Ulm C. 2015. Relative composition of fibrous connective and fatty/glandular tissue in connective tissue grafts depends on the harvesting technique but not the donor site of the hard palate. J Periodontol. 86(12):1331-1339.
Chambrone L, Botelho J, Machado V, Mascarenhas P, Mendes JJ, Avila-Ortiz G. 2022. Does the subepithelial connective tissue graft in conjunction with a coronally advanced flap remain as the gold standard therapy for the treatment of single gingival recession defects? A systematic review and network meta-analysis. J Periodontol. 93(9):1336-1352.
Couso-Queiruga E, Gonzalez-Martin O, Stuhr S, Gamborena I, Chambrone L, Avila-Ortiz G. 2023. Comparative histological evaluation of intra- and extraorally de-epithelialized connective tissue graft samples harvested from the posterior palate region. J Periodontol. 94(5):652-660.
Del Pizzo M, Modica F, Bethaz N, Priotto P, Romagnoli R. 2002. The connective tissue graft: A comparative clinical evaluation of wound healing at the palatal donor site. A preliminary study. J Clin Periodontol. 29(9):848-854.
Eliezer M, Sculean A, Miron RJ, Nemcovsky C, Weinberg E, Weinreb M, Zoabi H, Bosshardt DD, Fujioka-Kobayashi M, Moses O. 2019. Hyaluronic acid slows down collagen membrane degradation in uncontrolled diabetic rats. Journal of periodontal research. 54(6):644-652.
Fickl S, Fischer KR, Jockel-Schneider Y, Stappert CF, Schlagenhauf U, Kebschull M. 2014. Early wound healing and patient morbidity after single-incision vs. Trap-door graft harvesting from the palate--a clinical study. Clinical oral investigations. 18(9):2213-2219.
Fischer KR, Fickl S, Mardas N, Bozec L, Donos N. 2014. Stage-two surgery using collagen soft tissue grafts: Clinical cases and ultrastructural analysis. Quintessence Int. 45(10):853-860.
Fischer KR, Testori T, Wachtel H, Muhlemann S, Happe A, Del Fabbro M. 2019. Soft tissue augmentation applying a collagenated porcine dermal matrix during second stage surgery: A prospective multicenter case series. Clin Implant Dent Relat Res. 21(5):923-930.
Gluckman H, Du Toit J, Pontes CC, Hille J. 2019. Hyperplastic response following soft tissue augmentation in the esthetic zone. Clin Adv Periodontics. 9(2):50-54.
Griffin TJ, Cheung WS, Zavras AI, Damoulis PD. 2006. Postoperative complications following gingival augmentation procedures. J Periodontol. 77(12):2070-2079.
Guldener K, Lanzrein C, Eliezer M, Katsaros C, Stahli A, Sculean A. 2020. Treatment of single mandibular recessions with the modified coronally advanced tunnel or laterally closed tunnel, hyaluronic acid, and subepithelial connective tissue graft: A report of 12 cases. Quintessence Int. 51(6):456-463.
Halim FC, Sulijaya B. 2024. Allogenic acellular dermal matrix and xenogeneic dermal matrix as connective tissue graft substitutes for long-term stability gingival recession therapy: A systematic review and meta-analysis. Eur J Dent. 18(2):430-440.
Maymon-Gil T, Weinberg E, Nemcovsky C, Weinreb M. 2016. Enamel matrix derivative promotes healing of a surgical wound in the rat oral mucosa. J Periodontol. 87(5):601-609.
Miron RJ, Sculean A, Cochran DL, Froum S, Zucchelli G, Nemcovsky C, Donos N, Lyngstadaas SP, Deschner J, Dard M et al. 2016. Twenty years of enamel matrix derivative: The past, the present and the future. J Clin Periodontol. 43(8):668-683.
Mueller A, Fujioka-Kobayashi M, Mueller HD, Lussi A, Sculean A, Schmidlin PR, Miron RJ. 2017. Effect of hyaluronic acid on morphological changes to dentin surfaces and subsequent effect on periodontal ligament cell survival, attachment, and spreading. Clinical oral investigations. 21(4):1013-1019.
Pilloni A, Schmidlin PR, Sahrmann P, Sculean A, Rojas MA. 2019. Effectiveness of adjunctive hyaluronic acid application in coronally advanced flap in miller class i single gingival recession sites: A randomized controlled clinical trial. Clinical oral investigations. 23(3):1133-1141.
Puisys A, Auzbikaviciute V, Vindasiute-Narbute E, Zukauskas S, Razukevicus D, Dard MM. 2021. Full versus partial thickness flap to determine differentiation and over keratinization of non-keratinized mucosa. A 3-year split mouth randomized pilot study. Clin Exp Dent Res. 7(6):1061-1068.
Puisys A, Vindasiute E, Linkevciene L, Linkevicius T. 2015. The use of acellular dermal matrix membrane for vertical soft tissue augmentation during submerged implant placement: A case series. Clin Oral Implants Res. 26(4):465-470.
Ragghianti-Zangrando MS, Margarido Brondino NC, Damante CA, de Fatima Balderrama I, Veronesi GF, Cardoso MV, Campos Passanezi Sant'Ana A. 2021. Clinical outcomes and gingival blood flowmetry of two types of subepithelial connective tissue graft for root coverage in multiple gingival recessions: A preliminary study. Int J Periodontics Restorative Dent. 41(2):285-293.
Shirakata Y, Nakamura T, Kawakami Y, Imafuji T, Shinohara Y, Noguchi K, Sculean A. 2021. Healing of buccal gingival recessions following treatment with coronally advanced flap alone or combined with a cross-linked hyaluronic acid gel. An experimental study in dogs. J Clin Periodontol. 48(4):570-580.
Tavelli L, Barootchi S, Avila-Ortiz G, Urban IA, Giannobile WV, Wang HL. 2021. Peri-implant soft tissue phenotype modification and its impact on peri-implant health: A systematic review and network meta-analysis. J Periodontol. 92(1):21-44.
Tavelli L, Barootchi S, Greenwell H, Wang HL. 2019a. Is a soft tissue graft harvested from the maxillary tuberosity the approach of choice in an isolated site? J Periodontol. 90(8):821-825.
Tavelli L, Ravida A, Saleh MHA, Maska B, Del Amo FS, Rasperini G, Wang HL. 2019b. Pain perception following epithelialized gingival graft harvesting: A randomized clinical trial. Clinical oral investigations. 23(1):459-468.
Thoma DS, Jung RE, Schneider D, Cochran DL, Ender A, Jones AA, Gorlach C, Uebersax L, Graf-Hausner U, Hammerle CH. 2010. Soft tissue volume augmentation by the use of collagen-based matrices: A volumetric analysis. J Clin Periodontol. 37(7):659-666.
Villa O, Wohlfahrt JC, Mdla I, Petzold C, Reseland JE, Snead ML, Lyngstadaas SP. 2015. Proline-rich peptide mimics effects of enamel matrix derivative on rat oral mucosa incisional wound healing. J Periodontol. 86(12):1386-1395.
Yildirim S, Ozener HO, Dogan B, Kuru B. 2018. Effect of topically applied hyaluronic acid on pain and palatal epithelial wound healing: An examiner-masked, randomized, controlled clinical trial. J Periodontol. 89(1):36-45.
Zucchelli G, Felice P, Mazzotti C, Marzadori M, Mounssif I, Monaco C, Stefanini M. 2018. 5-year outcomes after coverage of soft tissue dehiscence around single implants: A prospective cohort study. Eur J Oral Implantol. 11(2):215-224.
Zucchelli G, Mele M, Stefanini M, Mazzotti C, Marzadori M, Montebugnoli L, de Sanctis M. 2010. Patient morbidity and root coverage outcome after subepithelial connective tissue and de-epithelialized grafts: A comparative randomized-controlled clinical trial. J Clin Periodontol. 37(8):728-738.
Zucchelli G, Mounssif I, Mazzotti C, Montebugnoli L, Sangiorgi M, Mele M, Stefanini M. 2014a. Does the dimension of the graft influence patient morbidity and root coverage outcomes? A randomized controlled clinical trial. J Clin Periodontol. 41(7):708-716.
Zucchelli G, Mounssif I, Mazzotti C, Stefanini M, Marzadori M, Petracci E, Montebugnoli L. 2014b. Coronally advanced flap with and without connective tissue graft for the treatment of multiple gingival recessions: A comparative short- and long-term controlled randomized clinical trial. J Clin Periodontol. 41(4):396-403.