MIH – alter Wein in neuen Schläuchen?
Anomalien der Zahnhartsubstanzen, die bereits beim Zahndurchbruch in Erscheinung treten, entstehen durch Störungen bei der Bildung von Schmelz und Dentin. Genetisch bedingte strukturelle Anomalien werden Dysplasien genannt. Diejenigen Strukturanomalien, die nicht genetisch bedingt sind, heißen Hypoplasien. Wenn die (Zahn-)Schmelzproduktion in bestimmten Bereichen ganz ausbleibt, spricht man von einer Aplasie. Schließlich sind nichthypoplastische Zahnverfärbungen zu differenzieren, die beispielsweise durch bestimmte Medikamenteneinnahmen (zum Beispiel Tetrazykline) während der Schmelzbildung hervorgerufen werden können. Schmelzhypoplasien entstehen durch Trauma oder metabolische Störungen der Ameloblasten. Ihre Lokalisation entspricht dem Zeitpunkt der Störung in der präeruptiven Zahnentwicklung: Bei lokaler Ursache finden sich die Hypoplasien an Einzelzähnen; bei systemischer Einwirkung entstehen sie symmetrisch an allen Zähnen, die zur gegebenen Zeit mineralisiert wurden.
Seit einiger Zeit macht der Begriff der MIH (Molaren-Inzisivi-Hypomineralisation) auf sich aufmerksam, so dass man den Eindruck gewinnen könnte, es handele sich hier um ein neues Erkrankungsbild in der Zahnmedizin. Ausgehend von einem Workshop im Jahr 2003 der European Academy of Paediatric Dentistry (EADP) wurde der Begriff Hypomineralisation von Weerheijm vorgeschlagen, auch wenn sie selbst konstatierte, dass dieser Begriff möglicherweise nur temporär zu verwenden sei, bis es einen terminologischen Konsens gäbe. Zwar handelt es sich bei der MIH um eine Mindermineralisation des Schmelzes, oft existieren jedoch auch Bildungsstörungen (Hypoplasien) oder gar Bildungsausfälle (Aplasien) der prismatischen Schmelzstruktur. Die MIH ist demnach Teil der nicht genetischen, entwicklungsbedingten Strukturanomalien.
Den entwicklungsbedingten Zahnhartsubstanzstörungen wurde über einen sehr langen Zeitraum nur wenig Aufmerksamkeit geschenkt; erst seit etwa einer Dekade wird verstärkt darüber berichtet – zuletzt sogar in der allgemeinen Presse. Dies wurde nicht zuletzt dadurch möglich, dass mit der Fünften Deutschen Mundgesundheitsstudie (DMS V) erstmalig bevölkerungsweite Daten hierzu für Deutschland vorgelegt wurden. Demnach weisen 28,7 Prozent der zwölfjährigen Kinder in Deutschland mindestens einen Zahn mit einer Hypoplasie/MIH auf. Die Prävalenz erscheint enorm – es verwundert daher nicht, dass sich die Medien förmlich darauf stürzten. Was dabei kaum berichtet wurde, ist, dass die allgemeine Erkrankungsschwere (severity) überwiegend gering ausgeprägt ist, lediglich 5,4 Prozent der Kinder weisen mehr als eine begrenzte Opazität auf. Opazitäten haben klinisch jedoch jenseits kosmetischer Aspekte oft keine Bedeutung, wenn sie nicht mit weiteren Symptomen assoziiert sind. Insofern ist es doch unter anderem das Verdienst Weerheijms, dass die verstärkte Aufmerksamkeit auf dieses Thema auch die Forschung inspiriert und die zahnärztliche Aus- und Fortbildung zu Diagnostik und Therapie von Hypomineralisationen und Hypoplasien nach vorne gebracht hat.
Ätiologie und Pathogenese
Für Pierre Fauchard [1728] beruhten die „Flecken, die weisser sind als die Substantz von dem Schmeltzwerke der Zähne selbst, und bis in die Holigkeit des Cörpers vom Zahne hinein dringen“ auf äußerlichen Ursachen. Ebenso beschrieb er in „Observationen von ungestalten [...] Zähnen“ eine hypoplastische Amelogenesis imperfecta als Erkrankung aller Zähne durch fehlende Mundhygiene mit „Schlamm und Theilgen von Speisen“ bei einem etwa 14-Jährigen.
G. V. Black [1908] beginnt die „Pathologie der harten Zahngewebe“ im ersten Band der Konservierenden Zahnheilkunde mit einem umfassenden Kapitel zur „Atrophie der Zähne“: Diese „bezeichnet eine partielle Entwicklungshemmung infolge einer Ernährungsstörung. [...] Die an mehreren Zähnen betroffenen Partien sind immer jene, die in einem gegebenen Zeitpunkt bei der betreffenden Person eben in Bildung begriffen waren.“ Das ist die bis heute gültige Ätiologieauffassung, umso mehr, als Black hinzufügt, „daß es keine spezielle Krankheit gibt, die für diese Mißbildung verantwortlich gemacht werden kann, und daß vielmehr jede Krankheit, welche die [zelluläre, Ergänzung der Autoren] Ernährung ernstlich beeinträchtigt, diese Folgen hervorzurufen imstande ist.“
Kronfeld und Schour [1939] prägten den Begriff der neonatalen dentalen Hypoplasie, gefolgt von den Untersuchungen von Sarnat und Schour [1941, 1942] zur Schmelz-Hypoplasie und Aplasie in Verbindung mit systemischen frühkindlichen Erkrankungen. Ein entscheidender Durchbruch war schließlich die Zusammenfassung der Entwicklung der menschlichen Dentition von Schour und Massler [1940, 1941] in klassisch gewordenen schematischen Abbildungen der beginnenden Mineralisation, der Wurzelentwicklung, der Exfoliation der Milchzähne und der Abschlussentwicklung der Kronen und Wurzeln der bleibenden Zähne in – pars pro toto – jeweils einem Quadranten (Abbildungen 4 und 5).
Weerheijm et al. [2001] schlugen mit der Molaren-Inzisiven-Hypomineralisation (MIH) einen neuen Namen vor, der die komplexe zellulär über die Ameloblasten und Odontoblasten gesteuerte Hypoplasie und Aplasie nur bedingt berücksichtigte und unglücklicherweise auf die bisher unbekannte Ätiologie abstellte. Dies trifft jedoch nur bedingt zu: Während der zeitgleichen Zelldifferenzierung der Ameloblasten aus dem inneren Schmelzepithel und der Odontoblasten aus den Mesenchymzellen haben diese Zellen zum Beginn der Sekretion der Dentinmatrix und der darauf folgenden Sekretion der Schmelzmatrix bis zum Abschluss einen hohen Energiebedarf. In Inzisivus- und Molaren-Organ-Kulturen von Mäusen konnten Ida-Yonemochi et al. [2016, 2020] zeigen, dass der Glucose-Metabolismus einer der kritischen Faktoren der Regulierung der Amelogenese ist. Die Inhibition von zellulären Glucose-Transportern und Ionen-Kanälen führt zur Störung der Schmelz- und Dentin-Matrix-Bildung und zusätzlich zu Invaginations-Veränderungen im Glockenstadium des Zahnkeims und damit zu Veränderungen der Form des Schmelzmantels. Der Zellstoffwechsel während der Zahnentwicklung ist abhängig vom systemischen Metabolismus des Makroorganismus, und der ist insbesondere perinatal durch Hypoxie bei verzögertem Geburtsvorgang und bei allen frühkindlichen Infekten und metabolischen Störungen bis zum dritten Lebensjahr besonders anfällig. Jeder frühkindliche Infekt und jede metabolische Störung kann je nach der individuellen Reaktion des Organismus zu Hypomineralisationen, Hypoplasien und Aplasien der bleibenden Zähne von den Frontzähnen, ersten Molaren, Eckzähnen bis zu den Prämolaren führen.
Störungen des Glucose-Metabolismus können auch am gesamten Skelett die komplexe Biomineralisation mit Hydroxylapatit beeinträchtigen. Durch den permanenten knöchernen Umbau verschwinden diese temporären Entwicklungsstörungen jedoch wieder. Nur bei der definitiven Schmelzentwicklung und lebenslangen Dentinentwicklung bleiben die präeruptiven, metabolisch ausgelösten Anomalien erhalten und werden klinisch Jahre später nach der Eruption erst am Schmelz sichtbar. Wenn keine Schmelzaplasie stattgefunden hatte, bleiben Hypoplasien des Dentins lebenslang verborgen.
Pathogenetisch erscheint hypomineralisierter oder hypoplastischer Schmelz in Abhängigkeit vom Zeitpunkt und der Intensität der metabolischen Störung als weiß-opaker Fleck infolge einer Prismenstrukturänderung des vollständig transparenten Schmelzes, als Einziehungen mit Grübchen und Streifen bei Verlust der Matrixbildung im äußeren Schmelzmantel, als freiliegendes hypoplastisches Dentin bei vollständigem Verlust der Schmelz-Matrix-Bildung in unterschiedlicher Ausdehnung von kleinen Arealen an den Glatt- oder Kauflächen bis zum Totalverlust des Schmelzmantels im oberen Drittel der Krone. Die Aplasie des Schmelzes führt durch Invaginationstörungen zu abgerundeten Schmelzrändern. Hypoplastisches verfärbtes Dentin kann den Schmelzmantel ungenügend unterstützen, dann entstehen an den Rändern Abbrüche. Symmetrische Anomalien an bleibenden Zähnen zeigen häufig mehrere pathogenetische Muster vom weißen Fleck bis zur Aplasie. Die ursächliche metabolische Störung kann einmalig kurz oder länger sowie auch wiederholt und mehrfach auftreten. Der Entstehungsmechanismus beeinflusst das vielfältige klinische Bild.
Klinische hypoplastische Anomalieformen
Das makroskopische Bild umfasst die Ausdehnung an einem Zahn, die Zahl der betroffenen Zähne und fünf Formen der Anomalie mit:
opaken weißlichen Flecken
pigmentierten gelblich-bräunlichen Flecken
horizontalen Grübchen und Linien
Höcker- und Inzisalkanten-Verlust
aplastischen Arealen mit freiliegendem, hypoplastisch-verfärbtem Dentin und abgerundeten Schmelzrändern (Invaginationsstörung im Glockenstadium) oder Schmelzabbrüchen.
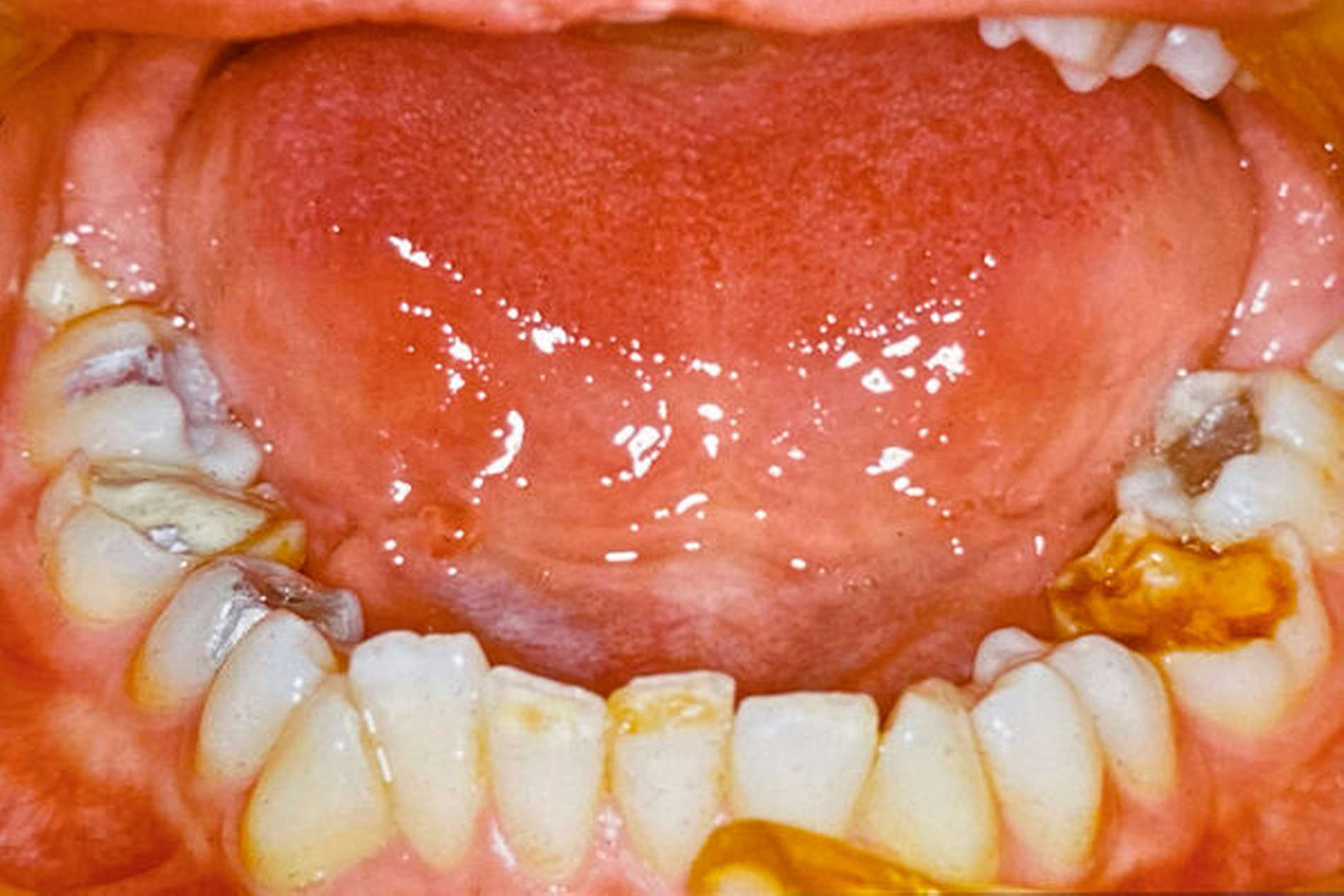
Die klinischen Bilder meist komplexer Anomalien sind in den Abbildungen 1 bis 3, 6 und 7 dokumentiert. Die Verteilung der Anomalien der Zahnhartgewebe in einem zufällig ausgewählten, aber trotzdem repräsentativen Patientengut einer Universitätszahnklinik ist in den Tabellen 1 und 2 dokumentiert.
Anamnese
Mit den Schour-Massler-Grafiken (Abbildungen 4 und 5) wird bei Hypomineralisation oder Hypoplasien an den Höckern der ersten Molaren nach Gesundheitsstörungen in der Perinatalperiode gefragt, bei Veränderungen im oberen Kronendrittel nach Erkrankungen im neunten bis zwölften Lebensmonat, was auch auf Hypomineralisation oder Hypoplasien der Inzisalkanten zutrifft. Bei Anomalien im mittleren Kronendrittel vom 18. bis zum 24. Lebensmonat (und inzisales Drittel der Kronen), bei zahnhalsnahen Anomalien der Molaren fragt man nach Erkrankungen vom zweiten bis zum vierten Lebensjahr (Tabelle 3). Anomalien, die nach dem fünften bis zum zwölften Lebensjahr ausgelöst werden, sind sehr selten, weil metabolische Gesundheitsstörungen mit einem Einfluss auf den Glucose-Metabolismus der Ameloblasten und Odontoblasten in diesem Zeitraum kaum noch auftreten.
Gefragt werden Anomalieträger und/oder Begleitpersonen ab dem sechsten Lebensjahr mit dem Durchbruch der ersten Molaren. Von Bedeutung sind die Geburtsumstände (Hypoxie, Asphyxie), alle Infektionskrankheiten einschließlich Säuglingsdyspepsie, Flüssigkeitsverlust, Rachitis, kongenitale Hypothyreose und Hypoparathyreoidismus. Die Frage der Kinder, Eltern, Großeltern (ob Anomalieträger oder Fürsorgeperson), ob und an welchen Zähnen nach späterem Zahndurchbruch die gleichen Veränderungen auftreten, kann man in der Regel kompetent nach einem Blick auf die Schour-Massler-Zeittafel beantworten, wenn sich anamnestisch kein weiterer Hinweis auf eine weitere Störung zu einem anderen Zeitpunkt der Schmelzbildung ergibt.
Klassifikation
Es gibt viele Klassifikationen, zum Beispiel den Developmental Dental Index DDE [1982, 1992], die Klassifikationen von Murray und Shaw [1979] oder von Kamann und Gängler [1999] sowie den MIH Treatment Need Index (MIH TNI). Sie haben eine Bedeutung für klinische, epidemiologische, mikromorphologische und molekularbiologische Studien; der MIH-TNI versucht auch, Diagnostik und Behandlung miteinander zu verknüpfen. Für die zahnärztliche Praxis sind jedoch das klinische Erscheinungsbild sowie die Ergebnisse der Anamnese wichtig; für eine gute Dokumentation sind intraorale Fotografien empfehlenswert.
Abgrenzung von anderen Hypoplasien und initialer Karies
Bei apikaler Parodontitis an Milchzähnen beeinflusst die Entzündung das Schmelzorgan des Ersatzzahnes. Diese bleibenden Turner-Zähne finden sich meist an Prämolaren, seltener an Frontzähnen. Sie zeigen die typischen Zeichen einer Hypoplasie und Aplasie, treten jedoch nicht symmetrisch auf.
Die Milchzahnintrusion bis zum vierten Lebensjahr schädigt die Ersatzzähne mit labial weißen Flecken, bei einem Hämatom können sie durch den Erythrozyten-Abbau gelblich-bräunlich pigmentiert sein. Bei schweren Traumata folgt eine Dilazeration mit Abknickung des Kronen- und des nachfolgenden Wurzelanteils.
Von klinischer Bedeutung sind Virusinfektionen im ersten Drittel der Schwangerschaft. Zum Rubella-Syndrom bei Röteln der Mutter zählen Schmelz-Hypoplasien kombiniert mit Hypodontie und Formanomalien. Wahrscheinlich haben auch andere Infektionen mit Influenzaviren, Coronaviren, Morbilliviren (Masern), Poliomyelitisviren und Varizellaviren (Windpocken) teratogene Schädigungen zur Folge, wozu Schmelz- und Dentin-Hypoplasien gehören könnten. Bei konnataler Lues liegt eine Infektion mit Treponema pallidum nach dem zweiten Schwangerschaftsdrittel vor. An den Inzisivi und ersten Molaren entwickeln sich typische Invaginationsstörungen im Glockenstadium, die zu tonnenförmigen Frontzähnen mit inzisalen Einbuchtungen als Hutchinson-Zähne und an den Molaren zu maulbeerförmigen Einschnürungen als Pflüger-Molaren führen. Ob SARS CoV-2-Infektionen im ersten oder zweiten Schwangerschaftsdrittel zu ähnlichen Symptomen führen, wird sich ab 2026 zeigen.
Intoxikationen mit Spurenelementen betreffen ausschließlich alimentäre oder medikamentöse Überdosierungen in der kindlichen Entwicklung durch Strontium (selten) oder Fluorid (häufiger). Bei einem Strontiumgehalt des Trinkwassers ab 0,2 bis 34,0 mg/l zeigt sich eine Korrelation zur Zunahme von linienförmigen Schmelz-Hypoplasien auch dann, wenn eine Fluorose ausgeschlossen werden kann.
Die Fluorose der Zähne entwickelt sich als milde Form mit opaken Linien entlang der Perikymatien oder mit opaken Flecken ab 0,25 mg Fluorid-Supplementierung/Tag im ersten Lebensjahr oder ab 1,0 mg/l Fluorid im Trinkwasser vom ersten bis etwa zum sechsten Lebensjahr. Die Fluoridwirkung beruht auf einer Störung der Schmelzmatrix-Bildung und -Reifung mit einer erhöhten Porosität von über 15 Prozent (gegenüber gesundem Schmelz mit 0,1 Prozent ), die dazu führt, dass der poröse Schmelz nach der Eruption wie ausgestanzt mechanisch degradiert wird. Diese scharfen Demarkierungen sind differenzialdiagnostisch von den runden Schmelzübergängen bei metabolischen Aplasien eindeutig abgrenzbar.
Die etablierte initiale Karies der Zähne führt mit dem porösen Körper der Läsion auch zu opak-weißen Flecken, deren Entstehung jedoch völlig verschieden von der metabolisch bedingten Schmelz-Hypoplasie ist. Deren optische Erscheinung ist klinisch leicht unterschiedlich; kariöse Läsionen sind oft weniger scharf begrenzt und selten so deutlich opak wie Bildungsstörungen. Zudem unterscheiden sich die Lokalisationen: Hypoplasien manifestieren sich fast immer an Höckerspitzen und nahe der Inzisalkante, seltener (bei spät entstandenen Störungen) zahnhalsnah. Der hypoplastische Fleck folgt in seiner Ausdehnung zudem den koronalen Entwicklungslinien. Die initiale Karies beginnt fast immer an Fissuren und Approximalflächen, seltener entlang des Gingivarandes, dabei folgt sie streng der gingivanahen Plaqueausdehnung. Mit dieser Unterscheidung lassen sich Hypoplasien und kariöse Läsionen in der Regel gut voneinander abgrenzen.
Epidemiologie
Für den behandelnden Zahnarzt ist es relevant zu wissen, wie oft eine Erkrankung vorliegt (Prävalenz) und wie viele neue Fälle es jedes Jahr gibt (Inzidenz): Diese Information erlaubt es ihm abzuschätzen, wie wahrscheinlich ein bestimmter Patient unter einer bestimmten Erkrankung leidet und welche Diagnostik- und Therapiemaßnahmen für diesen Patienten optimal sind. Andere Entscheidungsträger (Gesundheits- und Wissenschaftspolitiker, Hochschullehrer) sollten ebenfalls epidemiologische Kennziffern zur Hand haben, um beispielsweise Präventions- und Therapieprogramme zu priorisieren oder Lehrpläne entwickeln zu können, die die Häufigkeit und den Schweregrad von Erkrankungen angemessen berücksichtigen.
Die berichtete Prävalenz von Hypoplasien beziehungsweise – spezifischer – MIH variiert von Studie zu Studie erheblich, was vermutlich vor allem methodische Gründe hat: Verschiedene Stichproben wurden mit verschiedenen Erhebungsmethoden und Falldefinitionen (DDE, EAPD) untersucht, was eine Vergleichbarkeit zwischen den Studien erschwert. Eine kürzlich durchgeführte systematische Übersicht und Meta-Regressionsanalyse [Schwendicke et al., 2018, 2019] (Abbildung 8) hat beispielsweise die globale Prävalenz und Inzidenz von MIH geschätzt; hierbei wurden die Analysen innerhalb der räumlichen Einheiten der sogenannten „Global Burden of Disease (GBD) Studien“ durchgeführt. Bei den GBD-Studien werden Prävalenz, Inzidenz und die (auch durch den Schweregrad bestimmte) Krankheitslast (Burden) innerhalb von Superregionen und Regionen, die bestimmte sozioökonomische und geografische Ähnlichkeiten aufweisen, analysiert. Auch wurden Subgruppenanalysen nach Geschlecht (männlich versus weiblich) und MIH-Falldefinition (EAPD versus andere) durchgeführt. Weiterhin wurden Analysen des Behandlungsbedarfs (das heißt Patienten mit subjektiven Symptomen und/oder posteruptivem Schmelzeinbruch und Kavitation) vorgenommen.
Basierend auf einem Datensatz, der über 113.144 Teilnehmer aus 43 Ländern umfasste, wurde die durchschnittliche (95 Prozent Konfidenzintervall) globale Prävalenz mit 12,9 Prozent (11,7–14,3 Prozent) geschätzt, wobei signifikante Unterschiede zwischen Superregionen, Regionen und Ländern sichtbar wurden. Die geschätzte Zahl der MIH-Fälle wurde für 2016 mit 811 Millionen geschätzt. Die höchste Fallzahl wurde in Süd- und Ostasien und Nordamerika festgestellt; auf Länderebene trugen bevölkerungsreiche Länder wie Indien, China oder die Vereinigten Staaten erheblich zur Fallzahl bei. Die weltweite Zahl der neu Erkrankten wurde für 2016 auf 16,0 Millionen Menschen geschätzt; hierbei verzeichneten Länder in Südasien, Südostasien und im östlichen Afrika südlich der Sahara die höchsten Zahlen. Wachsende Länder wie Indien, die Vereinigten Staaten, China, Pakistan oder Indonesien rangierten bei der Zahl der neu Erkrankten ebenso weit vorn.
Prävalenz und Inzidenz unterschieden sich nicht signifikant zwischen weiblichen und männlichen Personen und auch räumliche, soziale, ökologische oder wirtschaftliche Faktoren waren nicht assoziiert mit der Prävalenz und Inzidenz. Hingegen wurden signifikante Unterschiede zwischen Studien, die die EAPD-Falldefinition verwendeten, und jenen, die eine andere Definition verwendeten, ausgemacht; dies liegt vermutlich daran, dass die EAPD-Falldefinition auch atypische Restaurationen und fehlende Zähne einschließt. Ungefähr 27,4 Prozent (23,5 – 31,7 Prozent) der MIH-Fälle (also jeder vierte Patient mit MIH, überschlagsweise also 12,9 Prozent * 27,4 Prozent = 3,5 Prozent) weisen Behandlungsbedarfe auf; diese Zahl deckt sich demnach mit der Größenordnung der in der DMS V als behandlungsbedürftig identifizierten Fälle. Weltweit leiden demnach über 200 Millionen Menschen an MIH und jedes Jahr kommen über vier Millionen neue Fälle hinzu.
Eine zeitliche Dynamik ist bisher aus diesen Daten nur schwer abzulesen (unter anderem wegen der methodischen Heterogenität); einen klaren Trend zu „mehr“ Hypomineralisationen oder Hypoplasien kann man nicht ausmachen. Gespannt wird demnach auf die Sechste Deutsche Mundgesundheitsstudie gewartet, bei der diese Erkrankungsformen bei Kindern erneut in den Blick genommen werden: Hier lassen sich dann auch im zeitlichen Verlauf zwischen 2014 (Erhebungszeitpunkt DMS V) und 2022 (Erhebungszeitpunkt DMS VI) robuste Aussagen zur Morbiditätsdynamik treffen.
Prof. Dr. Dr. h. c. Peter Gängler
ORMED, Institute for Oral Medicine at the University of Witten/Herdecke
Alfred-Herrhausen-Str. 45, 58455 Witten
peter.gaengler@uni-wh.de - mail
Prof. Dr. A. Rainer Jordan
Institut der Deutschen Zahnärzte (IDZ)
Universitätsstr. 73, 50931 Köln
Dr. Tomas Lang
ORMED, Institute for Oral Medicine at the University of Witten/Herdecke
Alfred-Herrhausen-Str. 45, 58455 Witten
Dr. Monika Kolski
Zahnärztliche Gemeinschaftspraxis Dres. M. Kolski & M. Kolski
Westerfilder Str. 6, 44357 Dortmund
Prof. Dr. Falk Schwendicke, MDPH
Leiter der Abteilung für Zahnärztliche Diagnostik, Digitale Zahnheilkunde und Versorgungsforschung
Centrum 3 für Zahn-, Mund- und Kieferheilkunde,
Charité – Universitätsmedizin Berlin
Aßmannshauser Str. 4–6, 14197 Berlin
Literaturliste
Des Herrn Pierre Fauchard Frantzösischer Zahn-Artzt oder Tractat von den Zähnen. Der Erste Theil. (S. 92 und S. 323 – 325), Joh. Andreas Rüdiger, Berlin 1733
Black GV. Konservierende Zahnheilkunde. Band I, Die Pathologie der harten Zahngewebe. Die Atrophie der Zähne (S. 6 – 46), Hermann Meusser, Berlin 1914
Kronfeld R, Schour I. Neonatal dental hypoplasia. J Am Dent Assoc 26 (1939), 18 – 32.
Sarnat BG, Schour I. Enamel hypoplasia (Chronologic enamel aplasia in relation to systemic disease). A chronologic, morphologic and etiologic classification. J Am Dent Assoc 28 (1941), 1989 – 2000; 29 (1942), 67 – 75.
Gängler P. Klinik der Konservierenden Stomatologie. Volk und Gesundheit, Berlin 1987; 2., überarb. Aufl. 1991
Gängler P, Hoffmann T, Willershausen B, Schwenzer N, Ehrenfeld M (Hrsg.). Konservierende Zahnheilkunde und Parodontologie. Thieme, Stuttgart – New York, 3. Aufl. 2010
Schour I, Massler M. Studies in tooth development. The growth patterns of human teeth.
J Am Dent Assoc 27 (1940), 1778 – 1793, 1918 – 1931.
Schour I, Massler M. The development of the human dentition. J Am Dent Assoc 28 (1941), 1153 – 1160
Schwendicke, F., Elhennawy, K., Reda, S., Bekes, K., Manton, D. J., & Krois, J. (2019). Corrigendum to „Global burden of molar incisor hypomineralization“ [J. Dent. 68C (2018) 10–18]. J Dent, 80, 89–92.
https://pubmed.ncbi.nlm.nih.gov/30554832/ - external-link-new-window
Kamann WK, Gängler P. Der Turner-Zahn – Wenn der Milchzahn Spuren hinterläßt. Zahnärztl Mitteil 89 (1999), 42-44
Weerheijm KL, Jälevik B, Alaluusua S. Molar-incisor-hypomineralisation. Caries Res 35 (2001),
390 – 391
Weerheijm KL, Mejàre I. Molar incisor hypomineralization: a questionnaire inventory of its occurrence in member countries of the European Academy of Paediatric Dentistry (EAPD).
Int J Paediatr Dent. 13 (2003), 411-416
Ida-Yonemochi H, Otsu K, Ohshima H, Harada H. The glycogen metabolism via Akt signaling is important for the secretion of enamel matrix in tooth development. Mech Dev 139 (2016), 18 - 30
Ida-Yonemochi H, Otsu K, Harada H, Ohshima H. Functional expression of sodium-dependent glucose transporter in amelogenesis. J Dent Res. 99 (2020), 977-986
https://journals.sagepub.com/doi/abs/10.1177/0022034520916130 - external-link-new-window



















