Aphthen – Update zu Diagnostik und Therapie
Aphthen treten als schmerzhafte Ulzerationen auf, die innerhalb von Wochen bis Monaten und Jahren rezidivieren [Kramer et al., 1980]. Sie können in der Mundhöhle, im Rachenraum, aber auch an anderen Stellen auftreten. Synonym werden sie in der Literatur auch als habituelle Aphthen, chronisch rezidivierende Aphthen, rezidivierende benigne Aphthosis, in der englischsprachigen Literatur als recurrent aphthous ulceration, recurrent oral ulceration, canker sore, aphthous ulcerations, recurrent aphthous stomatitis und aphtha bezeichnet.
Die Häufigkeit des Auftretens rezidivierender Aphthen liegt zwischen 5 und 60 Prozent [Majorana et al., 2010; Hornstein, 1998; Jurge et al., 2006]. Sie treten bei Frauen häufiger auf als bei Männern [Chattopadhyay et al., 2007], beginnen meist im zweiten oder im dritten Lebensjahrzent und kommen seltener bei alten Menschen vor [Reichart, 2000].
aphthöse Läsion | andere ulzeröse Läsionen |
|---|---|
meist oberflächliche entzündliche Erosion mit Fibrinbelag (Mikulicz).selten tiefer reichende Ulcera (Sutton) | exkavierter Gewebsdefekt. in der Regel echtes Ulcus. heterogeneUrsachen |
rasche Entstehung | Entstehung unterschiedlich rasch |
plan oder gering erhaben | Form und Tiefe sehr variabel |
geröteter Hof in Umgebung | variable Ulkusränder |
Dolenz: spontan und taktil | Dolenz variabel |
lokale Blutungsneigung gering | lokale Blutungsneigung erhöht |
Foetor ex ore negativ (außer M. Behçet. Synonym für M. Adamantiades-Behçet) | Foetor ex ore häufig |
regionale Lymphknoten meistohne pathologischen Befund | Lymphknoten häufig vergrößert und druckdolent (je nach Ursache) |
sehr hohe Rezidivneigung | Rezidive abhängig von Ursache |
Quelle: in Anlehnung an Scully et al.. 2008 |
Sie gehören zu den häufigsten Erkrankungen der Mund- und Rachenschleimhaut. Zudem besteht bei 30 bis 40 Prozent der Patienten eine familiäre Häufung rezidivierender Aphthen [Shohat-Zabarski et al., 1992]. Bei Kindern und Jugendlichen repräsentieren Aphthen die häufigste Läsion der Mundschleimhaut [Kleinman et al., 1994]. Die Ätiologie oropharyngealer Aphthen ist nach wie vor ungeklärt. Daher besteht weiterer Forschungsbedarf.
Als Differenzialdiagnosen zu Aphthen sind Malignome und deren Vorstufen, andere Stomatopathien, reaktive Veränderungen der Mund- und Rachenschleimhaut, gastrointestinale Syndrome, mukokutane Erkrankungen des rheumatischen Formenkreises, bullöse und lichenoide Dermatosen und Infektionskrankheiten zu berücksichtigen.
Morphologie und Klinik
In Übersicht 1 sind morphologische und klinische Kriterien zur Unterscheidung einer aphthösen Läsion von anderen ulzerösen Läsionen aufgeführt. Die rechtzeitige differenzialdiagnostische Abwägung ist wichtig, um präkanzeröse Vorläuferläsionen im Mund- und Rachenbereich zu erkennen – zur Prävention der Entstehung eines oropharyngealen Karzinoms, beziehungsweise um die Diagnose bereits im Frühstadium zu sichern, denn eine Therapieverzögerung von mehr als vier Wochen führt bei oropharyngealen Karzinomen zu einer signifikant schlechteren Überlebensrate [Allison et al., 1998; Kowalski et al., 2001], aber auch zur Notwendigkeit der Anwendung multimodaler und aggressiverer Therapiestrategien.
In der aktuellen S2k-Leitlinie „Diagnostik und Therapieoptionen von Aphthen und aphthoiden Läsionen der Mund- und Rachenschleimhaut“ [AWMF-Register-Nr. 007–101; Jackowski et al., 2017] werden diese Zusammenhänge besonders herausgestellt. Daher sei in diesem Kontext auf die besondere Bedeutung und enge differenzial diagnostische Beziehung zur S2k-Leitlinie „Diagnostik und Management von Vorläuferläsionen des oralen Plattenephitelkarzinoms in der Zahn-, Mund- und Kieferheilkunde“ [AWMF-Register-Nr. 007–092; Kunkel et al., 2010] und zur S2k-Leitlinie „Diagnostik und Therapie des Pemphigus vulgaris / foliaceus und des bullösen Pemphigoids“ [AWMF-Register-Nr. 013–071; Nast et al., 2014; Schmidt et al., 2015; Altenburg et al., 2014] hingewiesen.
Übersicht 2 stellt die klinisch-morphologischen Erscheinungsformen der rekurrierenden Aphthose zusammen: Die Phasen der oralen und pharyngealen Aphthose sind gekennzeichnet durch ein bis zu 24-stündiges Prodromalstadium mit Kribbeln, Spannungsgefühl, Brennen, Rauigkeit, an das sich eine bis zu drei Tage dauernde präulzeröse Phase mit einem inflammatorischen Erythem beziehungsweise dem Auftreten einer indurierten Papel anschließt. Das darauf folgende ein bis 16 Tage dauernde ulzerative Stadium ist durch die typische fibrinbelegte Ulzeration mit aufgeworfenem Rand gekennzeichnet. Die sich daran anschließende Abheilungsphase kann vier bis 30 Tage andauern.
Aphthen als Symptom
Aphthoide Erosionen beziehungsweise Ulzerationen der oropharyngealen Mukosa können im Zusammenhang mit vielen Erkrankungen auftreten. Anamnese, klinische Symptomatik, Krankheitsverlauf, Alter und Lebensgewohnheiten des Patienten sowie morphologische Kriterien sind bei der Diagnosefindung zu berücksichtigen.
1. Typus minor (Mikulicz): | |
|---|---|
– oberflächlich | |
– Mundhöhle. meist nichtkeratinisierte Mukosa | |
– eine bis vier Aphthen gleichzeitig | |
– meist 2–5 mm. < 10 mm Durchmesser | |
– sieben bis zehn Tage Präsenz | |
– drei bis fünf Tage schmerzhaft | |
– narbenfreie Abheilung | |
– drei- bis sechsmal/Jahr | |
– ca. 85 % aller rekurrierenden Aphthen | |
– 10–15 % der Bevölkerung | |
2. Typus maior (Sutton): | |
– tiefere Lage (Penetration bis in Speicheldrüsen/Muskelschichten) | |
– Induration. Ulzeration. Gewebsdestruktion | |
– Mundhöhle. Oropharynx. selten Genitalschleimhaut (Vulva) | |
– ≥ 10 mm. bis 30 mm | |
– zwei bis vier Wochen Präsenz | |
– sehr schmerzhaft. Lymphadenopathie | |
– mundgesundheitsbezogene Lebensqualität sehr eingeschränkt | |
– narbige Abheilung | |
– aufeinanderfolgend oder kontinuierlich | |
– ca. 10 % aller rekurrierenden Aphthen | |
3. Typus herpetiformis (Cooke): | |
– multipel (50 bis über 100) | |
– oft nur stecknadelkopfgroß. 1–2 mm | |
– gesamte oropharyngeale Mukosa (u. a. Gaumen. Gingiva) | |
– herpetiforme Anordnung | |
– kein Bläschenstadium | |
– sieben bis zehn Tage Präsenz | |
– drei bis fünf Tage schmerzhaft | |
– geringe Beeinträchtigung des Allgemeinzustandes | |
– episodisch | |
– ca. 5 % aller rekurrierenden Aphthen | |
Quelle: Jackowski et al.. 2017 |
Dabei werden die Unterscheidungen des Typs der oropharyngealen aphthoiden Erosionen wie Ulzerationen (Typen Minor, Major und herpetiform) und der Häufigkeit des Auftretens (rezidivierend beziehungsweise wiederkehrend: rekurrente aphthoide Erosionen/Ulzerationen oder Stomatitiden oder gelegentlich oder einmalig auftretende aphthoide Erosionen/Ulzerationen) im Zusammenhang mit den einzelnen Erkrankungen sehr verschiedenartig beschrieben. Die Differenzialdiagnose wird zusätzlich durch die mitunter ähnliche Morphologie erschwert.
Die Unterscheidung zwischen Aphthen beziehungsweise heterogenen ähnlichen (aphthoiden) Erosionen und Ulzerationen ist meist schwierig: große, anhaltende Läsionen erfordern eine weiterführende Diagnostik, um mögliche alternative Ursachen der Aphthosis zu erkennen.
Diagnostik und Differenzialdiagnostik
Zugrunde liegende Erkrankungen und ausdrücklich neoplastische Vorläuferläsionen oder ein manifestes Malignom sind insbesondere im Erwachsenenalter differenzialdiagnostisch auszuschließen.
Das Auftreten oropharyngealer aphthoider Erosionen beziehungsweise Ulzerationen kann auf Zusammenhänge mit autoinflammatorischen sowie intermediären Erkrankungen mit autoinflammatorischen und autoimmunologischen Aspekten vermutlicher immunpathologischer Ätiologie, hämatologischen Ursachen und Mangelerscheinungen, Erkrankungen des rheumatischen Formenkreises, Medikamentenanwendungen, möglicherweise auch mit bestimmten Nahrungsmitteln, weiteren Stoffen, Infektionskrankheiten, wahrscheinlich genetischen Faktoren und anderen Erkrankungen, beispielsweise prädisponierenden Faktoren, hindeuten. Daher sollten bei differenzialdiagnostischen Abwägungen etwaige Malabsorptions- oder Mangelzustände, Arzneimittelunverträglichkeiten oder systemische Erkrankungen Berücksichtigung finden [Kunkel et al., 2010].
Eine weiterführende spezialisierte Diagnostik sollte zudem bei Verdacht auf eine hämatologische oder immunologische Erkrankung als Hintergrund einer aphthoiden beziehungsweise ulzerösen Läsion erfolgen.
Zunächst sollten lokal begrenzte ulzeröse Läsionen anamnestisch und klinisch hinsichtlich möglicher mechanischer Ursachen – wie zum Beispiel Prothesendruckstellen, lokale Reizungen durch Halteelemente von Prothesen, mechanische Irritationen durch Restaurationen, etwaige Fadenreste nach operativen Eingriffen im Mund- oder Rachenbereich oder auch potenzielle Zustände nach zahnärztlichen Behandlungen (wie Irritationen durch Watterollen oder ähnlich), chemische oder thermische Irritationen oder lokale Einwirkungen von Medikamenten – untersucht werden.
Bei der pathohistologischen Untersuchung sind in der Regel nur unspezifische Veränderungen erkennbar. Zentral finden sich eine Nekrose und Fibrin, durchsetzt von Granulozyten. Am Rand entwickelt sich Granulationsgewebe. Bei granulomatösen Systemerkrankungen (wie M. Crohn mit Beteiligung der Mundhöhle) kann man typische Crohn-Granulome finden. Bei immunsupprimierten Patienten ist die entzündliche Reaktion geringer, beziehungsweise sie fällt zum Beispiel bei der Agranulozytose aus.
Grundsätzlich soll entsprechend der S2k-Leitlinie der DGMKG und der DGZMK bei einer unklaren Mundschleimhautveränderung ohne Rückbildungstendenz nach einer Beobachtung oder Therapie über zwei Wochen und ohne eindeutige Zuordnung zu einer definierten Grundkrankheit oder Ursache eine histologische Abklärung zum Ausschluss eines Plattenepithelkarzinoms und seiner Vorläuferläsionen erfolgen [Kunkel et al., 2010; Altenburg et al., 2014]. In gleicher Weise soll bei Rachenschleimhautveränderungen verfahren werden.
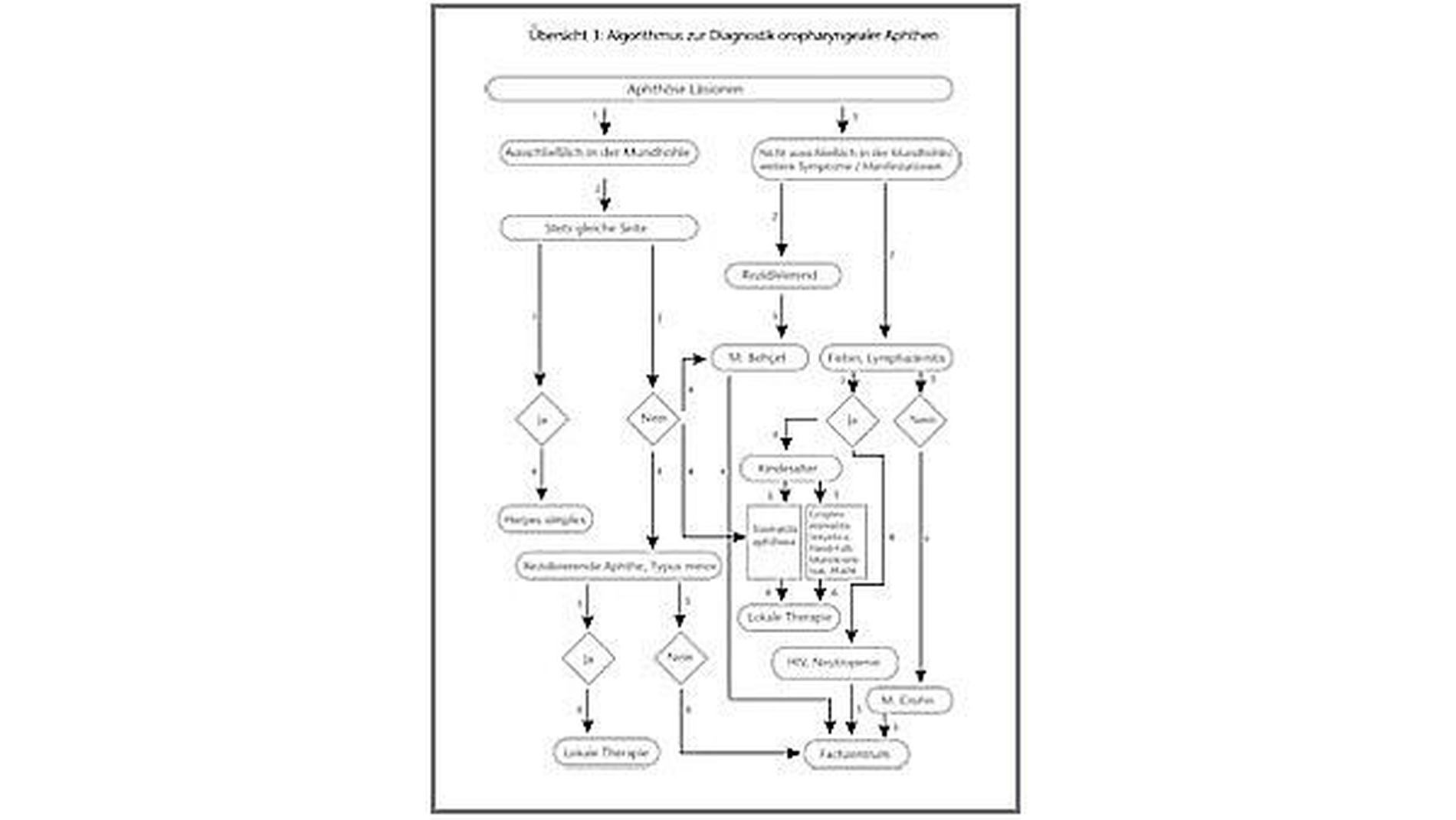
Übersicht 3 [aus: Jackowski et al., 2017] gibt den diagnostischen Algorithmus für oropharyngeale Aphthen wieder.
Therapie
Da die Ätiologie der rezidivierenden benignen Aphthosis nicht geklärt ist, erfolgt die Therapie symptomatisch (siehe auch Übersicht 4). In Deutschland sind hierzu derzeit lediglich Kortikosteroide und topische Antiseptika sowie Antiphlogistika zugelassen, die meisten anderen Substanzen kommen im „Off-Label-Use“ (siehe Kasten) [Alloson et al., 1998] zum Einsatz.
Da kontrollierte Studien ganz überwiegend an Erwachsenen durchgeführt wurden, ist die Indikation für Kinder und Jugendliche sowie während der Schwangerschaft und Stillzeit im Einzelfall gesondert zu prüfen. Nach Anwendung eines CO2 - oder Nd:YAG-Lasers bei der Behandlung oropharyngealer Aphthen wurde eine unmittelbare Schmerzreduktion beobachtet.
Bei länger als 14 Tage bestehenden Läsionen im Erwachsenenalter ist eine Biopsie obligat, vor allen Dingen wenn klinisch eine eindeutige Zuordnung zu habituellen Aphthen (Typus minor) nicht möglich ist.
Entsprechend der S2k-Leitlinie „Diagnostik und Management von Vorläuferläsionen des oralen Plattenepithelkarzinoms in der Zahn-, Mund- und Kieferheilkunde“ [AWMF-Register-Nr. 007/092; Kunkel et al., 2010] ist eine Abgrenzung von Vorläuferläsionen zu morphologisch ähnlichen Erkrankungen der Mundhöhle und des Rachens, zu denen auch die rezidivierenden oropharyngealen Aphthen gehören, erforderlich.
Bei länger bestehenden Aphthen im Kindesalter ist nur im Ausnahmefall eine Biopsie indiziert. Hier sollte die Abklärung möglicher weiterer Differenzialdiagnosen durch einen erfahrenen Pädiater oder Dermatologen erfolgen.
Bei habituellen oropharyngealen Aphthen sollten Lokalpräparate als Erstlinientherapie wegen des niedrigen Risikos systemischer Nebenwirkungen zur Anwendung kommen. Zu den topisch zu applizierenden Medikamenten zählen grundsätzlich Präparate, die adstringierend (Tinctura myrrhae et ratanhiae zur Behandlung gelegentlich auftretender Aphthen), antiseptisch (chlorhexidinhaltige Gele), antiinflammatorisch (kortisonhaltige Salben, die bei rezidivierendem Verlauf von Aphthen zwei- bis dreimal täglich lokal appliziert werden können), lokalanästhetisch (Lokalanästhetika) oder antibiotisch (Tetracyclin, Minocyclin: ab dem achten Lebensjahr) wirken. Lokalanästhetisch wirksame Medikamente sind vor der Einnahme von Mahlzeiten zu verabreichen. Ansonsten sind Tinkturen, Gele und Salben postprandial aufzulegen und vorübergehend mit einem Tupfer abzudecken.
Bei Aphthen vom Major-Typ können wiederholte tägliche Mundspülungen mit Tetracyclinlösung zur Vermeidung von Superinfektionen der Läsionen zum Einsatz kommen. Neben dem antimikrobiellen Effekt besitzen Tetracycline auf experimenteller Ebene nachgewiesene antiinflammatorische Eigenschaften, die über die Inhibition von Matrixmetalloproteinasen vermittelt werden [Skulason et al., 2009; Kennedy et al., 2014; Ogut et al., 2016; Gomes et al., 2017].
Bei schwersten Aphthosen sollten lokale Maßnahmen und systemische Therapien (Sucralfat, Colchicin, Prednisolon) angewandt werden. Es ist dabei jedoch zu beachten, dass die systemische Therapie nicht in das zahnärztliche Behandlungsspektrum fällt.
Bei Kindern und Jugendlichen sollte die Einleitung einer systemischen (gegebenenfalls auch „Off-Label-Use“) Therapie von hierin erfahrenen Pädiatern und bei Erwachsenen von hierin erfahrenen Fachärzten erfolgen (siehe auch Übersicht 4).
Therapieresistente, schwerste Aphthosen – wie zum Beispiel bei M. Behçet – können mit Dapson, Azathioprin, Ciclosporin-A oder Interferon-α behandelt werden. In Ausnahmefällen kann der Einsatz eines TNF-α-Inhibitors erwogen werden.
Bei zugrunde liegenden autoimmunologischen beziehungsweise autoinflammatorischen Erkrankungen sollte sich die Therapie nach der weiteren Organbeteiligung richten.
Entsprechende Hinweise zu den Therapiestrategien werden in der S2k-Leitlinie „Diagnostik und Therapieoptionen von Aphthen und aphthoiden Läsionen der Mund- und Rachenschleimhaut“ [AWMF-Register-Nr. 007–101, Jackowski et al., 2017] gegeben und weiter ausgeführt.
Anmerkung der Autoren
Für die Empfehlung zum Einsatz bei Aphthen und aphthoiden Läsionen der Mund- und Rachenschleimhaut müssen die „Off-Label-Use“-Kriterien beachtet werden:
nachgewiesene Wirksamkeit
günstiges Nutzen-Risiko-Verhältnis
fehlender Alternativ-Heilversuch.
Ein „Off-Label-Use“ ist nur bei schwerwiegenden Verlaufsformen statthaft, wenn es keine therapeutischen Alternativen gibt. Dem Stand der wissenschaftlichen Erkenntnisse entsprechend muss die begründete Aussicht bestehen, dass die Behandlung erfolgreich verläuft. Darüber hinaus unterliegt die Aufklärung einer zusätzlichen, besonderen Verpflichtung. Die Patientinnen/Patienten sind auf den Umstand des „Off-Label-Use“ und daraus resultierende mögliche Handlungskonsequenzen aufmerksam zu machen. Eine gemeinsame Entscheidungsfindung ist notwendig [aus: Jackowski et al., 2017].
PD Dr. Frank Peter Strietzel
Charité – Universitätsmedizin Berlin
Charité Centrum 3 für Zahn-, Mund- und Kieferheilkunde, Oralmedizin, zahnärztliche Röntgenologie und Chirurgie
Aßmannshauser Str. 4–6, 14197 Berlin
frank.strietzel@charite.de
Prof. Dr. Jochen Jackowski
Department für ZMK-Heilkunde, Fakultät für Gesundheit
Universität Witten/Herdecke
Abteilung für Zahnärztliche Chirurgie und Poliklinische Ambulanz
Alfred-Herrhausen-Str. 45, 58455 Witten
Dr. Andreas Altenburg
Klinik für Dermatologie, Venerologie und Allergologie / Immunologisches Zentrum
Klinikum Dessau
Auenweg 38, 06847 Dessau-Roßlau
und
Medizinische Hochschule Brandenburg Theodor Fontane
Fehrbelliner Str. 38, 16816 Neuruppin
Dr. Jörg Beck
KZBV – Kassenzahnärztliche Bundesvereinigung
Behrenstr. 42, 10117 Berlin
Dr. Dr. Markus Hullmann
Universitätsklinikum Regensburg
Klinik für Mund-, Kiefer- und Gesichtschirurgie
Franz-Josef-Strauß-Allee 11, 93053 Regensburg
PD Dr. Tilmann Kallinich
Charité – Universitätsmedizin Berlin
Klinik für Pädiatrie mit Schwerpunkt Pneumologie und Immunologie
Augustenburger Platz 1, 13353 Berlin
Prof. Dr. Ina Kötter
4. Medizinische Abteilung, Rheumatologie, Klinische Immunologie, Nephrologie
Asklepios Klinik Altona
Paul-Ehrlich-Str. 1, 22763 Hamburg
Prof. Dr. Armin Laubert
Katholisches Krankenhaus St.-Josef Hagen
Klinik für Hals-, Nasen- Ohrenheilkunde, Kopf- u. Hals-Chirurgie
Dreieckstr.15, 58097 Hagen
Prof. Dr. Wilko Weichert
Technische Universität München
Institut für Allgemeine Pathologie und Pathologische Anatomie
Trogerstr. 18, 81675 München
Prof. Dr. Andrea-Maria Schmidt-Westhausen
Charité – Universitätsmedizin Berlin
Charité Centrum 3 für Zahn-, Mund- und Kieferheilkunde, Oralmedizin, zahnärztliche Röntgenologie und Chirurgie
Aßmannshauser Str. 4–6, 14197 Berlin
Literaturliste
Allison, P, Franco, E, Black, M, Feine, J (1998). The role of professional diagnostic delay in the prognosis of upper aerodigestive tract carcinoma. Oral Oncology, 34, 147–153.
Altenburg, A, Micheli, CK, Puttkammer, M, Abdel-Naser, MB, Zouboulis, CC (2014). Behandlung chronisch-rezidivierender oraler Aphthen. Dtsch Ärztebl Int, 111, 665–673.
Chattopadhyay A, Chatterjee S (2007). Risk indicators for current aphthous ulcers among adults in the US. Community Dent Oral Epidemiol; 35(2), 152–159.
Gomes JR, Omar NF, Neves JDS, Novaes PD (2017). Doxycycline reduces the expression and activity of matrix metalloproteinase-2 in the periodontal ligament of the rat incisor without altering the eruption process. J Periodontal Res; 52(3), 353–359.
Hornstein, OP (1998). Aphthen und aphthoide Läsionen der Mundschleimhaut. HNO 2, 102–111.
Jackowski J, Strietzel FP, Altenburg A, Beck J, Hullmann M, Kallinich T, Kötter I, Laubert A, Schmidt-Westhausen AM, Weichert W (2017). S2k-Leitlinie Diagnostik und Therapieoptionen von Aphthen und aphthoiden Läsionen der Mund- und Rachenschleimhaut (AWMF-Registernummer: 007–101)
Jurge, S, Kuffer, R, Scully, C, Porter, SR (2006). Mucosal disease series. Number VI. Recurrent aphthous stomatitis. Oral Dis, 12(1), 1–21.
Kennedy R, Alibhai M, Shakib K (2014). Tetracycline: a cure all? Br J Oral Maxillofac Surg; 52(4),382–383.
Kleinman DV, Swango PA, Pindborg JJ (1994). Epidemiology of oral mucosal lesions in United States schoolchildren: 1986–1987. Community Dent Oral Epidemiol; 22 (4): 243–253.
Kowalski, LP, Carvalho, AL (2001). Influence of time delay and clinical upstaging in the prognosis of head and neck cancer. Oral Oncol, 37(1), 94–98.
Kramer, IR, Pindborg, JJ, Bezroukov, V., Infirri, JS (1980). Guide to epidemiology and diagnosis of oral mucosal diseases and conditions. World Health Organization. Community Dent Oral Epidemiol, 8(1), 1–26.
Kunkel, M, Hertrampf, K (2010). S2k-Leitlinie „Diagnostik und Management von Vorläuferläsionen des oralen Plattenepithelkarzinoms in der Zahn-, Mund- und Kieferheilkunde“ (AWMF-Register Nr. 007/092)
Legal, S, Behr, M, Fanghänel, M, Gosau, P, Reichert, TE (2013). Aphthen und Aphtoide Läsionen. Dtsch Zahnärztl Z, 68(5), 264–268.
Majorana, A, Bardellini, E, Flocchini, P, Amadori, F, Conti, G, Camous, G (2010).Oral mucosal lesions in children from 0 to 12 years old: ten years´ experience. Oral Surg Oral Med Oral Pathol Oral Radiol Endodod,110(1), e13–18.
Ogut D, Reel B, Gonen Korkmaz C, Arun MZ, Cilaker Micili S, Ergur BU (2016). Doxycycline down-regulates matrix metalloproteinase expression and inhibits NF-κB signaling in LPS-induced PC3 cells. Folia Histochem Cytobiol; 54(4), 171–180.
Reichart PA, (2000). Oral mucosal lesions in a representative cross-sectional study of aging Germans. Community Dent Oral Epidemiol; 28(5), 390–398.
Schmidt E, Goebeler M, Hertl M, Sárdy M, Sitaru C, Eming R, Hofmann SC, Hunzelmann N, Kern JS, Kramer H, Orzechowski HD, Pfeiffer C, Schuster V, Sporbeck B, Sticherling M, Worm M, Zillikens D, Nast A (2015) S2k guidelines for the treatment of pemphigus vulgaris/foliaceus and bullous pemphigoid. J Dtsch Dermatol Ges, 13(7), 713–721.
Scully, C, Porter, S (2008). Oral mucosal disease: recurrent aphthous stomatitis. Br J Oral Maxillofac Surg, 46(3), 198–206.
Shohat-Zabarski R, Kalderon S, Klein T, Weinberger A (1992). Close association of HLA-B51 in persons with recurrent aphthous stomatitis. Oral Surg Oral Med Oral Pathol; 74(4), 455–458.
Skulason S, Holbrook WP, Kristmundsdottir T (2009). Clinical assessment of the effect of a matrix metalloproteinase inhibitor on aphthous ulcers. Acta Odontol Scand; 67(1), 25–29.






