Metastase, Mukositis, Mundhygiene
Rund 29.000 Menschen erkranken jährlich in Deutschland an Blasenkrebs. Dabei sind Männer rund dreimal häufiger betroffen als Frauen, allerdings ist die Inzidenz der Krankheitsfälle bei ihnen rückläufig. Trotzdem steigt die Häufigkeit des Blasenkarzinoms aufgrund der demografischen Entwicklung.
Der Unterschied in der Krankheitshäufigkeit zwischen Männern und Frauen besteht in allen Altersgruppen und verstärkt sich mit steigendem Lebensalter. Dabei erkranken Männer im Mittel mit 74 Jahren, Frauen mit 77 Jahren.
Risikofaktoren
Neben einem höheren Lebensalter und dem männlichen Geschlecht zählt vor allem das Rauchen zu den Risikofaktoren für ein Urothelkarzinom. So sind Raucher zwei- bis dreimal häufiger betroffen als Nichtraucher. Das kann die rückläufige Inzidenz bei Männern erklären, da die Zahl der aktiven Raucher abnimmt.
Weitere Risikofaktoren sind chronische Blasenentzündungen sowie eine Exposition gegenüber verschiedenen Chemikalien (insbesondere aromatischen Aminen), weshalb das Harnblasenkarzinom als Berufserkrankung anerkannt ist. Gefährdet sind etwa Arbeiter in der Gummi-, Chemie- und Lederindustrie sowie Friseure, Metallarbeiter, Drucker, Maler, Textilarbeiter und Lastwagenfahrer. Vom Zeitpunkt der Exposition mit krebserregenden Chemikalien bis zur Manifestation und Diagnose eines Harnblasenkarzinoms kann es allerdings laut Krebsinformationsdienst (KID) bis zu 40 Jahre dauern. Daher tritt das berufsbedingte Blasenkarzinom laut KID trotz heutiger Schutzmaßnahmen weiterhin auf.
Davon abgesehen gibt es offensichtlich auch ein genetisches Risiko. Denn Patienten mit einem erblichen Darmkrebs, dem HNPCC (nicht polypöse Karzinome, Lynch-Syndrom), entwickeln überproportional häufig auch Blasenkrebs.
Etwa drei Viertel der Patienten weisen bei der Diagnosestellung einen oberflächlichen (nicht bis in den Muskel infiltrierten) Tumor auf. Bei einem Viertel dagegen liegt ein bereits fortgeschrittenes invasives Karzinom vor mit Infiltration der Muskelschicht. Ursache hierfür ist, dass das Blasenkarzinom im Frühstadium in aller Regel kaum Beschwerden verursacht. Es gibt zudem keine validen nicht invasiven Früherkennungsuntersuchungen, die ein entsprechendes Screening in der breiten Bevölkerung sinnvoll machen würden.
Symptome
Zu den Symptomen eines Harnblasenkarzinoms gehört vor allem die Hämaturie, wobei eine Mikro- oder eine Makrohämaturie vorliegen kann. Allerdings stellt auch die Hämaturie nur ein unspezifisches Symptom dar und kann auf verschiedene urologische Erkrankungen hinweisen. Weitere potenzielle Symptome sind allgemeine Veränderungen beim Wasserlassen, ein vermehrter Harndrang mit Druck auf der Blase sowie ein sogenanntes Blasengefühl, also das Gefühl, die Blase zu spüren. Im fortgeschrittenen Stadium kann sich der Tumor ferner durch Schmerzen im Unterbauch und/oder der Nierengegend sowie durch vergrößerte Lymphknoten bemerkbar machen.
Formen und Stadien
Bei rund 90 Prozent der Patienten gehen die Tumore direkt vom Urothel, also vom Epithel der ableitenden Harnwege aus. Sie entstehen zumeist direkt in der Harnblase, seltener im oberen Harntrakt, also den Harnleitern oder dem Nierenbecken, das von der gleichen Schleimhaut ausgekleidet ist. Die Tumore können flach oder auch warzenförmig (papillär) wachsen und bilden sich häufig multifokal.
Deutlich seltener kommt es laut KID in der Harnblase zu Tumoren, die von anderen Geweben ausgehen. Dazu gehören Plattenepithelkarzinome oder die aus den Deckschichten des Drüsengewebes hervorgehenden Adenokarzinome. Außerdem gibt es Mischformen, in denen sich Anteile von Tumorzellen aus verschiedenen Ausgangsgeweben finden. Zu beachten ist, dass die Harnblase auch betroffen sein kann, wenn Tumore sich von anderen Organen ausbreiten, was beispielsweise beim Darmkrebs, beim Nierenkrebs und bei gynäkologischen Tumoren der Fall sein kann.
Die Prognose beim Blasenkarzinom ist direkt abhängig vom Tumorstadium, also von der Frage, ob der Tumor noch auf die Schleimhautschicht der Blase beschränkt oder bereits in tiefere Schichten der Blasenwand oder in andere Organe im Harntrakt (Nierenbecken, Harnleiter oder Harnröhre) vorgedrungen ist.
Zu differenzieren sind bei nicht invasiven Tumoren die Stadien:
pTa als nicht muskelinvasives, auf die Schleimhaut begrenztes Karzinom
pTis als Carcinoma in situ und
Bei infiltrierenden, invasiven Karzinomen sind als Tumorstadien zu unterscheiden:
pT2 mit Ausbreitung des Tumors auf die Muscularis propria
pT3 mit Ausbreitung des Tumors über die Muscularis propria hinaus
pT4 mit Ausbreitung auf Organe im Becken wie die Prostata oder den Gebärmutterhals
pN1 bei Vorliegen einer solitären Lymphknotenmetastase im kleinen Becken
pN2 bei multiplen Lymphknotenmetastasen im kleinen Becken
pN3 bei Lymphknotenmetastasen im Bereich der Arteria iliacae communes
NX wenn regionäre Lymphknoten nicht beurteilt werden können
N0 wenn es keinen Anhalt für regionäre Lymphknotenmetastasen gibt
MX wenn Fernmetastasen nicht beurteilt werden können
M0 wenn es keinen Anhaltspunkt für Fernmetastasen gibt
M1 wenn Fernmetastasen vorliegen.
Behandlung
Die Behandlung des Harnblasenkarzinoms richtet sich nach dem Tumorstadium und der Lokalisation des Tumors. Zu differenzieren ist auch bei der Behandlung zwischen einem oberflächlichen und einem muskel-infiltrierenden Tumorstadium:
Liegt ein nicht invasiver Tumor vor, besteht das Therapieziel in der Heilung. Primär ist eine transurethrale Resektion (TUR-B) angezeigt, wobei versucht wird, die Geschwulst über eine Elektroschlinge zu entfernen. Der Eingriff erfolgt üblicherweise in Teil- oder in Vollnarkose. Zusätzlich ist meist eine lokale Chemotherapie indiziert oder eine Instillationstherapie mit dem attenuierten Lebendimpfstoff Bacillus Calmette-Guérin, um das Rezidivrisiko zu senken. Der abgeschwächte Tuberkulose-Erreger kann eine relativ unspezifische Immunantwort gegen den Tumor auslösen, die die Wirkung der Chemotherapie unterstützt. Die Instillationstherapie erstreckt sich üblicherweise über mehrere Monate. Die Spülungen werden über einen Blasenkatheter durchgeführt, eine Narkose ist nicht erforderlich. Die Lösung verbleibt laut KID für eine halbe bis zu zwei Stunden in der Blase. Die Patienten sollten vorher und währenddessen nicht trinken, um eine Verdünnung der Medikamente in der Blase zu verhindern.
Bei einem papillären oder bei einem bereits tiefer vorgedrungenen Tumor reicht die erste transurethrale Resektion laut KID nicht aus, da möglicherweise noch Tumorzellen in der Harnblasenwand verblieben sind. Studien zeigen, dass nach einer ersten TUR in 20 bis 75 Prozent der Fälle in der Harnblase noch Tumorzellen nachweisbar sind.
Um das Rezidivrisiko zu senken, wird daher bei vielen Patienten eine Nachresektion empfohlen. Hierfür sprechen sich die Experten laut KID aus,
wenn die erste TUR unvollständig war und möglicherweise Tumorgewebe verblieben ist,
wenn bei der ersten TUR kein Muskelgewebe im entnommenen Gewebe zu finden war oder
wenn bei der histologischen Aufbereitung eine aggressiv wachsende Tumorform festgestellt wurde.
Die zweite TUR sollte im Idealfall innerhalb von sechs Wochen nach dem ersten Eingriff erfolgen.
In seltenen Fällen kann auch beim nicht muskelinvasiven Karzinom eine Teilresektion oder eine komplette Zystektomie notwendig sein. Die Indikation hierfür besteht bei sehr hohem Rückfallrisiko aufgrund eines aggressiv wachsenden Tumors mit multifokalen Tumorherden.
Liegt ein muskelinvasives Karzinom vor, ist eine Teilresektion der Blase und in der Mehrzahl der Fälle sogar eine radikale Zystektomie einschließlich der Entfernung der Beckenlymphknoten indiziert. Bei Männern werden außerdem die Prostata und die Samenblasen entfernt und die Samenleiter durchtrennt. Bei Frauen werden die Gebärmutter, die Eierstöcke, die Eileiter und ein Teil der Scheidenwand operativ entfernt.
Der Urin wird dann häufig über ein zwischen Harnleiter und Bauchwand geschaltetes Darmstück nach außen abgeleitet und in einen auf die Bauchdecke geklebten Beutel entleert (Ileumkonduit). Eine weitere Möglichkeit besteht nach Angaben der Deutschen Krebsgesellschaft in der Ausbildung einer Ersatzblase (Neoblase) aus einem Stück Dünndarm, die an die Harnröhre angeschlossen wird. Damit wird das Wasserlassen über den ursprünglichen Weg möglich, allerdings mit einer hohen Wahrscheinlichkeit für die Entwicklung einer Harninkontinenz. Die Bildung einer Neoblase aus Darmgewebe ist in aller Regel allerdings nicht möglich bei Patienten mit chronischen Darmerkrankungen wie einem Morbus Crohn oder einer Colitis ulcerosa.
Musste neben der Harnblase auch die Harnröhre entfernt werden, wird im Allgemeinen ein Pouch gebildet. Dabei wird ein Ende des Darms mit der Bauchdecke verbunden. Über das Stoma wird der Urin mittels eines Katheters, der in das Stoma eingeführt wird, entleert. Damit nicht ständig Urin austritt, kann der Pouch mit einem speziellen Ventilmechanismus versehen werden. Eine Alternative ist die Harnableitung über den Enddarm, wenn der Patient über einen gut funktionierenden Schließmuskel verfügt und eine gewisse Menge an Flüssigkeit im Darm halten kann.
Neben der Operation ist bei fortgeschrittenen Tumoren eine Chemotherapie und gegebenenfalls auch eine Radiotherapie indiziert. Vor allem bei einem bereits metastasierten Tumor sind die Heilungsaussichten allerdings gering.
Krebsimmuntherapie
Als neue Therapieoption ist die Krebsimmuntherapie auch beim Urothelkarzinom zugelassen worden. Es geht bei dem Verfahren darum, das körpereigene Immunsystem im Kampf gegen den Tumor zu unterstützen. Denn Krebszellen können Immun-Checkpoints aktivieren, die den Organismus vor überschießenden Immunreaktionen bewahren. Dadurch wird die Abwehrkraft herunterreguliert und das Tumorwachstum begünstigt. Durch Immun-Checkpoint-Inhibitoren kann versucht werden, diese Entwicklung wieder umzukehren. Solche Krebsimmuntherapeutika bewirken zwar keine Heilung des Tumors, können das Fortschreiten der Erkrankung aber hemmen und eine signifikante Verlängerung des Überlebens der Patienten bewirken.
Christine VetterMedizinische Fachjournalistin
Weiterführende Informationen:
Deutsche Krebsgesellschaft
Onkopedia Leitlinien
Krebsinformationsdienst
Aus Sicht der Zahnmedizin
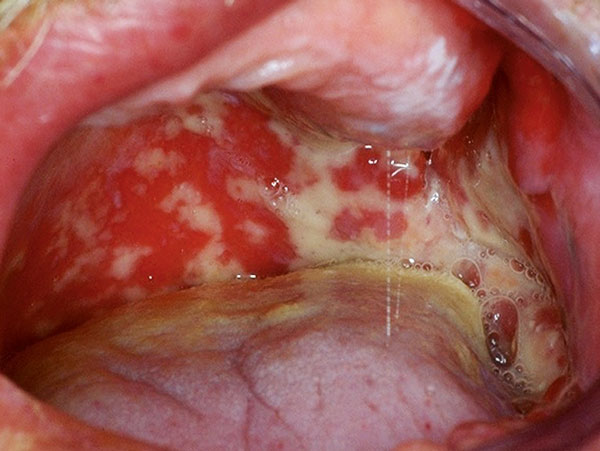
Orale Mukositis
Die Behandlung des Harnblasenkarzinoms richtet sich – wie bei malignen Erkrankungen anderer Lokalisationen – nach der Histologie, dem Tumorstadium und dem Vorhandensein weiterer Faktoren, zum Beispiel einer Metastasierung. Bei jedem Patienten mit einer Tumorgröße ≥ cT2 (lokalisiertes, muskelinvasives Blasenkarzinom) sollte die Option einer zusätzlichen neoadjuvanten oder adjuvanten Chemotherapie in Erwägung gezogen werden, die die Gesamtüberlebensrate und somit die Prognose deutlich verbessert. Bei beiden Ansätzen wird vor allem eine Cisplatin-haltige Kombinationstherapie (Cisplatin/Gemcitanin/Methotrexat/Vinblastin/Doxorubicin) angewandt. Trotz bemerkenswerter Fortschritte in der Therapie entwickeln ungefähr 40 Prozent dieser Patienten unter vorangegangener oder laufender Chemotherapie Nebenwirkungen in der Mundhöhle, wobei bei etwa der Hälfte dieses Kollektivs eine orale Mukositis entsteht (Mundhöhle, Oro- und Hypopharynx; siehe Abbildung), die unter anderem eine Veränderung, Verschiebung oder gar prognoserelevante Unterbrechung der Therapie verursachen kann. Mukositis-bedingte Schmerzen müssen häufig mit Morphinen behandelt werden, da diese es den Patienten unter anderem erschweren, Nahrung aufzunehmen, was möglicherweise zur Unterernährung führt. Dies kann mit allgemeinen Gesundheitsrisiken einhergehen, einschließlich einer verringerten Immunreaktion und dem potenziellen Risiko einer Aspiration von Nahrungsmitteln aufgrund von Schluckstörungen. Darüber hinaus können Schwierigkeiten bei der Nahrungsaufnahme und eine schlechte Mundhygiene zu einem synergistischen Anstieg der oralen Bakterien und zu einem wiederum erhöhten Risiko für eine Aspirationspneumonie führen. Mit zunehmender Langlebigkeit und verbesserter Zahnpflege kann die Zunahme älterer Patienten unter Chemotherapie mit verbliebenen Zähnen und/oder komplexen oralen Prothesen erwartet werden. Dieses Szenario erhöht die Möglichkeit, dass die komplexe orale Umgebung in Kombination mit einer verbesserungswürdigen Mundhygiene zu einer weiteren Exazerbation der oralen Nebenwirkungen beitragen wird.
Die unterstützende Rolle des Zahnarztes
Basierend auf den aktuellen Leitlinien wird daher die zahnärztlich-supportive Intervention als ein wesentlicher Bestandteil der Krebstherapie gesehen. In Studien wurde nachgewiesen, dass die Inzidenz einer aufgrund von Chemo- und Strahlentherapie entstandenen oralen Mukositis unter sorgfältiger zahnärztlicher Pflege um 70 Prozent reduziert werden konnte. Insbesondere zeigte sich eine prätherapeutische Sanierung möglicher Foci und eine unterstützende Verbesserung der Mundhygiene (inklusive antifugaler Therapie) und Mundfeuchtigkeit sowie die Anwendung lokaler Oberflächenanästhetika als zielführend. Die Anzahl der Bakterien im Mund und somit das Auftreten von Sekundärinfektionen der Mundschleimhaut und des Parodontalgewebes werden reduziert. Regelmäßige Kontrollen können frühzeitig das Ausmaß weiterer Probleme (etwa Schleimhautverletzungen aufgrund von unsachgemäßer Selbstpflege) reduzieren. Insbesondere in Krankenhäusern ohne zahnärztliche Versorgungsmöglichkeit oder im Rahmen ambulant durchgeführter Chemotherapien erscheint daher eine intensivierte Zusammenarbeit mit dem für das Problem sensibilisierten niedergelassenen Zahnarzt notwendig.
PD Dr. Dr. Peer W. Kämmerer, M.A., FEBOMFS
Stellvertretender Klinikdirektor/Leitender Oberarzt
Klinik und Poliklinik für Mund-, Kiefer- und Gesichtschirurgie, Universitätsmedizin Mainz
Augustusplatz 2, 55131 Mainz
peer.kaemmerer@unimedizin-mainz.de
Dr. Dr. Andreas Pabst
Assistenzarzt
Klinik für Mund-, Kiefer- und Plastische Gesichtschirurgie
Bundeswehrzentralkrankenhaus Koblenz
Rübenacherstr. 170, 56072 Koblenz




