Vergrößerungshilfen in der Kariologie
Eigentlich gibt es nur drei Anforderungen, die man an eine brauchbare Kariesdiagnostik stellen kann. Sie muss
Karies von Nicht-Karies unterscheiden,
Kavitationen erkennen und
die Progressionswahrscheinlichkeit („Läsionsaktivität“) abschätzen können [Neuhaus und Lussi, 2018].
Aus der Erkenntnis dieser drei Informationen leitet sich die Behandlungsstrategie ab, die von Abwarten und Beobachten über geeignete Prophylaxemaßnahmen, mikroinvasive und Füllungstherapie bis zum Entscheid über den Zahnerhalt reicht. Das Erkennen von Kavitationen ist dabei sicherlich die Paradedisziplin für die visuell-taktile Kariesdiagnostik [Lussi, 1993; Lussi, 1996; Neuhaus et al., 2009].
Dieser Punkt ist von besonderer Relevanz, da er über den Einsatz invasiver Behandlungsoptionen entscheidet – insbesondere im Hinblick darauf, dass eine nicht mit häuslichen Mitteln zu reinigende kariöse Kavität eine Indikation zur invasiven Kariestherapie darstellt. Mit keinem anderen Hilfsmittel ist dies so sicher möglich wie mit dem Auge. Das Röntgenbild kann zwar die Kariesprogression im Dentin (approximal auch im Schmelz) gut darstellen, erlaubt aber eigentlich keine Aussage darüber, ob die Oberfläche eingebrochen ist oder nicht. Bei einer röntgenologisch mittleren bis tiefen Dentinläsion erwarten wir eine Kavität, weil wir empirisch die entsprechende Erfahrung gemacht haben, aber „sehen“ kann man die Kavität auf dem Röntgenbild nicht.
Die menschliche Sehfähigkeit
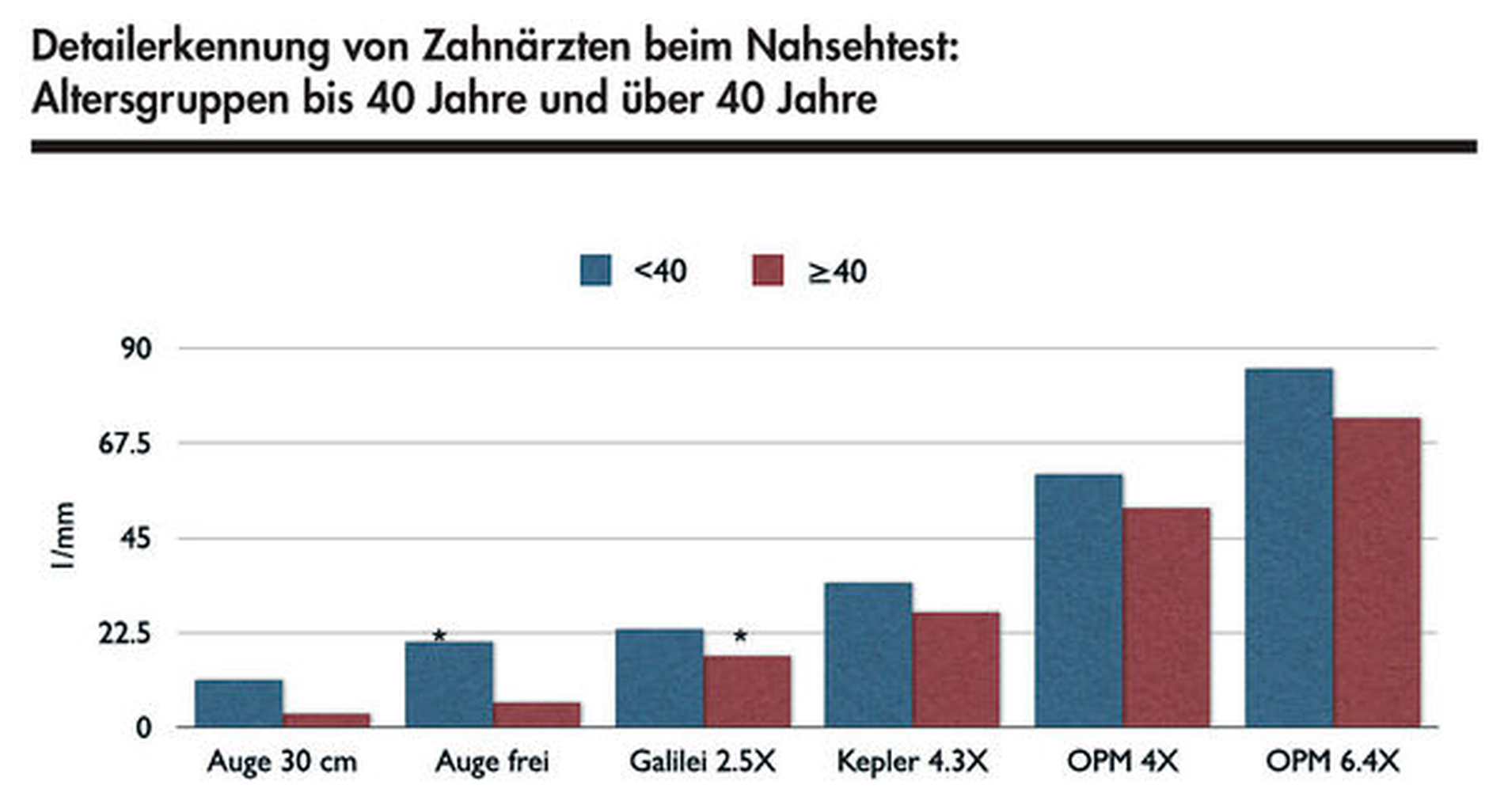
Wir wissen, dass der menschliche Körper mit zunehmendem Alter bestimmten Alterungsprozessen unterliegt. Bekannt ist die „Weitsichtigkeit“, die gemeinhin ab dem 40. Lebensjahr (individuell unterschiedlich!) langsam beginnt und fortschreitet. Die Linse wird weniger flexibel, dadurch gelingt die Akkommodation mit der Zeit schlechter. Das heißt, dass die Fähigkeit zur Nahsicht abnimmt. Ein Beispiel aus dem zahnärztlichen Alltag: Man präpariert eine Klasse-II-Kavität und gibt auf den Nachbarzahn acht, damit er nicht touchiert und unbeabsichtigt verletzt wird. Durch eine Annäherung des eigenen Kopfes an den Mund des Patienten vergrößert sich das wahrgenommene Bild und man präpariert vorsichtiger und sicherer [Eichenberger et al., 2018].
Dieses ergonomisch schlechte Verhalten lässt sich hundertfach im Studentenkurs beobachten; daher wird der Gebrauch von Lupenbrillen empfohlen, um die Nahsicht durch Heranbewegen des Kopfes auszugleichen und den Rücken des Behandlers zu schonen. Es wurde nämlich gezeigt, dass eine 2,5-fache Galilei-Lupenbrille bei Zahnärzten über 40 Jahren zu einem gleich guten Sehresultat führt wie die (akkomodierte) Nahsicht bei jüngeren Kollegen [Eichenberger et al., 2011].
In Bezug auf die visuelle Kariesdiagnostik, die nicht zuletzt auch vom Detailsehen abhängt, leitet sich daraus ab, dass man wissen muss, ob die eigenen Augen noch gut funktionieren. Ein jährlicher Sehtest ist spätestens ab dem 40. Lebensjahr sinnvoll [Perrin et al., 2014; Eichenberger et al., 2015]. Es gibt sogar eine Studie, nach der man behelfsmäßig mit einem 5-Dollar-Schein einen Schnell-Sehtest machen kann, der erstaunlich genau ist [Perrin et al., 2017]. Studien aus Bern zeigten bei zahnärztlichen Kollegen (n = 136), dass die Selbsteinschätzung und das tatsächliche Sehen in etwa einem Drittel der Fälle stark differierte: Ein Drittel der Kollegen meinte, gut bis sehr gut sehen zu können, zeigte aber bei einem validierten Nahsehtest eine unterdurchschnittliche Performance.
In einer Studie von Koller wurde bei zwei kalibrierten Zahnärzten mit exzellentem Visus die Sehkraft durch sogenannte „Okklusivfolien“ standardisiert in zwei Schritten verschlechtert, so dass sie normal- bis schlechtsichtig wurden. Es zeigte sich, dass sowohl für Schmelzkaries als auch für Dentinkaries die Genauigkeit der Diagnostik signifikant abnahm [Koller, 2017]. Dieses Ergebnis war zu erwarten, aber dass die Sensitivität für Dentinkaries in diesem Versuch unter 50 Prozent sank, lässt doch aufhorchen.
Viel hilft viel – wirklich?
Vergrößerung
Nun ist es so, dass es auch viele zahnärztliche Kollegen gibt, die sich der Probleme der Alterssichtigkeit bewusst sind und daher bewusst für sich den Entscheid getroffen haben, mit Lupe, Prismenlupe oder Mikroskop zu arbeiten. Das ist unbedingt zu begrüßen, da man mit geeigneten Vergrößerungen „besser“ arbeitet [Eichenberger et al., 2018]. Besseres Detailsehen führt zu genauerem Arbeiten und insbesondere in der Endodontie kann man eine verbesserte Prozess- und Ergebnisqualität erwarten [Perrin et al., 2017].
Die Herstellerangaben zu Vergrößerungen der Lupen sind nicht normiert. In einer Studie wurden von einem unabhängigen Institut in definiertem Abstand durch die Lupen jeweils Fotos auf Millimeterpapier angefertigt und es fanden sich bedeutende Unterschiede in Bezug auf nominale und gemessene Vergrößerungen der Lupen [Neuhaus et al., 2013]. Auch die optische Qualität der Brillen auf dem Markt schien unterschiedlich zu sein.
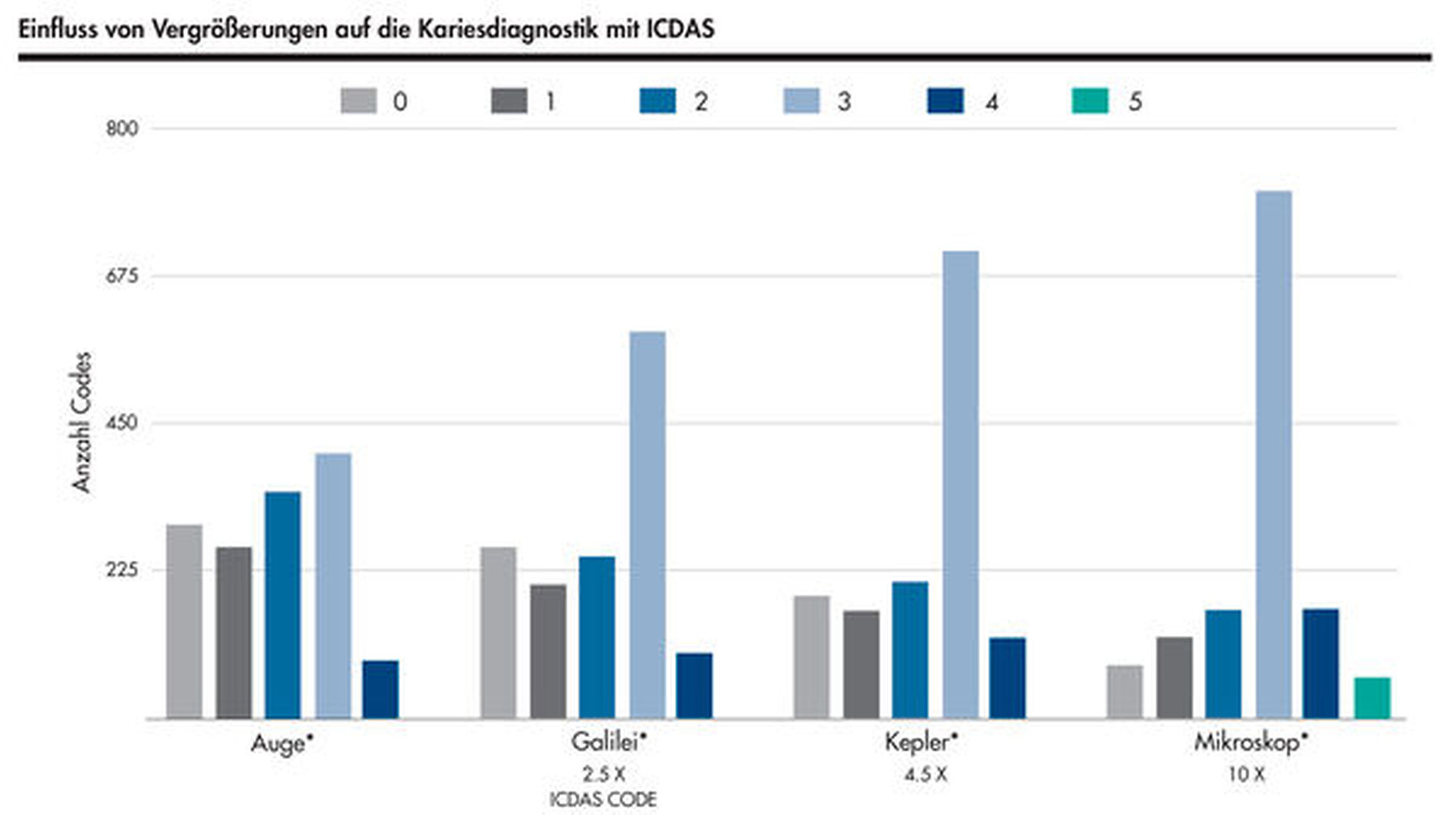
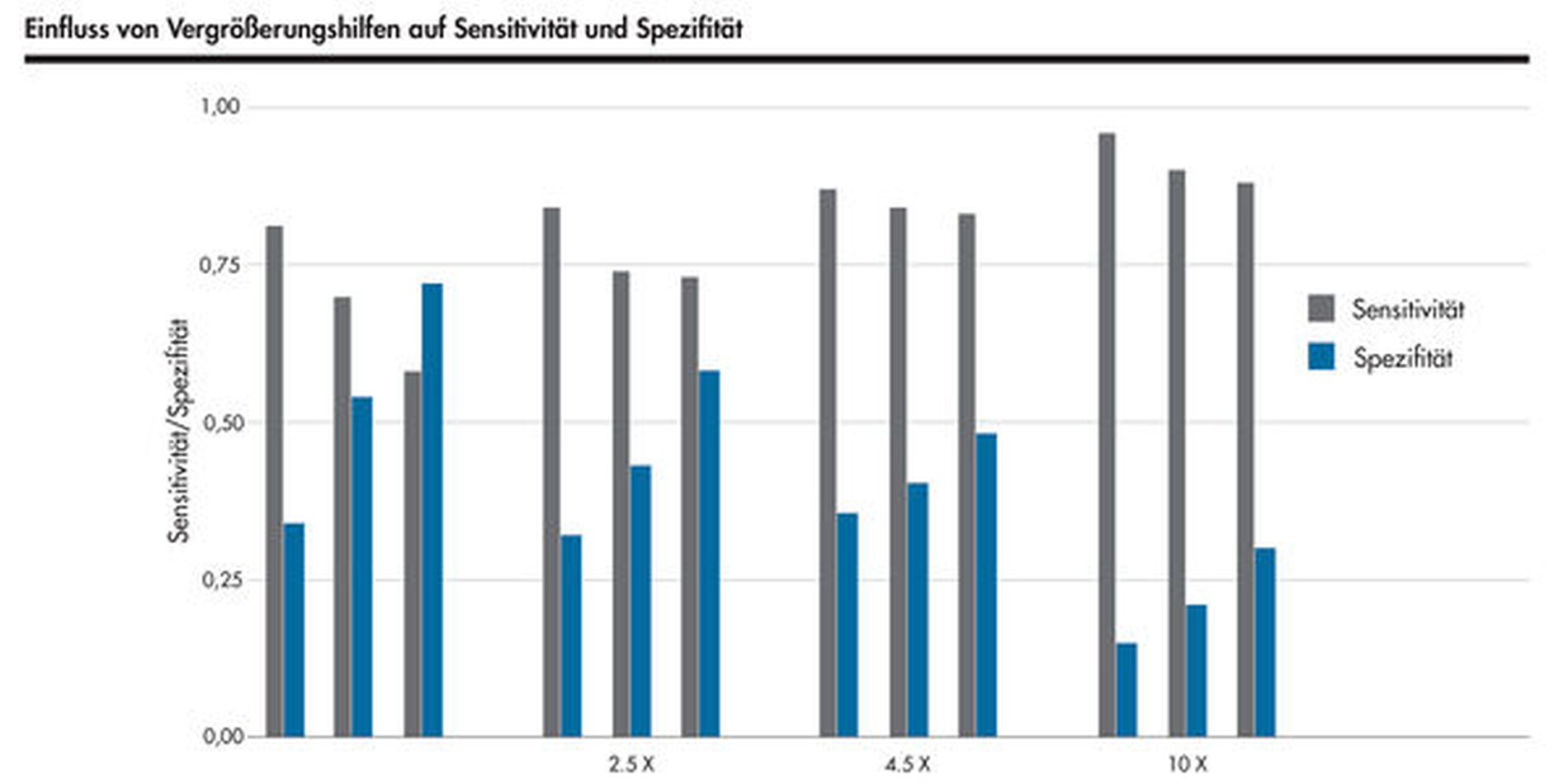
Für die visuelle Kariesdiagnostik können sich aber Probleme bei zu großen Vergrößerungen ergeben. Vergrößerungen mit dem Mikroskop erlauben mitunter eine direkte Sicht in verfärbte Fissuren oder Grübchen. In einer Studie mit 15 Untersuchern (je fünf Studenten, Allgemeinzahnärzte und Spezialisten) wurde gezeigt, dass mit dem Mikroskop vermeintlich offene Dentinläsionen detektiert wurden, die keine waren [Neuhaus et al., 2015]. Die gleichen Zähne wurden bei kleineren Vergrößerungen richtigerweise als Initialläsionen klassifiziert (Abbildungen 6 und 7). Die Konsequenz ist dramatisch: Eine offene Dentinläsion wird schließlich invasiv behandelt, während eine Initialkaries mit pseudointakter Oberfläche eine non-invasive Behandlung erfährt.
Vermutlich ist die Fehlinterpretation „offene Dentinläsion“ durch intensive Kalibrierung vermeidbar, aber entsprechende Lernprogramme für Kariesdiagnostik mit großen Vergrößerungen existieren bislang nicht. Die Studie hat gezeigt, dass schon mit Prismenlupen die Spezifität stark abnimmt. Daher muss man sagen, dass zu große Vergrößerungen (ab circa 4,5x) das Risiko falsch positiver Kariesbewertungen mit der Konsequenz einer Übertherapie nach sich ziehen.
Beleuchtung
Gerade in der älteren Literatur und in Lehrbüchern finden sich Formulierungen wie etwa die, dass für eine gute visuelle Kariesdiagnostik die Zähne trocken und optimal beleuchtet sein müssen. Was aber ist die optimale Beleuchtung? Schaut man sich die Entwicklung der zahnärztlichen OP-Lampen an, fällt einem über die Jahrzehnte eine starke Zunahme der Helligkeit (ausgedrückt in Lux) auf. Es müssen bestimmte ISO-Normen erfüllt werden und moderne Lampen sind in der Regel so grell, dass viele Patienten (insbesondere Kinder) eine Sonnenbrille aufgesetzt bekommen möchten.
Darüber hinaus erfreuen sich insbesondere im Zusammenhang mit Lupenbrillen auch Stirnlampen zunehmender Beliebtheit, weil der Strahlengang des Lichts annähernd koaxial zu dem des Sehens verläuft und so eine fast schattenfreie Beleuchtung der Zähne möglich ist. Schaut man in die Herstellerprospekte, scheinen diese sich mit immer höheren Luxzahlen überbieten zu wollen. Während eine OP-Lampe vielleicht 20.000 lx aufweist, gibt es Stirnlampen mit nominell bis zu 80.000 lx. Das Problem ist, dass es für Stirnlampen genauso wenig eine verbindliche Normierung gibt wie für Lupenbrillen. Die publizierten Helligkeitswerte sind in vielen Fällen zu hoch.
Im Rahmen einer Studie wurden Stirnlampen verschiedener Hersteller von der Eidgenössischen Materialprüfungsanstalt auf ihre Helligkeit hin untersucht. Fazit: Es war oft nur halb so viel Helligkeit messbar wie angegeben. Ferner nahm die Helligkeit bei den meisten Modellen ab, weil die LEDs sich mit der Zeit erhitzen und weil nicht gekühlte LEDs eine deutlich messbare Helligkeitsabnahme erfahren. Prinzipiell erleichtert zusätzliches Licht das Detailsehen im Mund, wie in einer Studie von Perrin et al. gezeigt wurde [Perrin et al., 2017].
In Bezug auf die visuelle Kariesdiagnostik gilt auch für Licht, dass zu starkes Licht zu einer Abnahme der diagnostischen Genauigkeit führt. Dies gilt sowohl für das Entdecken von Initialkaries als auch für Dentinkaries [Neuhaus et al., 2016]. Durch zu grelles Licht wird die Zahnoberfläche „überstrahlt“ und die Kontraste zwischen einer weißen Initialläsion und einer annähernd weißen Zahnoberfläche verschwinden. Soweit es die Kariesdiagnostik betrifft, scheinen Helligkeitswerte über 20.000 lx zu einer bestehenden OP-Lampe hinzu problematisch zu sein und zu einer Verschlechterung der diagnostischen Performance zu führen.
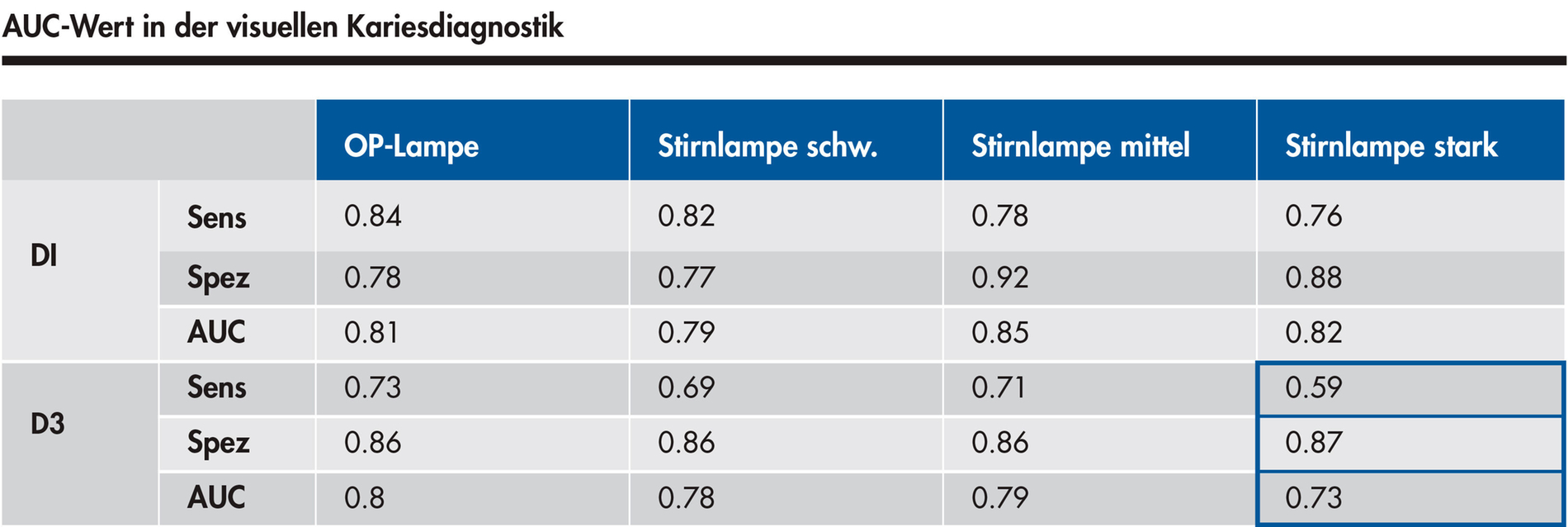
Was bislang noch nicht näher untersucht wurde, ist die Zusammensetzung des LED-Lichts in Bezug auf die Kariesdiagnostik. „Weiße“ LEDs weisen einen sehr hohen Anteil an blauem Licht auf. Während bei OP-Lampen am Stuhl die Leuchtdioden mit Phosphor bedampft sind, damit das abgestrahlte Licht auch einen ausreichenden Rotlicht-Anteil hat, haben die auf dem Markt befindlichen Stirnlampen-LEDs sowie die Dentalmikroskope meist einen ungefiltert hohen Blaulichtanteil. Es gibt Hinweise aus Tierversuchen auf Retinaschädigungen durch die Phototoxizität von exzessivem LED-Licht mit hohem Blaulichtanteil [Renard und Leid, 2016], aber arbeitsschutzrechtliche Empfehlungen gibt es bislang nicht.
Zähne trocknen – aber wann?
Für die visuelle Kariesdiagnostik wird gemeinhin empfohlen, die Zahnoberflächen mittels Druckluft zu trocknen. Dadurch wird der glänzende Speichelfilm verblasen oder getrocknet und die Zahnoberfläche wird ein Stück weit matter. Bestehende Initialläsionen weisen ein größeres Porenvolumen auf als gesunde Schmelzprismen. Das Trocknen entzieht diesen vergrößerten Schmelzporen Wasser und der Lichtbrechungsindex verändert sich, so dass white spots tatsächlich als kreideweiß erscheinen. Nach dem ICDAS-System (International Caries Detection and Assessment System) soll aber zusätzlich eine visuelle Diagnostik der ungetrockneten Oberfläche erfolgen. Der Grund liegt darin, dass Initialläsionen im Schmelz, die bereits im feuchten Zustand gut erkennbar sind, tiefer sind als solche, die erst nach dem Trocknen sichtbar werden. Dieser zweifache visuelle Durchgang durch die Zahnreihen benötigt nicht viel mehr Zeit – die unterschiedliche Tiefe der Initialläsionen sollte dann auch entsprechend in der Dokumentation vermerkt werden, wenn sich daraus unterschiedliche Behandlungs- und Prophylaxekonzepte ableiten.
Zahnreinigung vor der visuellen Kariesdiagnostik
Zu diesem Punkt gibt es einen Gelehrtenstreit ohne klaren Sieger. Klar ist, dass man Karies unter einem Plaquerasen nicht sehen kann. Die Zahnoberfläche muss also gereinigt sein, damit die Zahnoberflächen der visuellen Diagnostik überhaupt zugänglich sein können. Insofern macht die Empfehlung Sinn, dass vor der visuellen Diagnostik durch den Zahnarzt die Zähne gereinigt werden müssen. So hat es sich vielfach eingebürgert, dass beim zahnärztlichen Recall die Zahnreinigung vorgängig durch die ZMP, PA oder DH vorgenommen und anschließend der Zahnarzt für die Kontrolle gerufen wird.
Auf der anderen Seite ist ein Plaquerasen auch in gewisser Weise relevant für die Diagnose. Es werden chronisch vernachlässigte Areale aufgezeigt, bei denen das Kariesrisiko erhöht ist. Eine maturierte, klebrige Plaque wird mit „aktiven“ Schmelzläsionen assoziiert und unterstützt die visuelle Bestimmung der Läsionsaktivität [Nyvad et al., 1999]. Zudem ist ein weiteres Kriterium für eine „aktive“ Schmelzkaries, dass die Oberfläche rau ist und matt scheint [Nyvad et al., 1999]. Vergrößerungen erlauben ein besseres Erkennen der Oberflächentextur, so dass insbesondere im Zusammenspiel mit Lichtreflexen eine raue Oberfläche leichter von einer glatten unterschieden werden kann [Neuhaus et al., 2013]. Werden nun die Zahnoberflächen durch eine Schmelzpolitur im Rahmen einer Professionellen Zahnreinigung abschließend behandelt, geht der „Mattglanz“ als diagnostisches Kriterium verloren. Ein klinisch sinnvoller Kompromiss, der so auch in epidemiologischen Studien praktiziert wurde, kann darin bestehen, dass man den Patienten vor der Inspektion sich selber die Zähne putzen lässt. Auf den Arealen, die ohnehin chronisch schlecht geputzt sind, wird dabei mit hoher Wahrscheinlichkeit Plaque verbleiben. Die interdentale Reinigung muss dann eben, wenn nötig, der Zahnarzt selbst durchführen.
Fazit
Es gibt viele Gründe, weshalb die Zahnmedizin von Vergrößerungshilfen profitieren kann. Die Kariesdiagnostik gehört bedingt auch dazu. Vergrößerungen bis 2,5x erlauben älteren Zahnärzten, in etwa so gut zu sehen wie jüngere ohne Vergrößerungshilfe. Vergrößerungen ab circa 4,5x hingegen bergen das Risiko einer falsch positiven Diagnostik, also von Übertherapie. Zusätzliche Beleuchtung kann ab circa 20.000 lx zu einer Verschlechterung der visuellen Diagnostik führen, da die Kontraste zwischen Karies und Zahn abnehmen.
PD Dr. Klaus W. Neuhaus MMA MAS
1999:Diplom-Pianist, HfM Köln (Meisterklasse Prof. Pavel Gililov)
2003: Staatsexamen Universität Witten/Herdecke
2004: Dissertation Universität Witten/Herdecke
2004–2007: Assistent und wissenschaftlicher Mitarbeiter, Klinik für Parodontologie, Endodontologie und Kariologie, Universität Basel
2008–2018 Oberarzt an der Klinik für Zahnerhaltung, Präventiv- und Kinderzahnmedizin, ZMK Bern
2012: Master of Advanced Studies in Kariologie, Endodontologie und Kinderzahnmedizin, Universität Bern
2014: Habilitation im Fach Zahnerhaltung
Seit 2016: Präsident der Aktion Zahnfreundlich, Schweiz
Seit 2018: tätig in eigener Praxis in Herzogenbuchsee sowie Forschungs-Oberarzt an der Klinik für Parodontologie, Endodontologie und Kariologie, Universitäres Zentrum für Zahnmedizin Basel
Literaturliste
Eichenberger M, Perrin P, Neuhaus KW, Bringolf U, Lussi A. Influence of loupes and age on the near visual acuity of practicing dentists. J Biomed Opt. 2011 Mar;16(3):035003.
Eichenberger M, Perrin P, Ramseyer ST, Lussi A. Visual Acuity and Experience with Magnification Devices in Swiss Dental Practices. Oper Dent. 2015 Jul-Aug;40(4):E142-9
Eichenberger M, Biner N, Amato M, Lussi A, Perrin P. Effect of Magnification on the Precision of Tooth Preparation in Dentistry. Oper Dent. 2018 Sep/Oct;43(5):501-507.
Jasarevic E. Impact of different illumination conditions on visual caries detection with ICDAS. Dissertation, Universität Bern, 2016.
Koller E. Potential optical bias in visual caries detection systems. Master Thesis (MAS), Universität Bern, 2017.
Lussi A. Comparison of different methods for the diagnosis of fissure caries without cavitation. Caries Res. 1993;27(5):409-16.
Lussi A. Impact of including or excluding cavitated lesions when evaluating methods for the diagnosis of occlusal caries. Caries Res. 1996;30(6):389-93.
Neuhaus KW, Jost F, Perrin P, Lussi A. Impact of different magnification levels on visual caries detection with ICDAS. J Dent. 2015 Dec;43(12):1559-64.
Neuhaus KW, Perrin P, Lussi A. Substantial difference between declared and real magnification in medical loupes. Medical instrumentation 2013;1(1). Doi: 10.7243/2052-6962-1-2
Neuhaus KW, Jasarevic E, Lussi A. Impact of Different Illumination Conditions on Visual Caries Detection With ICDAS. Caries Res. 2015;49(6):633-6.
Neuhaus KW, Lussi A. Carious Lesion Diagnosis: Methods, Problems, Thresholds. Monogr Oral Sci. 2018;27:24-31.
Neuhaus KW, Ellwood R, Lussi A, Pitts NB. Traditional lesion detection aids. Monogr Oral Sci. 2009;21:42-51.
Neuhaus KW, Nyvad B, Lussi A, Jaruszewski L. Evaluation of perpendicular reflection intensity for assessment of caries lesion activity/inactivity. Caries Res. 2011;45(4):408-14.
Nyvad B, Machiulskiene V, Baelum V. Reliability of a new caries diagnostic system differentiating between active and inactive caries lesions. Caries Res. 1999 Jul-Aug;33(4):252-60.
Perrin P, Ramseyer ST, Eichenberger M, Lussi A. Visual acuity of dentists in their respective clinical conditions. Clin Oral Investig. 2014 Dec;18(9):2055-8.
Perrin P, Neuhaus KW, Lussi A. The impact of loupes and microscopes on vision in endodontics. Int Endod J. 2014 May;47(5):425-9.
Perrin P, Eichenberger M, Neuhaus KW, Lussi A. A Near Visual Acuity Test for Dentists. Oper Dent. 2017 Nov/Dec;42(6):581-586
Perrin P, Neuhaus KW, Eichenberger M, Lussi A. Influence of different loupe systems and their light source on the vision in endodontics. Swiss Dent J. 2019 Nov 11;129(11):922-928
Renard G , Leid J. The Dangers of Blue Light: True Story! J Fr Ophtalmol. 2016 May;39(5):483-8.


























