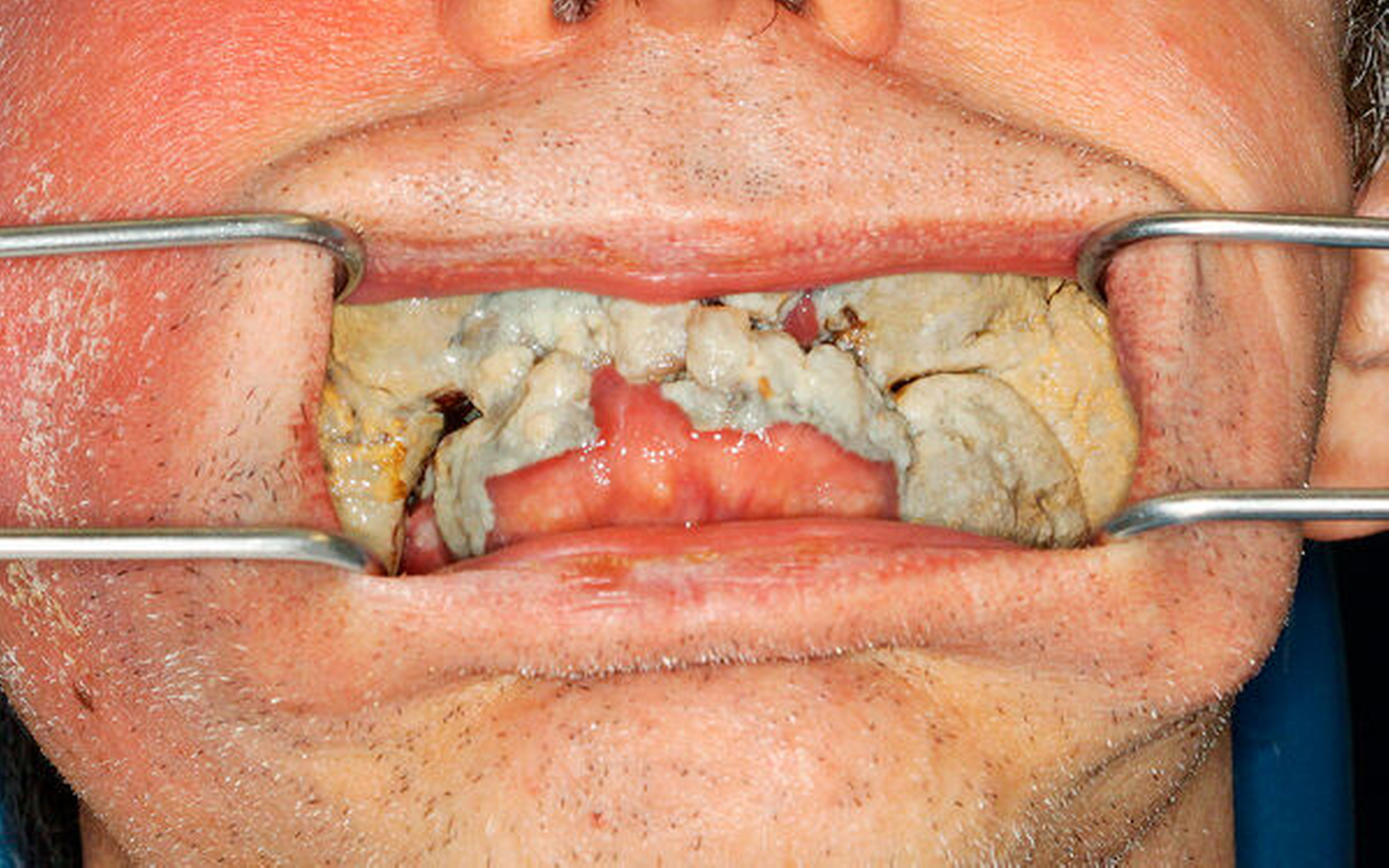
Massiver Zahnsteinbefund mit perforierendem Wangenabszess
Ein 57 Jahre alter Mann wurde uns an einem späten Nachmittag von seinem Hausarzt überwiesen. Der Patient stellte sich mit erhöhter Körpertemperatur (38,2 Grad Celsius) und einer deutlich geschwollenen rechten Wange vor. Am punctum maximum der Schwellung zeigte sich eine zentrale Ulzeration mit serösem Ausfluss und einer Umgebungsröte, die bis an den Kieferwinkel, den Nasenabhang, den Mundwinkel und nach infraorbital heranreichte (Abbildung 1).
Bei der en Face-Inspektion zeigte sich auch eine deutliche Schwellung der linken Wange, allerdings ohne die entzündliche Komponente. Der Hausarzt hatte aufgrund der deutlichen Ulzeration sowie der Spontanperforation die Verdachtsdiagnose eines malignen Geschehens oder einen exazerbierten Abszess vermutet. Die intraorale Untersuchung zeigte allerdings eine massive Ausbildung von Zahnstein in Ober- und Unterkiefer sowie eine Entzündung des gesamten Mundraums. Im Oberkiefer lagerte sich der überwiegende Teil des Zahnsteins vestibulär an, der im Endeffekt auch die Entzündung der rechten Wange mit folgendem Abszess und Perforation hervorrief (Abbildungen 2, 3, 4). Der Zahnstein war in palato-vestibulärer Richtung teilweise bis zu drei mal breiter als die Molaren. Im Unterkiefer war vor allem ein Massenzuwachs lingual der Unterkieferfrontzähne zu beobachten. Die Zunge war dadurch dauerhaft nach posterior verlagert, was zu kloßiger Sprache und einer Entzündung des gesamten Mundbodens führte (Abbildung 5).
In der Folge leiteten wir eine intravenöse Antibiotikatherapie ein und nahmen den Patienten stationär auf. In der durchgeführten Röntgendiagnostik (OPG) zeigte sich eine Aufhellung im gesamten zahntragenden Bereich beider Kiefer (Abbildung 6). Die Beurteilung der Zahnwurzeln stellte sich mitunter als sehr schwierig dar.
Am folgenden Tag sanierten wir den Patienten in Intubationsnarkose. Die Zahnsteinanteile wurden sukzessiv entfernt (Abbildung 7). Trotz des Versuchs, möglichst viele Zähne vom Zahnstein zu trennen und sie zu erhalten, zeigten sich insgesamt 19 Zähne als nicht mehr erhaltungswürdig (Abbildung 8). In vielen Fällen stellte sich nur noch marginaler oder gar kein Kontakt mehr zum Alveolarknochen dar. Lediglich im zweiten Quadranten konnten vier Zähne erhalten werden (23, 26, 27, 28) (Abbildung 9). Sämtliche Schleimhäute waren entzündlich verändert und zum Teil mit eitrigen und serösen Auflagerungen belegt (Abbildung 10). Zusätzlich wurde ein Abstrich des Ulkus von intraoral genommen. Hier zeigte sich nach Bebrütung ein Staphylokokkus capitis, welcher gegen die Reserveantibiotika Vancomycin, Teicoplanin und Fosfomycin resistent war.
Der Patient konnte nach drei Tagen entlassen werden und wurde prothetisch vom Hauszahnarzt weiter versorgt.
Diskussion
Unterschieden wird der supra- vom subgingivalen Zahnstein. Der subgingivale Zahnstein ist als „Konkrement“ bekannt, akkumuliert vergleichbar langsam, haftet dafür aber sehr stark an der Zahnhartsubstanz an. Der supragingivale Zahnstein ist deutlich vermehrt an den Stellen der Bezahnung aufzufinden, wo die Ausführungsgänge der exokrinen Speicheldrüsen nach intraoral münden. Häufigste Prädilektionsstellen sind daher die linguale Fläche der Unterkieferfrontzähne (Glandula submandibularis und sublingualis) und die vestibuläre Fläche der Oberkiefermolaren (Glandula parotis) [Roberts-Harry und Clerehugh, 2000].
Zahnstein entsteht über viele Zwischenstufen, beginnend mit dem dünnen Pellikel, das sich bereits kurz nach dem Zähneputzen anlagert und die Grundlage für weitere Retentionsvorgänge bildet. Bakterien und Nahrungsreste lagern sich an, Polysaccharide, Epithelzellen und Speichelbestandteile sind weitere anhaftende Elemente. Bleiben diese Bestandteile über 24 bis 48 Stunden unberührt, wird die entstandene Plaque zunehmend wasserunlöslich und verhärtet sich. Durch Mineralien aus dem Speichel beginnt der Mineralisierungsprozess, der schließlich im Zahnstein mündet.
Die Annahme, dass sowohl Gingivitis als auch Parodontitis hauptsächlich durch Zahnstein bedingt werden, wurde mittlerweile von zahlreichen Wissenschaftlern widerlegt. In vivo-Studien zeigten, dass der Biofilm und seine mikrobielle Zusammensetzung den ausschlaggebenden Faktor für diese Erkrankungen darstellen [Mandel und Gaffar, 1986].
Die Entstehung von Zahnstein ist ein komplexes und multifaktorielles Geschehen. Neben Faktoren, die eine erhöhte bakterielle Plaqueretention zur Folge haben [Suomi et al., 1971] spielen biochemische Prozesse wie die Zusammensetzung des Speichels und der Sulkusflüssigkeit eine übergeordnete Rolle [Slomiany et al., 1971]. Darüber hinaus sind Vorgänge von Bedeutung, die im Zusammenhang mit Plaque-produzierenden Mikroorganismen stehen [Ennever et al., 1979], und nicht zuletzt sind die Ernährungsgewohnheiten zu nennen, die Art und Menge des zur Verfügung stehenden Substrats für die Keime beeinflussen [Hidaka & Oishi, 2007].
Das Ausbilden von Zahnstein zeigt eine große interindividuelle Breite in der Bevölkerung. In mehreren Studien konnte gezeigt werden, dass es Menschen gibt, die trotz sehr guter Mundhygiene und regelmäßiger Reinigung zu deutlich erhöhter Plaque-Akkumulation neigen [Fons-Badal et al., 2020].
Im vorliegenden Fall war unzureichende Mundhygiene zwar unumstritten die Ursache für die massive Zahnsteinentwicklung, darüber hinaus allerdings auch eine aggressive Form der Neubildung zu vermuten. Patienten mit extremer Zahnsteinausbildung müssen über diesen Umstand aufgeklärt und auf die Notwendigkeit höher frequentierter Kontrolltermine hingewiesen werden.
Eine aktuelle Studie konnte zeigen, dass einige Faktoren einen signifikanten Einfluss auf die Geschwindigkeit der Zahnsteinentwicklung hatten. Neben Parodontitisbefunden spielen Zahnfehlstellungen, der Gehalt an Harnsäure und Phosphor im Speichel sowie die vermehrte Anwesenheit von Streptokokkus mutans dabei eine Rolle [Fons-Badal et al., 2020]. Die Studie belegte weiterhin, dass Parodontitis im Stadium III und IV sowie Grad C statistisch signifikant mit der vermehrten Ausbildung von Zahnstein im Zusammenhang steht. Patienten mit schneller und mengenmäßig hoher Zahnsteinakkumulation sehen sich demnach mit deutlich schwereren Verläufen konfrontiert. Ein weiterer Risikofaktor für eine vermehrte Zahnsteinbildung könnte ein erhöhter Gehalt an Kalzium im Sekret der Glandula submandibularis sein [Mandel, 1974].
Die Entfernung fast aller Zähne, wie im vorliegenden Fall, ist nicht die Regel. Allerdings kann bei aggressivem Befall die Zahnhartsubstanz wie auch der Zahnhalteapparat so stark geschädigt sein, dass ein Erhalt der Zähne nicht mehr möglich ist.
Das Auftreten eines Staphylokokkus-Stamms mit Resistenzen gegen absolute Reserveantibiotika ist bemerkenswert und unterstreicht den engen Zusammenhang zwischen pathologischen Mikroorganismen und der Ausbildung von Zahnstein.
Staphylokokkus capitis gehört zur residenten Flora der Haut und gilt als opportunistisch pathogen, wenn das Wirtsimmunsystem geschwächt ist. Der ansonsten ubiquitär dermal vorkommende Mikroorganismus wurde bei geschwächter Abwehrlage bereits als auslösendes Bakterium bei Neugeborenensepsis, Meningitis und Endokarditis isoliert [Cameron et al., 2015].
Fazit für die Praxis
Die Ausbildungsgeschwindigkeit von Zahnstein unterliegt einer großen interindividuellen Breite. Aufgabe des Zahnarztes ist es, Patienten mit einem erhöhten Risikoprofil klinisch zu identifizieren und sie den entsprechenden Maßnahmen in adäquaten Zeitintervallen zuzuführen.
Da die Verhärtung der Plaque bereits nach einem Tag ohne Zähneputzen zunimmt, sind besonders Patienten mit schneller Zahnsteinentwicklung gefährdet, bei mangelnder Mundhygiene bleibende Schäden an Zahnhartsubstanz und Zahnhalteapparat zu erleiden.
Zahnsteinentwicklung ist eng mit Parodontitisbefunden verbunden. Wenn bei einem Patienten supragingival eine erhöhte Neigung zu Zahnsteinbildung beobachtet wird, empfiehlt sich im Weiteren auch eine Parodontitisdiagnostik.
Im aktuellen Fall war der Keim als einziger nachweisbar. Wir vermuten, dass die vergleichbar lange „Bebrütung“ des Keims in der Mundhöhle und die persistente Entzündung des gesamten Teguments zur Entwicklung des Staphylokokkus beigetragen hat. Glücklicher weise waren die gängigen Antibiotika, die von uns in der Regel empirisch angewendet werden (Ampicillin + Sulbactam), wirksam. Somit konnte der Patient additiv zur chirurgischen Sanierung suffizient antibiotisch therapiert werden.
Dr. Nils Heim
Abteilung für Mund-, Kiefer- und Plastische Gesichtschirurgie des Universitätsklinikums Bonn, Direktor: Prof. Dr. Dr. F.-J. Kramer
Sigmund-Freud-Str. 25
53127 Bonn
Dr. Dr. Valentin Wiedemeyer
Abteilung für Mund-, Kiefer- und Plastische Gesichtschirurgie des Universitätsklinikums Bonn
Sigmund-Freud-Str. 25
53127 Bonn
Benedict Jürgensen
Klinik und Poliklinik für Mund-, Kiefer- und Plastische Gesichtschirurgie Universitätsklinikum Bonn
Assistenzarzt der Klinik
Venusberg – Campus 1, Haus 11, 2. OG, 53127 Bonn
Prof. Dr. Dr. Franz-Josef Kramer
Abteilung für Mund-, Kiefer- und Plastische Gesichtschirurgie des Universitätsklinikums Bonn
Sigmund-Freud-Str. 25
53127 Bonn
Literaturliste
1. Roberts-Harry EA, Clerehugh V. Subgingival calculus: where are we now? A comparative review. Journal of dentistry. 2000;28:93–102.
2. Mandel ID, Gaffar A. Calculus revisited. A review. J. Clin. Periodontol. 1986;13:249–257.
3. Suomi JD, Greene JC, Vermillion JR, Doyle J, Chang JJ, Leatherwood EC. The effect of controlled oral hygiene procedures on the progression of periddontal disease in adults: Results after third and final year. J. Periodontol. 1971;42:152–160.
4. Slomiany A, Slomiany B, Mandel I. Lipid composition of human parotid saliva from light and heavy dental calculus-formers. Arch. Oral Boil. 1981;26:151–152.
5. Ennever J, Vogel J, Boyan-Salyers B, Riggan, L. Characterization of Calculus Matrix Calcification Nucleator. J. Dent. Res. 1979;58:619–623.
6. Hidaka S, Oishi A. An in vitro study of the effect of some dietary components on calculus formation: Regulation of calcium phosphate precipitation. Oral Dis. 2007;13:296–302.
7. Fons-Badal C, Fons-Font A, Labaig-Rueda C, Solá-Ruiz MF, Selva-Otaolaurruchi E, Agustín-Panadero R. Analysis of Predisposing Factors for Rapid Dental Calculus Formation. J Clin Med. 2020;20:9(3)
8. Mandel ID. Biochemical aspects of calculus formation. II. Comparative studies of saliva in heavy and light calculus formers. J. Periodontal Res. 1974;9:211–222.