Idiopathische Osteomyelitis führt zur Kontinuitätsresektion der Mandibula
Eine 56-jährige Patientin stellte sich initial in unserer MKG-chirurgischen Ambulanz mit einer HNO-ärztlichen Überweisung und der Bitte um Abklärung eines entzündlichen Fokus im Bereich des rechten Unterkiefers vor. Sie gab an, seit sieben Jahren unter chronisch-rezidivierenden Beschwerden im Bereich der rechten Gesichtshälfte zu leiden. Diese gingen einher mit Einschränkungen der Mundöffnung und schmerzhaften Schwellungszuständen. Die erhebliche Beschwerdesymptomatik habe in der Vergangenheit zu regelmäßigen und gehäuften Krankmeldungen zum Teil über mehrere Wochen geführt. Die durch den Hauszahnarzt eingeleiteten Behandlungsmaßnahmen, die dem Therapieregime einer CMD-Symptomatik entsprechen (okklusale Schienentherapie und physiotherapeutische Behandlungsmaßnahmen), zeigten keine Besserung des Beschwerdebildes.
Allgemeinanamnestisch lagen eine arterielle Hypertonie, eine Hypothyreose sowie eine hormonell und operativ behandelte Endometriose (Unterleibserkrankung) vor. Zum Zeitpunkt der Erstvorstellung imponierte eine bis nach submandibulär reichende, ödematöse Schwellung der rechten Parotisregion. Die Schneidekantendifferenz war schmerzhaft auf 22 mm eingeschränkt. Die klinisch orientierte, funktionelle Untersuchung der Kaumuskulatur zeigte einen Druckschmerz des Muskulus masseter, des Muskulus pterygoideus medialis und des Muskulus temporalis rechts. Der Zahnstatus des prothetisch und konservierend suffizient versorgten Gebisses war gepflegt; die Mundschleimhaut rosig, durchfeuchtet und intakt. Im Bereich des sensiblen Innervationsgebiets des rechten Nervus mentalis imponierte eine circa 2 cm2 große Hypästhesie im Sinne eines positiven Vincent-Symptoms. Der Status der übrigen sensiblen Trigeminusäste war regelrecht, dies galt auch für die motorischen Anteile des die mimische Muskulatur innervierenden Nervus facialis.
Im Rahmen der Fokussuche erfolgte neben der Anfertigung eines Orthopantomogramms (Abbildung 1) die Durchführung einer Computertomografie (Abbildung 2). Der röntgenologische Befund dokumentierte osteomyelitisch typische CT-morphologische Korrelate wie eine inhomogene großflächige Sklerosierung des rechten Unterkiefers mit zystisch-osteolytischen Veränderungen. Bei klinisch und radiologisch dringendem Verdacht auf eine primär chronische Osteomyelitis des Unterkiefers wurde nach Erörterung der Therapiemöglichkeiten mit der Patientin die Indikation zur zeitnahen operativen Intervention gestellt.
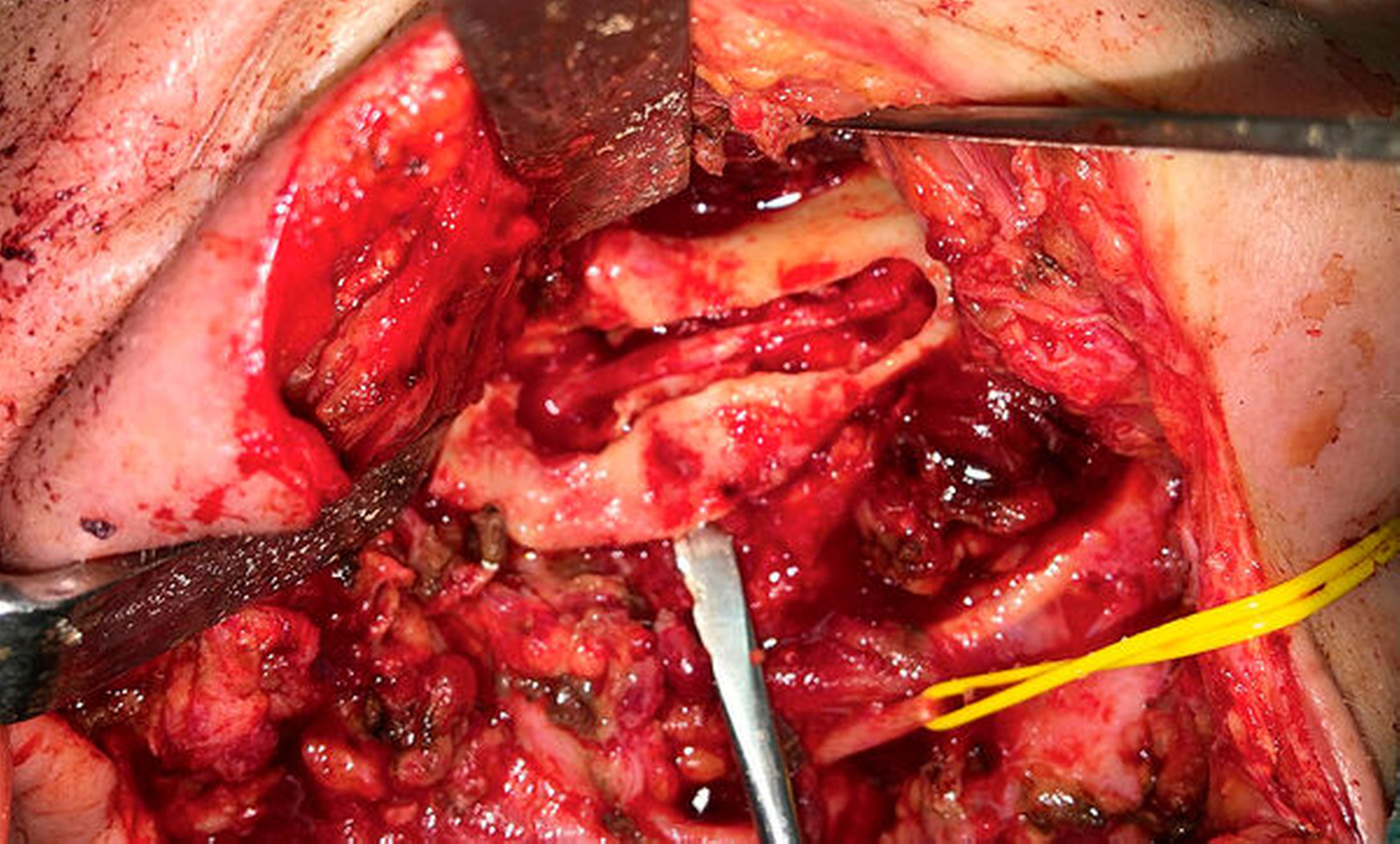
Über einen submandibulären, nach kranial bis präaurikulär extendierten Zugang erfolgte die Exploration des rechten Unterkiefers vom Kieferwinkel bis zum Proc. condylaris. Abbildung 3 zeigt die rechte Kieferwinkelregion mit dem bereits freigelegten Nervus alveolaris inferior. Eindrücklich kommen die zystisch-osteomyelitisch affektierten Lakunen im Bereich der äußeren Kortikalis zur Darstellung. Nach erfolgter Lateralisation des Nervus alveolaris inferior wurde die Kontinuitätsresektion des Unterkiefers von regio 048 bis unmittelbar unterhalb des Proc. condylaris vorgenommen (Abbildung 4). Die histopathologische Aufarbeitung des Resektats bestätigte die Diagnose einer chronischen Osteomyelitis. Der entstandene knöcherne Defekt wurde unmittelbar mit einem an die Facialisgefäße mikrochirurgisch-reanastomosierten Fibula-Transplantat rekonstruiert (Abbildung 5).
Nach komplikationslosem postoperativem Verlauf kam es zu einer sukzessiven Verbesserung der klinischen Beschwerdesymptomatik, so dass die Patientin am zehnten postoperativen Tag bei sanatio per primam intentionem in die ambulante Weiterbehandlung entlassen werden konnte. Zur Verbesserung der Nervenregeneration wurde Vitamin B12 oral substituiert. Bei der letztmaligen ambulanten Wiedervorstellung sechs Monate postoperativ zeigten sich reizfreie extraorale Wundverhältnisse (Abbildung 6), eine Regredienz der Vincent-Symptomatik sowie eine deutliche Verbesserung der SKD auf einen Wert von 38 mm bei subjektiver Beschwerdefreiheit.
Diskussion
Der vorliegende Fall demonstriert die Notwendigkeit zur regelmäßigen Überprüfung der Arbeitsdiagnose, des Therapiefortschritts und gegebenenfalls auch die erneute Durchführung einer weiterführenden Diagnostik. Insbesondere bei ausbleibendem Therapieerfolg ist eine erneute diagnostische Abklärung erforderlich, um den Krankheitsverlauf zu überprüfen oder die Therapie individualisiert anzupassen. Im vorliegenden Fall zeigte sich hierbei eine andere Erkrankung als zunächst angenommen, da die Auswirkungen der Osteomyelitis das zunächst vermutete Krankheitsbild darstellten. Wie sich jedoch herausstellte, bestand die Ursache der CMD-Symptomatik in der fortschreitenden (fortgeschrittenen?) Osteomyelitis.
Der Begriff der Osteomyelitis wird definiert als eine progressive Entzündung des Knochens und Knochenmarks und betrifft im Bereich des Gesichtsschädels vorwiegend die zahntragenden Kieferanteile. Formalterminologisch wird der Begriff der Osteomyelitis im klinischen Alltag oftmals nicht ganz korrekt verwendet, da Knochenentzündungen zumeist Mischformen einer Infektion der Kompakta (Ostitis) und des Knochenmarks (Osteomyelitis) beinhalten. Da der Terminus der Osteomyelitis jedoch im klinischen Gebrauch ungeachtet der exakten Lokalisation der knöchernen Entzündung in Kompakta und/oder Spongiosa Anwendung findet und sich hieraus keine Unterschiede in Bezug auf Ätiologie und Therapie ergeben, soll im Folgenden der Terminus „Osteomyelitis“ im Sinne eines Oberbegriffs für eine Knochenentzündung verwendet werden.
Die Pathogenese der Kieferosteomyelitis ist multifaktoriell und kann Folge von Traumen, chirurgischen Interventionen, Parodontopathien und Infektionen des Endodonts sein. Die Behandlung gilt als anspruchsvoll und langwierig. In der Vergangenheit hat es zahlreiche Bemühungen gegeben, eine einheitliche Klassifikation der Osteomyelitiden zu finden, so dass nicht weniger als elf verschiedene Klassisifikationssysteme beschrieben worden sind [Baltensperger et al., 2004]. Die bis heute gebräuchlichste Klassifikation geht auf Eyrich et al. [Eyrich et al., 2003] zurück, die sowohl das klinische Erscheinungsbild wie den zeitlichen klinischen Verlauf berücksichtigt.
Hierbei wird zwischen den Formen der akuten Osteomyelitis, der sekundär chronischen Osteomyelitis (SCO) sowie der primär chronischen Osteomyelitis unterschieden (PCO). Definitionsgemäß werden die akute Osteomyelitis und die SCO durch ihren zeitlichen Verlauf differenziert. Eine symptomatische, akute Osteomyelitis geht bei Persistenz des klinischen Beschwerdebildes über einen Zeitraum von vier Wochen in eine SCO über. Es handelt sich also um die gleiche Erkrankung in einem unterschiedlichen zeitlichen Stadium mit der gleichen Ätiologie.
Die SCO, in der Literatur auch mit dem Synonym chronisch-eitrige Osteomyelitis tituliert, ist gekennzeichnet durch eine ausgeprägte, floride Entzündungssymptomatik mit putridem, fistulierendem und/oder sequestrierendem Verlauf. Die Ursache liegt überwiegend in der bakteriellen Invasion und Kontamination des Knochens mit einem klar definierten Keimspektrum begründet, oftmals als Folge chirurgischer Eingriffe oder von Traumen. Demgegenüber ist die PCO gekennzeichnet durch eine nicht-eitrige Entzündung unbekannter Ätiologie, die zunächst ohne schwere Krankheitssymptome abläuft.
Von den beschriebenen Formen der Osteomyelitis abzugrenzen sind die Osteoradionekrose und die Antiresorptiva-induzierte Osteomyelitis, die primär auf eine medikamentös oder strahleninduzierte veränderte Knochenphysiologie mit konsekutiver Immunkompromittierung zurückzuführen sind. Folglich sind diese beiden Krankheitsbilder nomenklatorisch nicht als chronische Osteomyelitiden zu betrachten [Baltensperger und Eyrich, 2009].
Die Ätiologie der primär-chronischen Osteomyelitis ist in 80 Prozent der Fälle unklar [Julien Saint Amand et al., 2009]. Ein Zusammenhang mit dem Auftreten der PCO nach zahnärztlichen Eingriffen wird kontrovers diskutiert. Im vorliegenden Patientenfall war kein dentogener Fokus ersichtlich oder eine stattgehabte zahnärztliche Therapie ätiologisch in Zusammenhang mit der Entwicklung der Kieferosteomyelitis zu bringen. Dies korreliert ebenfalls mit einer adäquaten Mundhygiene bei gepflegtem Zahnstatus. Zahlreiche Studien beschäftigten sich mit möglichen Ätiologien für die Ausbildung einer PCO. Hierbei wurden vaskuläre Ursachen im Rahmen von Mikrozirkulationsstörungen bei einer Endarteriitis obliterans, bei Autoimmunerkrankungen oder bei einer muskulären Hyperaktivität diskutiert [Bevin et al., 2008; Groot et al., 1992]. Fleuridas et al. [2004] und Baltensperger et al. [2004] zeigten in Patienten, die an einem SAPHO-Syndrom litten, eine erhöhte Prävalenz für das Auftreten einer PCO. Hieraus lässt sich die Empfehlung ableiten, bei einer diagnostizierten PCO eine zusätzliche Erkrankung am SAPHO-Syndrom auszuschließen. Das Akronym SAPHO beschreibt den klinischen Symptomkomplex einer seltenen Variante der Psoriasis-Arthritis bestehend aus Synovitis, Akne, Psoriasis pustolosa, Hyperostosis und Ostitis. Bei einer gleichzeitigen Infektion mit dem HI-Virus werden häufig schwere Verläufe beobachtet.
Grundsätzlich ist das Outcome bei an einer PCO erkrankten Patienten deutlich schlechter als bei der SCO [Julien Saint Amand et al., 2009]. Eine radikale chirurgische Therapie mit einer segmentalen Resektion der von der Osteomyelitis affektierten Areale erscheint deutlich effektiver als konservative Behandlungsansätze [Slough et al., 2008]. In diesem Kontext ist eine unmittelbare, knöcherne Rekonstruktion der zum Teil ausgeprägten Resektionsdefekte mit mikrochirurgisch reanastomosierten, freien knöchernen Transplantaten [Rustemeyer et al., 2019; Abe et al., 2011] sehr erfolgreich. In therapierefraktären Fällen sind zum Teil gute Ergebnisse bei der medikamentösen Therapie mit Bisphosphonaten [Otto et al., 2015; Montonen et al., 2001], dem monoklonalen Antikörper Denosumab [Otto et al., 2018] oder dem Peptidhormon Calcitonin [Jones et al., 2005] dokumentiert. Bei einer PCO im Rahmen eines SAPHO-Syndroms scheinen Biologika aus der Gruppe der TNF-alpha-Inhibitoren sowie das Folsäure-Analogon Methotrexat vielversprechend [Mari et al., 2004].
Unabhängig von den beschriebenen und vorwiegend experimentellen Therapieansätzen ist das Krankheitsbild der PCO nach wie vor ätiologisch unklar und bedarf einer umfangreichen und frühen chirurgischen Intervention, um schwere Krankheitsverläufe zu verhindern. Oftmals erfolgt, wie im vorliegenden Fall, die Diagnosestellung aufgrund des Fehlens von eindeutigen klinischen Zeichen, wie sie bei der akuten und bei der sekundär-chronischen Osteomyelitis zu finden sind, erst in einem fortgeschrittenen Krankheitsstadium, so dass ausgedehnte und radikale Resektionen erforderlich werden. Eine funktional-rehabilitierende Therapie macht in vielen Fällen aufwendige Rekonstruktionen mit mikrovaskulären Transplantaten erforderlich.
Fazit für die Praxis
Die Osteomyelitiden werden unterschieden in eine akute, eine sekundär chronische und eine primär chronische Form.
Die Ätiologie der primär chronischen Osteomyelitis (PCO) ist nach wie vor weitgehend unklar.
Eine länger als vier Wochen persistierende Osteomyelitis wird als sekundär chronische Osteomyelitis (SCO) bezeichnet.
Die Therapie beinhaltet primär die chirurgische Resektion osteomyelitisch affektierter Areale sowie eine Langzeitantibiose.
Viele Krankheitsverläufe sind langwierig und therapieresistent.
Die primär chronische Osteomyelitis hat ein schlechteres Outcome als die sekundär chronische Form.
Es besteht eine Assoziation der PCO mit dem SAPHO-Syndrom.
In therapierefraktären Fällen können Antiresorptiva, Biologika oder Immunmodulatoren zum Einsatz kommen.
Das radikale chirurgische Vorgehen macht oftmals aufwendige Rekonstruktionen mit mikrovaskulären Transplantaten erforderlich.
Literaturliste
[1] M. Baltensperger, K. Grätz, E. Bruder, R. Lebeda, M. Makek, G. Eyrich. Is primary chronic osteomyelitis a uniform disease? Proposal of a classification based on a retrospective analysis of patients treated in the past 30 years. J Cranio-Maxillofac Surg, 32 (1) (2004), pp. 43-50
[2] G.K.H. Eyrich, M.M. Baltensperger, E. Bruder, K.W. Graetz. Primary chronic osteomyelitis in childhood and adolescence: A retrospective analysis of 11 cases and review of the literature. J Oral Maxillofac Surg, 61 (5) (2003), pp. 561-573
[3] M. Baltensperger, G. Eyrich. Osteomyelitis of the jaws: definition and classification in osteomyelitis of the jaws. Springer-Verlag, Berlin (2009)
[4] Julien Saint Amand M, Sigaux N, Gleizal A, Bouletreau P, Breton P. Chronic osteomyelitis of the mandible: A comparative study of 10 cases with primary chronic osteomyelitis and 12 cases with secondary chronic osteomyelitis. J Stomatol Oral Maxillofac Surg. 2017 Dec;118(6):342-348. doi: 10.1016/j.jormas.2017.08.006. Epub 2017 Aug 18. PMID: 28823691.
[5] C.R. Bevin, C.Y. Inwards, E.E. Keller Surgical management of primary chronic osteomyelitis: a long-term retrospective analysis. J Oral Maxillofac Surg, 66 (10) (2008), pp. 2073-2085
[6] R.H. Groot, J.P. van Merkesteyn, J.J. van Soest, J. Bras. Diffuse sclerosing osteomyelitis (chronic tendoperiostitis) of the mandible An 11-year follow-up report. Oral Surg Oral Med Oral Pathol, 74 (5) (1992), pp. 557-560
[7] C.M. Slough, B.M. Woo, B.A. Ueeck, M.K. Wax. Fibular free flaps in the management of osteomyelitis of the mandible. Head Neck, 30 (11) (2008), pp. 1531-1534
[8] Rustemeyer J, Siegmund BJ, Okcu Y, Busch A. Total mandibular reconstruction following diffuse sclerosing osteomyelitis. Oral Maxillofac Surg. 2019 Mar;23(1):95-99. doi: 10.1007/s10006-018-0731-9. Epub 2018 Oct 16. PMID: 30327981.
[9] Abe T, Kitada H, Sato J, Yamazaki Y, Notani K, Yamaguchi T, Kitagawa Y (2011) Successful total mandibular reconstruction using a fibular graft with long-term follow-up: a case report. Asian J Oral Maxillofac Surg 23:196–200
[10] Otto S, Troeltzsch M, Burian E, Mahaini S, Probst FA, Pautke C, Ehrenfeld M, Smolka W (2015) Ibandronate treatment of diffuse sclerosing osteomyelitis of the mandible: pain relief and insight into pathogenesis. J Craniomaxillofac Surg 43:1837–1842
[11] Otto S, Burian E, Troeltzsch M, Kaeppler G, Ehrenfeld M (2018) Denosumab as a potential treatment alternative for patients suffering from diffuse sclerosing osteomyelitis of the mandible - rapid communication. J Craniomaxillofac Surg 46:534–537
[12] M. Montonen, E. Kalso, L. Pylkkären, B.-M. Lindströrm, C. Lindqvist. Disodium clodronate in the treatment of diffuse sclerosing osteomyelitis (DSO) of the mandible. Int J Oral Maxillofac Surg, 30 (4) (2001), pp. 313-317
[13] J. Jones, T.R. Amess, P.D. Robinson. Treatment of chronic sclerosing osteomyelitis of the mandible with calcitonin: a report of two cases. Br J Oral Maxillofac Surg, 43 (2) (2005), pp. 173-176
[14] A. Marí, A. Morla, M. Melero, R. Schiavone, J. Rodríguez. Diffuse sclerosing osteomyelitis (DSO) of the mandible in SAPHO syndrome: a novel approach with anti-TNF therapy. Systematic review. J Cranio-Maxillofac Surg, 42 (8) (2014), pp. 1990-1996









