Enukleation einer nasopalatinalen Zyste und Augmentation des knöchernen Defekts
Ein 64-jähriger Patient stellte sich zur Enukleation einer zystischen Läsion in der Maxilla, mit Beteiligung nach enoral durch einen zentral im anterioren Gaumen gelegenen Fistelgang, vor. Der Patient trägt im Oberkiefer eine Modellgussprothese, die Oberkieferfront fehlt. Bereits Ende 2024 war alio loco ein Entfernungsversuch unternommen worden, der jedoch aufgrund einer starken intraoperativen Blutung abgebrochen werden musste.
Die geplante Operation erfolgte unter Intubationsnarkose – mit postoperativem stationärem Aufenthalt zur Blutungskontrolle und Schwellungsprophylaxe. Eine Verbandsplatte zur postoperativen Anpassung und Eingliederung war im Vorfeld abgeformt und hergestellt worden. Zum Zeitpunkt der Vorstellung dehnte sich die Zyste transversal 16 mm, sagittal 9 mm und axial 12 mm aus, wie in der präoperativ alio loco angefertigten radiologischen Bildgebung erkennbar ist (Abbildungen 2 und 3).
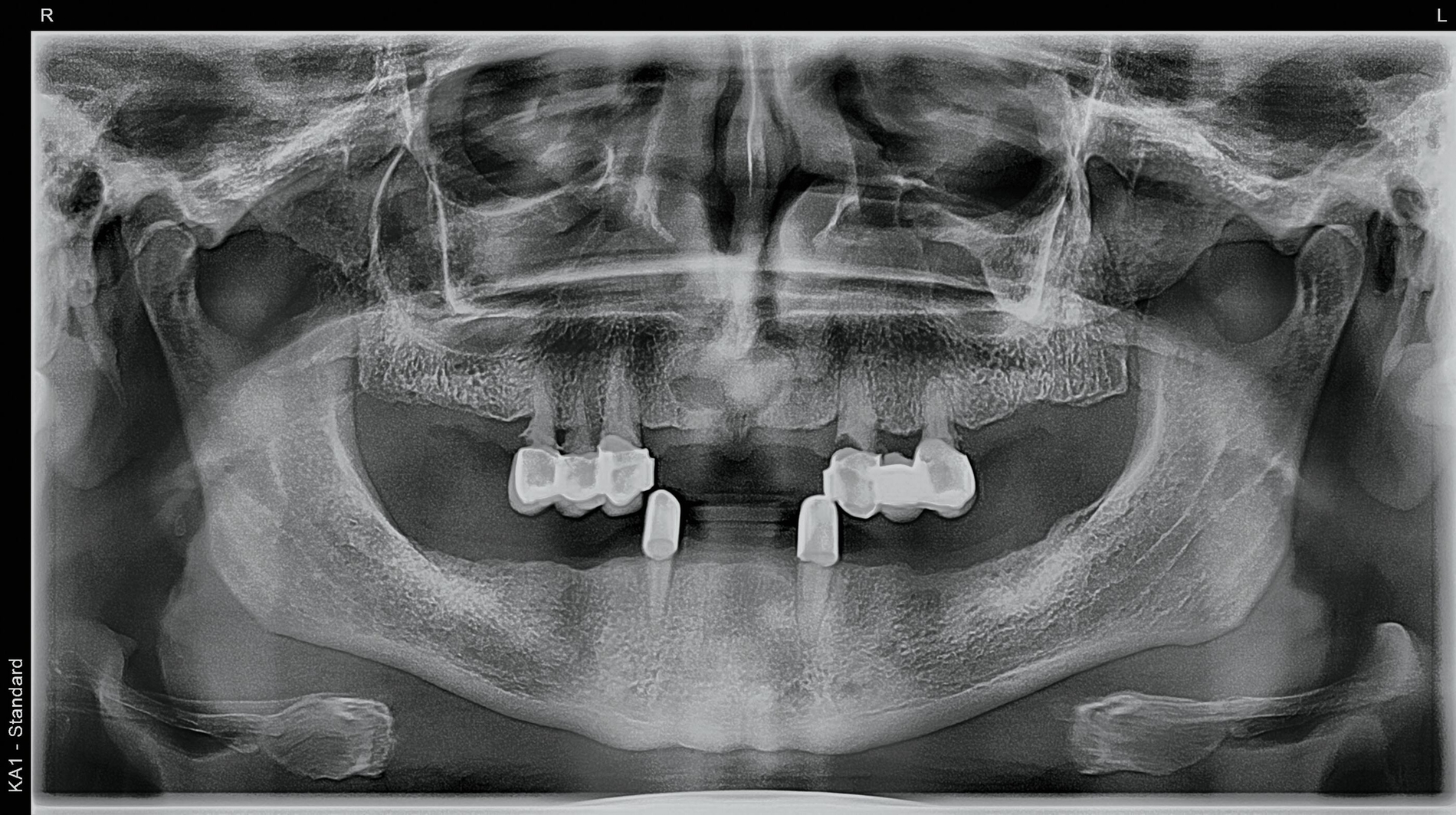
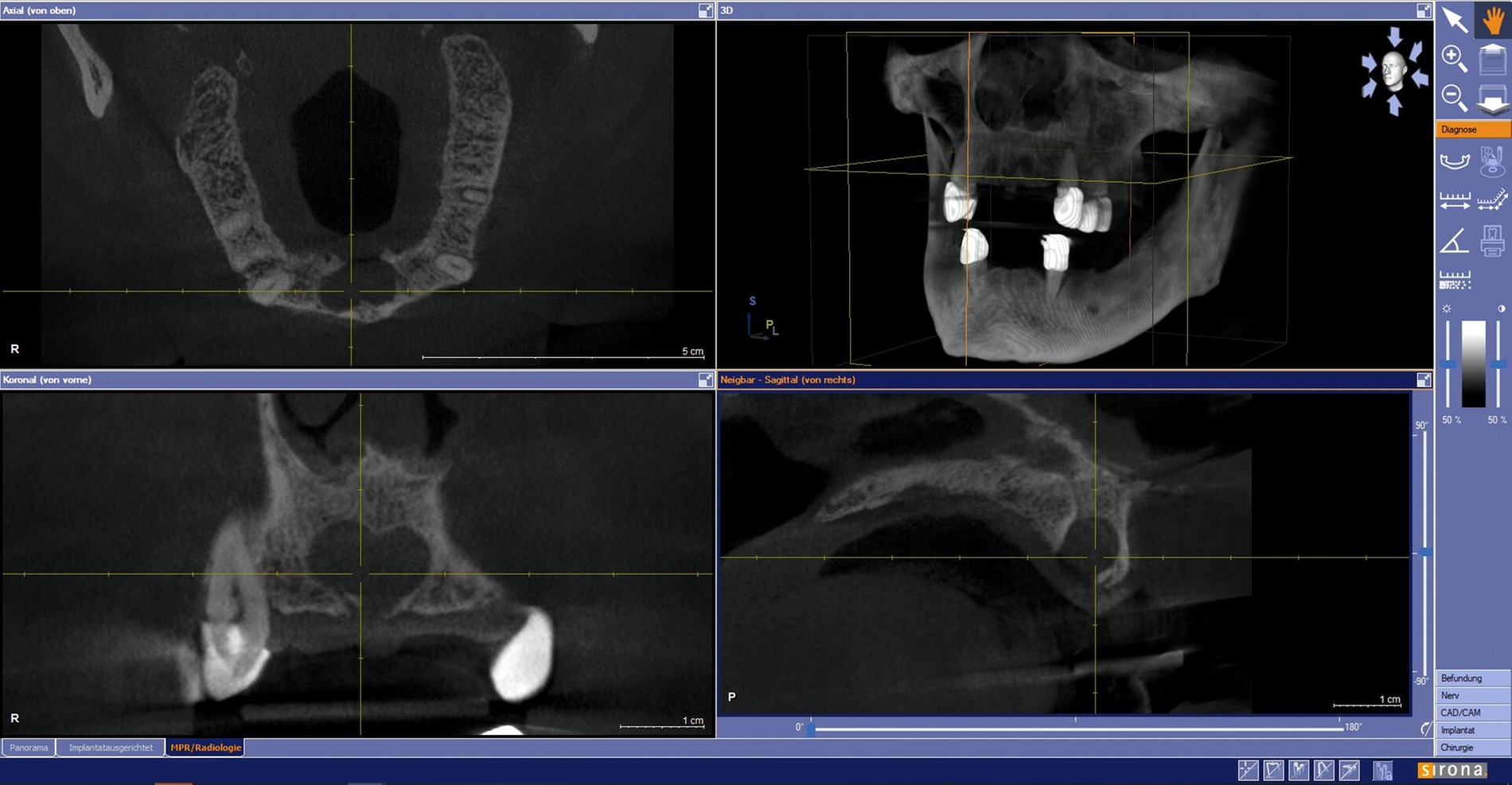
Therapie
Die Schnittführung verlief von dem rechten bis zum linken Tuber maxillae. Durch vorsichtiges, streng subperiostales Abpräparieren der Schleimhaut des harten Gaumens konnte eine gute Übersicht über den Befund gewährt werden (Abbildung 4). Nach Enukleation der Zyste zeigte sich der Defekt vollständig knöchern begrenzt, eine Perforation zur Nase lag nicht vor (Abbildung 5).
Um die Regeneration zu beschleunigen, wurde der Defekt mit Corticalis Granulat der Größe 0,212–0,85 mm (DIZG, Berlin, Deutschland), gemischt mit autologem Knochen und PRGF, hergestellt nach der ENDORET® Technologie (BTI Deutschland GmbH, Pforzheim, Deutschland), aufgefüllt. Die sogenannte geführte Knochenregeneration (Guided Bone Regeneration – GBR) schafft ein stabiles Widerlager, das das regenerative Potenzial autolog gewonnenen Knochens nutzt, die knöcherne Regeneration in der unbelasteten Region des anterioren Gaumens fördert und einen stabilen Untergrund für den Wundverschluss bildet.
Das Augmentat aus allogenem und autologem Knochen wurde mit einer resorbierbaren Bio-Gide-Membran (Geistlich Pharma AG Wolhusen, Kanton Luzern, Schweiz) sowie einer PRGF-Fibrin-Membran (BTI Deutschland GmbH, Pforzheim, Deutschland) abgedeckt. Diese dienten sowohl zur Stabilisierung der Weichgewebsverhältnisse als auch als Schutzbarriere gegen eine bakterielle Kontamination, um optimale Bedingungen für die knöcherne und die weichgewebige Regeneration zu schaffen, wie in Abbildung 6 dargestellt.
Aufgrund des vorab alio loco abgelaufenen Therapieversuchs, aus dem eine Dehiszenz und damit ein Gewebeverlust am Gaumen zentral über der NPDC resultierte, musste eine ausgedehnte Mobilisation der umliegenden Gewebe durchgeführt werden, um einen spannungsfreien Wundverschluss erreichen zu können. Die subperiostale Präparation der Gaumenschleimhaut bis zur A-Linie erfolgte unter Schonung der Aa. Palatinae majores beidseits, nach Präparation zeigen sich beide Arterien intakt, siehe Abbildung 7.
Hierzu wurden – zusätzlich zur Präparation der Gaumenschleimhaut bis zum weichen Gaumen – vestibulär Entlastungsschnitte in regio 13 und 23 gesetzt. Nach Präparation eines Mukoperiostlappens und Periostschlitzung konnte ausreichend Beweglichkeit im Lappen gewonnen werden (Abbildung 8). Um zu erreichen, dass der Patient seine Prothese ohne aufwendige Unterfütterung durch einen Zahntechniker postoperativ nach Abschluss der Wundheilung wieder tragen kann, wurde versucht, beim Wundverschluss das Vestibulum möglichst wenig zu verschieben. Der spannungsfreie Wundverschluss erfolgte durch horizontale U-Nähte als Haltenaht sowie Einzelknopfnähte zur Adaptation der Wundränder und interdentale Papillennähte mit Ethylon 5/0 (Abbildung 9). Zuvor war die Perforation der Gaumenschleimhaut mittels Vicryl rapid 5/0 von beiden Seiten verschlossen worden. Zur postoperativen Adaptation der Gaumenschleimhaut und Hämatomprophylaxe sowie zum Schutz der Wundfläche wurde die präoperativ angefertigte Verbandsplatte eingegliedert.
Diskussion
Die Entfernung und vor allem der spannungsfreie Wundverschluss einer nasopalatinalen Zyste können eine Herausforderung darstellen. Wenngleich sie lange Zeit unbemerkt und asymptomatisch sein kann, so kann es auch zu einer Infektion und spontanen Perforation der Gaumenschleimhaut kommen, was dazu führt, dass der Befund entfernt werden muss [Anneroth et al., 1986; Swanson et al., 1991; Vasconcelos et al., 1999].
Entwicklungsgeschichtlich stammt die NPDC aus epithelialen Resten des Ductus nasopalatinus, der während der Embryonalentwicklung paarig vorliegt und die Nasenhöhle mit der vorderen Maxilla verbindet. Während der Entwicklung des Gaumens, kommt es durch die Verlagerung der Zunge in der siebten Schwangerschaftswoche zum Verschluss des harten Gaumens, indem der primäre Gaumen (Teil des Zwischenkiefersegments) mit den beiden Gaumensegmenten verschmilzt – hierbei kommt es normalerweise zur Rückbildung des Ductus nasopalatinus [Paulsen et al., 2023; Suter et al., 2011; Thiele und Schilling, 2024]. Obwohl die nasopalatinale Zyste typischerweise asymptomatisch ist, kann sie durch ihr spontan auftretendes Wachstum zu einem erheblichen Defekt in der anterioren Maxilla führen und zudem Symptome wie eine Vorwölbung des Gaumens oder ein Druckgefühl verursachen [Main, 1970]. Röntgenologisch zeigt sie sich als eine gut begrenzte, birnen- oder herzförmige hypodense Läsion, die je nach Ausprägung schon im OPG gut erkennbar sein kann [Dedhia et al., 2013]. Die chirurgische Entfernung stellt die Therapie der Wahl dar.
Eine NPDC wird häufig zufällig entdeckt, dies kann zum Beispiel im Rahmen einer dreidimensionalen Diagnostik zur Implantatplanung geschehen. Als Behandler ist es wichtig, die NPDC von einer physiologischen Erweiterung des Canalis incisivus abzugrenzen. Die Kanalerweiterung stellt eine anatomische Variante des Canalis incisivus dar. Dieser enthält paarig angelegt die A. sphenopalatina, den N. nasopalatinus und den Ductus nasopalatinus. Letzterer atrophiert normalerweise während der embryonalen Entwicklung. Radiologisch zeigt sich eine Kanalerweiterung meist als schmale, symmetrische Struktur im Bereich des Canalis incisivus. Der Canalis incisivus hat in der Regel einen Durchmesser von etwa 2 bis maximal 6 mm [Aranha Neto et al., 2024; Cinn et al., 2009]. Zur Differenzialdiagnostik können – wenn vorhanden – auch alte Röntgenaufnahmen herangezogen werden, um zu untersuchen, ob ein expansives Wachstum vorliegt.
Im Gegensatz zum erweiterten Kanal handelt es sich bei der NPDC um eine echte pathologische Formation. Durch ihr Wachstum kann sie funktionelle und strukturelle Probleme verursachen. Die Zyste erscheint in der radiologischen Bildgebung als runde, gut abgegrenzte, radioluzente Struktur. In fortgeschrittenen Stadien kann sie eine deutliche Expansionstendenz aufweisen, die sogar zu einer Perforation in die Nasenhaupthöhle führen kann. Daher sind eine präzise Diagnosestellung und eine entsprechende Therapie essenziell für den Patienten.
Ein klinisch relevantes Problem stellt die meist asymptomatische nasopalatinale Zyste insbesondere bei der implantologischen Rehabilitation des anterioren Oberkiefers dar. Durch ihr expansives Wachstum kann es zu einer deutlichen Reduktion des vorhandenen Knochenangebots kommen. Die Resorption des knöchernen Gaumens sowie des palatinalen Anteils des Alveolarfortsatzes kann auch die Stabilität und die Prognose von vorhandenen Implantaten negativ beeinflussen. Ohne ausreichendes Knochenangebot ist eine Implantation nicht möglich, was zusätzliche Augmentationsverfahren erforderlich macht und die Behandlungsdauer erheblich verlängert. Es gibt auch Fallberichte über eine Induktion des Wachstums der NPDC nach Implantation [Al-Shamiri et al., 2016; Casado et al., 2008].
Bei der Enukleation der NPDC kann es durch die Verletzung der Aa. sphenopalatinae, die paarig durch den Canalis incisivus verlaufen, zu einer starken Blutung kommen – wie es laut Patient beim alio loco durchgeführten Entfernungsversuch der Fall war. Zusätzlich können eine fehlerhafte Schnittführung oder eine Fistelbildung der NPDC infolge einer sekundären Infektion zu Perforationen der Gaumenschleimhaut und zu einer Dehiszenz führen, was den spannungsfreien Wundverschluss erheblich erschwert. Grundsätzlich sollte der Wundverschluss nie direkt über dem Befund erfolgen, sondern möglichst über einer stabilen knöchernen Unterlage, um eine sichere Heilung zu gewährleisten.
Deshalb sollte die Schnittführung nicht im Punctum maximum des Befunds, der die Gaumenschleimhaut vorwölben kann, liegen, sondern eine marginale Schnittführung erfolgen. Um eine vorhandene Dehiszenz am Gaumen zu verschließen, ist eine ausgedehnte Mobilisation der Gaumenschleimhaut – wie in diesem Fall – notwendig. Niedergelassene Kollegen sollten dabei beachten, dass es bei der Präparation der Gaumenschleimhaut aufgrund der Lagebeziehung zu den beiden Aa. palatinae majores ebenfalls zu erheblichen Blutungsereignissen intraoperativ kommen kann, was nicht nur die Sicht im Operationsfeld erschwert, sondern auch postoperative Komplikationen wie Nachblutungen oder eine Hämatombildung begünstigt.
Liegt keine Dehiszenz vor, kann in vielen Fällen auf eine ausgedehnte Präparation verzichtet werden, wodurch das Blutungsrisiko reduziert wird. Eine Verletzung den Aa. sphenopalatinae ist bei der sorgfältigen Enukleation der NPDC allerdings sehr wahrscheinlich. Die Stärke der Blutung aus den Aa. sphenopalatinae variiert und kann unter Umständen sehr stark sein. Darauf sollte man vorbereitet sein und geeignete Maßnahmen wie Koagulation zur Blutstillung einsetzen.
Die Schleimhaut des harten Gaumens ist stark keratinisiert und wenig elastisch, was eine Mobilisation der Lappen für einen spannungsfreien Verschluss weiter erschwert. Anders als in anderen Regionen der Mundhöhle, in denen die Schleimhaut leicht gedehnt und verschoben werden kann, ist am Gaumen eine direkte Adaption der Wundränder bei einem Gewebedefekt aufgrund von Dehiszenz oder Fistelung schwieriger. Dies führt häufig zu offenen Wundflächen, die sekundär granulieren müssen, was die Heilungsdauer verlängern und das Infektionsrisiko erhöhen kann.
Wie im beschriebenen Fall kann durch eine dreidimensionale präoperative Diagnostik, die sorgsame Präparation der Lappen und eine ausgedehnte Mobilisation von palatinal und vestibulär auch unter diesen Umständen ein spannungsfreier Wundverschluss erreicht werden.
Wenn die NPDC sich weit nach kranial ausdehnt, kann sie alternativ auch durch transnasale Marsupialisation entfernt werden [Cinn et al., 2009; Kagoya et al., 2022; Kim et al., 2023].
Fazit für die Praxis
Die nasopalatinale Zyste ist nicht nur eine diagnostische Herausforderung, sondern auch ein potenzielles Hindernis für eine erfolgreiche implantologische Rehabilitation.
Die Abgrenzung zur einfachen Kanalerweiterung ist essenziell, da eine unbehandelte Zyste das Knochenangebot reduziert, sich sekundär entzünden und langfristig zu Symptomen und Komplikationen führen kann.
Bei der chirurgischen Entfernung stellen das hohe Blutungsrisiko und die anspruchsvolle plastische Deckung – insbesondere bei Vorliegen eines Gewebedefekts – durch die unbewegliche Gaumenschleimhaut eine besondere Herausforderung dar.
Eine vorausschauende chirurgische Planung, die Wahl der geeigneten Entfernungs- und gegebenenfalls Augmentationstechnik sowie eine engmaschige postoperative Kontrolle sind entscheidend, um eine komplikationsfreie Heilung zu gewährleisten.
Postoperative Komplikationen umfassen vor allem Nachblutungen, Infektionen und Wundheilungsstörungen. Aufgrund der schlechten Verschiebbarkeit der palatinalen Schleimhaut kann es zu einer Dehiszenz und einer verzögerten Wundheilung bis hin zu Wundheilungsstörungen kommen. Zudem besteht bei unvollständiger Entfernung der Zyste das Risiko eines Rezidivs, weshalb eine radiologische postoperative Verlaufskontrolle empfehlenswert ist.
Literaturliste
Al-Shamiri, H. M., Elfaki, S., Al-Maweri, S. A., Alaizari, N. A., & Tarakji, B. (2016). Development of Nasopalatine Duct Cyst in Relation to Dental Implant Placement. N Am J Med Sci, 8(1), 13-16. doi.org/10.4103/1947-2714.175187.
Anneroth, G., Hall, G., & Stuge, U. (1986). Nasopalatine duct cyst. International journal of oral and maxillofacial surgery, 15(5), 572-580.
Aranha Neto, I. S., Cruz, W. H. S., Ribeiro, I. C., Oliveira Coutinho, D. C., Ladeira Vidigal, B. C., Carmelo, J. C., Martins-Júnior, P. A., Vespasiano Silva, A. I., Manzi, F. R., & Alves, E. S. M. R. M. (2024). Morphometric study of incisive canal and its anatomic variations in brazilian individuals. Cranio, 42(1), 94-101. doi.org/10.1080/08869634.2021.1887610.
Casado, P. L., Donner, M., Pascarelli, B., Derocy, C., Duarte, M. E. L., & Barboza, E. P. (2008). Immediate Dental Implant Failure Associated With Nasopalatine Duct Cyst. Implant Dentistry, 17(2). journals.lww.com/implantdent/fulltext/2008/06000/immediate_dental_implant_failure_associated_with.7.aspx
Cinn, Y.-G., Park, M.-K., Kang, H. J., & Lee, H.-M. (2009). A case of endoscopic marsupialization of a nasopalatine duct cyst. J Rhinol, 16(2), 152-154.
Dedhia, P., Dedhia, S., Dhokar, A., & Desai, A. (2013). Nasopalatine duct cyst. Case reports in dentistry, 2013(1), 869516.
Kagoya, R., Iwanami, T., Mochizuki, M., Kondo, K., & Ito, K. (2022). Case report: Unilateral transnasal endoscopic marsupialization of nasopalatine duct cyst [Case Report]. Frontiers in Surgery, 9. doi.org/10.3389/fsurg.2022.978915.
Kim, S.-J., Moon, J. W., & Lee, H.-M. (2023). Huge Nasopalatine Duct Cyst Treated by Transnasal Endoscopic Marsupialization: A Case Report and Literature Review. Ear, Nose & Throat Journal, 01455613231177986. doi.org/10.1177/01455613231177986.
Main, D. M. G. (1970). Epithelial jaw cysts: A clinicopathological reappraisal. British Journal of Oral Surgery, 8(2), 114-125. doi.orghttps://doi.org/10.1016/S0007-117X(70)80002-6.
Paulsen, F., Proff, P., & Waschke, J. (2023). Sobotta Atlas der Anatomie für Zahnmedizin. Urban & Fischer. books.google.de/books.
Suter, V. G. A., Sendi, P., Reichart, P. A., & Bornstein, M. M. (2011). The Nasopalatine Duct Cyst: An Analysis of the Relation Between Clinical Symptoms, Cyst Dimensions, and Involvement of Neighboring Anatomical Structures Using Cone Beam Computed Tomography. Journal of Oral and Maxillofacial Surgery, 69(10), 2595-2603. doi.orghttps://doi.org/10.1016/j.joms.2010.11.032.
Swanson, K. S., Kaugars, G. E., & Gunsolley, J. C. (1991). Nasopalatine duct cyst: An analysis of 334 cases. Journal of Oral and Maxillofacial Surgery, 49(3), 268-271. doi.orghttps://doi.org/10.1016/0278-2391(91)90217-A.
Thiele, J., & Schilling, O. (2024). Synonyms: Canalis incisivus-Ductus nasopalatinus?„ The rare is rare…?“. Rofo: Fortschritte auf dem Gebiete der Rontgenstrahlen und der Nuklearmedizin.
Vasconcelos, R., de Aguiar, M. F., Castro, W., de Araújo, V. C., & Mesquita, R. (1999). Retrospective analysis of 31 cases of nasopalatine duct cyst. Oral diseases, 5(4), 325-328.












